خبير طبي في المقال
منشورات جديدة
الورم الأرومي العصبي عند الأطفال: الأسباب والتشخيص والعلاج
آخر مراجعة: 04.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
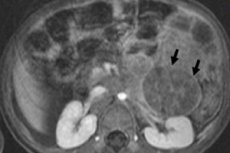
في طب الأورام عند الأطفال، يعد الورم العصبي عند الأطفال أحد أكثر الأورام خارج الجمجمة شيوعًا، وهو ورم خبيث جنيني في الخلايا العصبية الجذعية، أي الخلايا العصبية الجنينية (غير الناضجة) في الجهاز العصبي الودي.
علم الأوبئة
وفقًا لإحصائيات مجموعة مخاطر الأورام العصبية الدولية (INRG)، فإن الأورام العصبية تمثل حوالي 8% من جميع الأمراض الأورامية عند الأطفال في جميع أنحاء العالم وتحتل المرتبة الثالثة من حيث الانتشار، بعد سرطان الدم وأورام المخ.
وفقًا لبيانات أخرى، يُمثل ورم الأرومة العصبية حوالي 28% من جميع حالات السرطان لدى الرضع. يُشخَّص أكثر من ثلث حالات ورم الأرومة العصبية لدى الأطفال دون سن عام واحد؛ ويتراوح متوسط عمر التشخيص بين 19 و22 شهرًا. أكثر من 90% من الحالات المُشخَّصة تحدث لدى الأطفال الذين تتراوح أعمارهم بين سنتين وخمس سنوات (مع غلبة الذكور)؛ ويُلاحظ ذروة الإصابة في سن سنتين إلى ثلاث سنوات، بينما تُمثل حالات الأطفال الذين تزيد أعمارهم عن خمس سنوات أقل من 10%.
الأسباب الأورام الأرومية العصبية
عند دراسة أسباب ورم الخلايا العصبية، خلص الباحثون إلى أن هذا الورم لدى الأطفال يحدث نتيجة طفرات جينية متفرقة خلال مرحلة التكوين الجنيني أو في مراحل النمو المبكرة بعد الولادة. إلا أن أسباب هذه التغيرات الجينية غير معروفة، إذ لم يُحدد تأثير العوامل البيئية المسببة للتشوهات.
يمكن أن تحدث هذه الأورام في أي مكان، بما في ذلك المنصف، والرقبة، والبطن، والغدد الكظرية، والكلى، والعمود الفقري، والحوض.
في حالات نادرة، قد يرتبط ورم الخلايا العصبية لدى الرضع بطفرة وراثية. وتحديدًا، طفرة في جين بروتين الغشاء CD246 على الكروموسوم 2 - إنزيم تيروزين كيناز ALK، الذي يضمن التواصل بين الخلايا ويلعب دورًا هامًا في عمل الجهاز العصبي؛ وفي جين بروتين PHOX2B (على الكروموسوم 4)، الذي يشارك في نضوج الخلايا العصبية.
قد يرتبط الورم العصبي أيضًا بمرض الورم العصبي الليفي من النوع الأول عند الأطفال،ومتلازمة بيكويث-فيدمان ، وانخفاض سكر الدم بسبب فرط الأنسولين (التهاب البنكرياس النيزيدي).
عوامل الخطر
اليوم، تُعتبر الوراثة من عوامل الخطر للإصابة بورم الخلايا العصبية لدى الأطفال، وتشمل وجود هذا الورم في التاريخ العائلي، بالإضافة إلى التشوهات الخلقية المرتبطة بطفرات جينية أثناء النمو داخل الرحم. وينطبق هذا بشكل خاص على حالات ظهور العديد من الأورام في أعضاء مختلفة.
ولم يتمكن الباحثون من تحديد أي من العوامل الخارجية التي تزيد من خطر الإصابة بهذا الورم.
طريقة تطور المرض
آلية تطور أورام الخلايا العصبية البدائية ناتجة عن اضطرابات في تمايز ونضج خلايا العرف العصبي، وهي خطوط خلوية ثنائية الجانب تتشكل على حواف الأنبوب العصبي من الطبقة الجرثومية الخارجية للجنين البشري. تهاجر هذه الخلايا (تتحرك) وتتمايز إلى أنواع عديدة من الخلايا: الخلايا العصبية الحسية واللاإرادية، والخلايا العصبية الصماء، وخلايا نخاع الغدة الكظرية، وخلايا غضروف الوجه والجمجمة، بالإضافة إلى الخلايا الصبغية.
في ورم الخلايا العصبية، لا تنضج الخلايا العصبية المهاجرة، بل تستمر في النمو والانقسام، مُشكّلةً ورمًا. وترتبط آلية تكوّنه بالطفرات الجينية التالية:
- مع مضاعفة جزء من تسلسل الكروموسوم أو مضاعفة أجزاء من جين LMO1 على الكروموسوم 11، مما يشفر بروتين RBTN1 في خلايا القمة العصبية للجنين؛
- مع تغير في عدد نسخ جين NBPF10 على الكروموسوم 1q21.1، المُشفِّر لبروتين DUF1220، الذي يتحكم في تكاثر الخلايا الجذعية العصبية البشرية. تؤدي هذه الاضطرابات إما إلى مضاعفة هذا الكروموسوم أو إلى حذفه - أي غياب جزء من الحمض النووي.
- مع التغيرات في جين قمع الورم ATRX (على الكروموسوم Xq21.1)؛
- بوجود نسخ إضافية (تضخيم) من جين عامل النسخ N-Myc على الكروموسوم 2، والذي يُشفِّر أحد عوامل النسخ (بروتين رابط للحمض النووي) الذي يُنظِّم نشاط الجينات الأخرى ويُنظِّم تكاثر الخلايا السلفية أثناء تكوين البروتينات اللازمة لتكوين أنسجة وأعضاء الجنين. يُحوِّل تضخيم هذا الجين إلى جين ورمي، مما يُؤدي إلى اضطراب دورة الخلية، وزيادة تكاثرها، وتكوين الأورام.
الأعراض الأورام الأرومية العصبية
العلامات الأولى لورم الخلايا العصبية غير محددة وقد تشمل فقدان الشهية (وفقدان الوزن)، والتعب عند التغذية، والحمى، وآلام المفاصل.
تعتمد الأعراض السريرية على موقع الورم الأولي ووجود نقائل (تحدث في 60-73% من الحالات).
في كثير من الأحيان، يتمركز الورم الأرومي العصبي الأولي في نخاع الغدة الكظرية، الذي له أصل مشابه للخلايا العصبية. يُشخَّص الورم الأرومي العصبي الكظري لدى الأطفال دون سن عام واحد بنسبة 35-40% من الحالات. تشمل أعراضه ألمًا في البطن، وحُمّى، وفقدانًا في الوزن، وآلامًا في العظام، وفقر دم، أو متلازمة بيبر المصاحبة: تلف كبدي منتشر مع تضخم كبدي حاد ومتلازمة ضائقة تنفسية.
الورم العصبي خلف الصفاق أو الورم العصبي خلف الصفاق عند الأطفال، ومع نموه يبدأ بالضغط على المثانة أو الأمعاء، مما قد يسبب مشاكل في التبول أو التغوط، وتورم الساقين (عند الأولاد، ينتفخ كيس الصفن).
غالبًا ما يضغط ورم الخلايا العصبية في المنصف عند الأطفال (ورم الخلايا العصبية المنصفية) على الوريد الأجوف العلوي، مما قد يُسبب تورمًا في الوجه والرقبة والذراعين وأعلى الصدر (مع تحول الجلد إلى اللون الأحمر المزرق، مع ظهور عقيدات تحت الجلد). يظهر السعال والصفير، ومشاكل في التنفس (ضيق في التنفس) أو مشاكل في البلع (عسر البلع)؛ ويُلاحظ تضخم في الغدد الليمفاوية في الرقبة، وفوق الترقوة، وتحت الإبطين.
يؤدي انتشار الخلايا السرطانية إلى نخاع العظم إلى فقر الدم وقلة الصفيحات الدموية وقلة الكريات البيض مع الميل إلى النزيف.
ومع انتشار الورم في منطقة حول العين، تظهر هالات سوداء أو كدمات حول العينين. كما يمكن أن يسبب هذا الورم صداعًا ودوارًا، وجحوظًا (انتفاخًا في مقلة العين)، وانخفاضًا في حجم حدقة العين (تضيق الحدقة) نتيجة ضغط النهايات العصبية.
يؤدي ورم الخلايا العصبية البطنية أو ورم الخلايا العصبية في تجويف البطن لدى الأطفال إلى تكوّن أختام محسوسة في البطن، وانتفاخه، وفقدان الشهية، والإمساك، وارتفاع ضغط الدم. ويمكن أن يؤدي ضغط الورم على النخاع الشوكي أو جذر العصب إلى تنميل وضعف في الأطراف، وعدم القدرة على الوقوف أو الزحف أو المشي. وفي حال إصابة العظام، قد يحدث ألم عظمي.
في حالة الورم في المرحلة 3-4 في تجويف البطن مع تلف الغدد الليمفاوية، يمكن أن تدخل خلايا الورم إلى أنسجة الكلى، ومن ثم يتطور ورم عصبي واسع النطاق في الكلى عند الأطفال، مما يؤدي إلى خلل في وظائفها.
مراحل
- الورم العصبي في المرحلة الأولى هو ورم أولي موضعي ومعزول في منطقة واحدة من الجسم؛ ولا تتأثر الغدد الليمفاوية على كلا الجانبين.
- المرحلة الثانية من ورم الخلايا العصبية. في المرحلة 2أ، يقتصر الورم الرئيسي على منطقة واحدة ولكنه كبير الحجم؛ ولا يشمل العقد الليمفاوية الثنائية. في المرحلة 2ب، تكون العقد الليمفاوية في جانب الجسم الذي يقع فيه الورم إيجابية للنقائل.
- المرحلة الثالثة من الورم العصبي: يعبر الورم الأساسي النخاع الشوكي أو خط الوسط للجسم، وتوجد نقائل أحادية أو ثنائية الجانب في العقد الليمفاوية.
- المرحلة الرابعة من ورم الخلايا العصبية: انتشر الورم إلى عقد ليمفاوية بعيدة، أو نخاع العظم، أو العظام، أو الكبد، أو أعضاء أخرى. وتُحدد المرحلة 4S لدى الأطفال دون سن عام واحد الذين يعانون من ورم أولي موضعي، مع انتشار إلى الجلد، أو الكبد، أو نخاع العظم.
نظام تصنيف مخاطر الورم الأرومي العصبي الدولي (INRGSS)
يستخدم INRGSS عوامل الخطر المحددة بالتصوير (IDRFs)، وهي العوامل التي تظهر في اختبارات التصوير والتي قد تعني أن إزالة الورم سيكون أكثر صعوبة.
يقسم INRGSS الأورام العصبية إلى 4 مراحل:
- L1: لم ينتشر الورم من مكانه الأصلي ولم يتوسع إلى هياكل حيوية. يقتصر على جزء واحد من الجسم، كالرقبة أو الصدر أو البطن.
- L2: لم ينتشر الورم (ينتشر) بعيدًا عن المكان الذي بدأ فيه (على سبيل المثال، ربما نما من الجانب الأيسر من البطن إلى الجانب الأيسر من الصدر)، ولكن لديه على الأقل IDRF واحد.
- م: انتشر الورم إلى جزء بعيد من الجسم (باستثناء الأورام في مرحلة التصلب المتعدد).
- MS: مرض نقيلي يصيب الأطفال الذين تقل أعمارهم عن 18 شهرًا، حيث ينتشر السرطان فقط إلى الجلد والكبد و/أو نخاع العظام.
المضاعفات والنتائج
يتميز الورم العصبي الأرومي بمضاعفات وعواقب مثل:
- الانتشار (النقائل) إلى الغدد الليمفاوية ونخاع العظام والكبد والجلد والعظام؛
- ضغط الحبل الشوكي (الذي يمكن أن يسبب الألم ويؤدي إلى الشلل)؛
- تطور متلازمة الورم الحليمي (بسبب عمل بعض المواد الكيميائية التي يفرزها الورم، بالإضافة إلى مستضد ديسيالوجانجليوزيد GD2 الذي تعبر عنه خلاياه)، والذي يتجلى في حركات العين اللاإرادية السريعة، وضعف التنسيق، وتشنجات العضلات، والإسهال؛
- الانتكاسات بعد الانتهاء من العلاج الأساسي (كما تظهر الممارسة السريرية، فإن أورام الخلايا العصبية عالية الخطورة تعاني من الانتكاس في 50٪ من الحالات).
التشخيص الأورام الأرومية العصبية
يتطلب تشخيص الإصابة بورم الخلايا العصبية المشتبه به عند الطفل إجراء فحص واختبارات مخبرية وتصوير.
تُجرى فحوصات الدم والبول للكشف عن الكاتيكولامينات (النورإبينفرين والدوبامين) وأحماض الهوموفانيليك أو الفانيليلماندليك (التي تتكون أثناء استقلاب هذه الهرمونات)؛ وفحص دم للإينولاز العصبي النوعي، واختبار الممتز المناعي المرتبط بالإنزيم (ELISA) لمصل الدم، وتحليل نخاع العظم (تُؤخذ عينة منه ببزل الشفط). يُجرى اختبار الحمض النووي لتحديد الطفرات، وتُؤخذ خزعة لفحص الشكل الخلوي لأنسجة الورم.
بعد أخذ عينات الخزعة، تُرسل إلى المختبر حيث يُفحصها تحت المجهر أخصائي علم الأمراض (طبيب مُدرّب على تحديد الخلايا السرطانية). كما تُجرى غالبًا فحوصات معملية خاصة على العينات لتحديد ما إذا كان الورم ورمًا عصبيًا.
إذا كان الأمر يتعلق بورم الخلايا العصبية، فإن الاختبارات المعملية يمكن أن تساعد أيضًا في تحديد مدى سرعة نمو الورم أو انتشاره، بالإضافة إلى العلاجات التي قد تعمل بشكل أفضل.
يصور التشخيص الآلي الورم باستخدام الموجات فوق الصوتية أو الأشعة السينية أو التصوير بالرنين المغناطيسي أو التصوير المقطعي المحوسب أو التصوير بالإصدار البوزيتروني مع إدخال مسح 18F-fluorodeoxyglucose أو MIBG - التصوير الومضاني باستخدام ميتا أيودوبنزيل جوانيدين. [ 1 ]
تشخيص متباين
يتضمن التشخيص التفريقي الورم العصبي العقدي الحميد، وورم الخلايا العصبية العقدية، وورم العضلات المخططة، وورم الخلايا الكلوية.
من الاتصال؟
علاج او معاملة الأورام الأرومية العصبية
في حالة ورم الخلايا العصبية، يعتمد العلاج على فئة الخطر لدى المريض (مرحلة تطور الورم)، وموقع الورم، والخصائص الجينومية لخلايا الورم، وعمر الطفل. وقد يشمل ذلك المراقبة، والجراحة، والعلاج الكيميائي، والعلاج الإشعاعي، والعلاج المناعي، وزراعة الخلايا الجذعية المكونة للدم.
يُعطى العلاج الكيميائي قبل الجراحة أو بعدها لأورام الخلايا العصبية لدى الأطفال، كما هو الحال مع أي علاج كيميائي للسرطان ، على دفعات: يُعطى الدواء لعدة أيام متتالية، تليها فترة استراحة لتعافي الجسم. عادةً ما تتكرر الدورات كل ثلاثة إلى أربعة أسابيع.
يتم استخدام الأدوية التالية (ومجموعاتها): سيكلوفوسفاميد، سيسبلاتين أو كاربوبلاتين، دوكسوروبيسين (أدرياميسين)، فينكريستين، إيتوبوسيد.
تشمل الآثار الجانبية الشائعة لأدوية العلاج الكيميائي تساقط الشعر، وفقدان الشهية، والتعب، والغثيان والقيء، وقرح الفم، والإسهال، أو الإمساك. كما يمكن أن يُلحق العلاج الكيميائي الضرر بنخاع العظم، ويسبب انخفاضًا في عدد خلايا الدم.
يستخدم العلاج المناعي المُوَجَّه (المُوَجَّه لمستضد الورم GD2) أدوية من مجموعة الأجسام المضادة وحيدة النسيلة (مضادات GD2 MAb) دينوتوكسيماب (يونيتوكسين) وناكسيتاماب. تُعطى هذه الأدوية عن طريق الوريد بالتسريب المُطوّل، بالتزامن مع عامل تحفيز مستعمرات الخلايا المحببة والبلعمية (السيتوكين GM-CSF) والإنترلوكين-2.
تشمل الآثار الجانبية لهذه الأدوية الألم (غالباً ما يكون شديداً جداً)، وانخفاض ضغط الدم، وزيادة معدل ضربات القلب، وضيق التنفس (مع احتمال تورم مجاري الهواء)، وارتفاع درجة الحرارة، والغثيان، والقيء والإسهال، والتغيرات في التركيب الخلوي والمعدني للدم.
لتقليل خطر تكرار الإصابة بالسرطان بعد العلاج الكيميائي بجرعات عالية وزرع الخلايا الجذعية، يتم علاج الأطفال المصابين بالورم الأرومي العصبي عالي الخطورة باستخدام الريتينويدات الجهازية وحمض الريتينويك 13-سيس (إيزوتريتينوين). [ 2 ]
العلاج الجراحي لورم الخلايا العصبية - إزالة الورم، على سبيل المثال، استئصال الغدة الكظرية المفتوح أو استئصال ورم الخلايا العصبية الكظرية بالمنظار؛ استئصال الغدد الليمفاوية (إزالة العقد الليمفاوية المصابة)، إلخ. [ 3 ]
بالنسبة لأورام الخلايا العصبية عالية الخطورة، قد يتم استخدام العلاج الإشعاعي.[ 4 ]
الوقاية
نظرًا لأسباب ورم الخلايا العصبية لدى الأطفال، قد يكون الإجراء الوقائي الوحيد هو الاستشارة الوراثية عند التخطيط للحمل. مع ذلك، تجدر الإشارة إلى أن هذا الورم يرتبط بطفرات وراثية في 1-2% فقط من الحالات.
توقعات
لدى الورم العصبي الطفلي القدرة على التراجع تلقائيًا.
العلامات التشخيصية
- الأورام عالية الخطورة، وكذلك الأورام العصبية لدى الأطفال من جميع الفئات العمرية وجميع المراحل (باستثناء المرحلة 4S) - مع زيادة التعبير عن جين N-MYC وتضخيم الجين الورمي N-Myc - لها تشخيص غير موات يؤثر على متوسط العمر المتوقع.
- وجود خلايا ورمية تفتقر إلى أجزاء معينة من الكروموسومين 1 أو 11 (المعروفة بحذف 1p أو 11q) له تشخيص أسوأ. كما يرتبط وجود جزء إضافي من الكروموسوم 17 (زيادة 17q) بتشخيص أسوأ.
- تتمتع خلايا الورم العصبي التي تحتوي على كمية كبيرة من الحمض النووي بتشخيص أفضل، وخاصة للأطفال الذين تقل أعمارهم عن سنتين.
- الأورام العصبية التي تحتوي على عدد أكبر من مستقبلات عامل نمو الأعصاب، وخاصة مستقبل عامل نمو الأعصاب TrkA، لها تشخيص أفضل.
مجموعة مخاطر البقاء على قيد الحياة حسب مجموعة أورام الطفولة (COG)
- المجموعة منخفضة الخطورة: يتمتع الأطفال في المجموعة منخفضة الخطورة بمعدل بقاء على قيد الحياة لمدة 5 سنوات يزيد عن 95%.
- مجموعة الخطر المتوسط: يبلغ معدل البقاء على قيد الحياة لمدة 5 سنوات للأطفال في مجموعة الخطر المتوسط ما بين 90% إلى 95%.
- المجموعة عالية الخطورة: يبلغ معدل البقاء على قيد الحياة لمدة خمس سنوات لدى الأطفال في المجموعة عالية الخطورة حوالي 50%.
يُعزى حوالي 15% من وفيات سرطان الأطفال إلى ورم الخلايا العصبية. ولا تتجاوز فرص البقاء على قيد الحياة على المدى الطويل لهذا الورم الخبيث عالي الخطورة 40%. ويتراوح معدل البقاء الإجمالي لمدة خمس سنوات بين 67% و74%، منها 43% في الفئة العمرية من سنة إلى أربع سنوات، وأكثر من 80% في حالة ورم الخلايا العصبية الذي يُشخَّص في السنة الأولى من العمر.
Использованная литература

