خبير طبي في المقال
منشورات جديدة
تشخيص الفصال العظمي المفصلي: التصوير بالرنين المغناطيسي
آخر مراجعة: 04.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
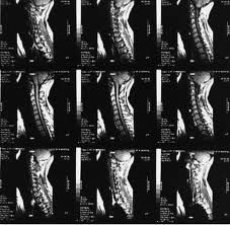
أصبح التصوير بالرنين المغناطيسي (MRI) من أبرز الطرق غير الجراحية لتشخيص هشاشة العظام في السنوات الأخيرة. منذ سبعينيات القرن الماضي، عندما استُخدمت مبادئ الرنين المغناطيسي (MRI) لأول مرة لدراسة جسم الإنسان، شهدت هذه الطريقة في التصوير الطبي تطورًا جذريًا وسريعًا.
يجري تحسين المعدات التقنية والبرمجيات، وتطوير أساليب التقاط الصور، وعوامل التباين في التصوير بالرنين المغناطيسي. هذا يتيح اكتشاف مجالات تطبيق جديدة للتصوير بالرنين المغناطيسي باستمرار. بعد أن اقتصر استخدامه في البداية على دراسات الجهاز العصبي المركزي، يُستخدم التصوير بالرنين المغناطيسي الآن بنجاح في جميع مجالات الطب تقريبًا.
في عام ١٩٤٦، اكتشف فريقان من الباحثين من جامعتي ستانفورد وهارفارد، بشكل مستقل، ظاهرة تُسمى الرنين المغناطيسي النووي (NMR). يكمن جوهرها في أن نوى بعض الذرات، الموجودة في مجال مغناطيسي، تحت تأثير مجال كهرومغناطيسي خارجي، قادرة على امتصاص الطاقة ثم إصدارها على شكل إشارة راديو. وقد مُنح ف. بلوخ وإي. بارميل جائزة نوبل عام ١٩٥٢ عن هذا الاكتشاف. وسرعان ما استُخدمت هذه الظاهرة الجديدة في التحليل الطيفي للهياكل البيولوجية (مطيافية الرنين المغناطيسي النووي). في عام ١٩٧٣، أظهر بول راوتنبرغ لأول مرة إمكانية الحصول على صورة باستخدام إشارات الرنين المغناطيسي النووي. وهكذا ظهر التصوير المقطعي بالرنين المغناطيسي النووي. وقد عُرضت أول صور مقطعية بالرنين المغناطيسي النووي للأعضاء الداخلية لشخص حي عام ١٩٨٢ في المؤتمر الدولي لأطباء الأشعة في باريس.
يجب توضيح أمرين. على الرغم من أن هذه الطريقة تعتمد على ظاهرة الرنين المغناطيسي النووي، إلا أنها تُسمى بالرنين المغناطيسي (MR)، مع حذف كلمة "نووي". ويتم ذلك لتجنّب فكرة النشاط الإشعاعي المرتبط بتحلل النوى الذرية. أما الشرط الثاني، فهو أن أجهزة التصوير بالرنين المغناطيسي لا تُضبط بالصدفة على البروتونات، أي نوى الهيدروجين. يوجد هذا العنصر بكثرة في الأنسجة، وتتمتع نواته بأكبر عزم مغناطيسي بين جميع النوى الذرية، مما يُحدد مستوى إشارة الرنين المغناطيسي المرتفع نسبيًا.
إذا كان عدد الأجهزة المناسبة للأبحاث السريرية في العالم في عام ١٩٨٣ محدودًا، فإنه بحلول بداية عام ١٩٩٦، بلغ عدد أجهزة التصوير المقطعي العاملة حوالي ١٠٠٠٠ جهاز حول العالم. ويتم إدخال ألف جهاز جديد إلى الخدمة سنويًا. أكثر من ٩٠٪ من أجهزة التصوير المقطعي بالرنين المغناطيسي هي نماذج مزودة بمغناطيسات فائقة التوصيل (٠.٥-١.٥ تسلا). ومن الجدير بالذكر أنه في منتصف الثمانينيات، كانت الشركات المصنعة لأجهزة التصوير المقطعي بالرنين المغناطيسي تسترشد بمبدأ "كلما ارتفع المجال، كان ذلك أفضل"، مع التركيز على نماذج ذات مجال ١.٥ تسلا فأكثر، إلا أنه بحلول نهاية الثمانينيات، اتضح أنها لا تتمتع بمزايا جوهرية في معظم مجالات التطبيق مقارنةً بالنماذج ذات شدة المجال المتوسطة. لذلك، يُولي المُصنِّعون الرئيسيون لأجهزة التصوير المقطعي بالرنين المغناطيسي (جنرال إلكتريك، سيمنز، فيليبس، توشيبا، بيكر، بروكر، وغيرها) اهتمامًا كبيرًا حاليًا لإنتاج نماذج ذات مجالات متوسطة وحتى منخفضة، والتي تختلف عن أنظمة المجالات العالية من حيث صغر حجمها وكفاءتها، مع جودة صورة مُرضية وتكلفة أقل بكثير. تُستخدم أنظمة المجالات العالية بشكل رئيسي في مراكز الأبحاث في مجال مطيافية الرنين المغناطيسي.
مبدأ طريقة التصوير بالرنين المغناطيسي
المكونات الرئيسية لجهاز التصوير بالرنين المغناطيسي هي: مغناطيس فائق القوة، وجهاز إرسال لاسلكي، وملف استقبال ترددات لاسلكية، وجهاز كمبيوتر، ولوحة تحكم. تحتوي معظم الأجهزة على مجال مغناطيسي بعزم مغناطيسي موازٍ للمحور الطولي لجسم الإنسان. تُقاس قوة المجال المغناطيسي بوحدة تسلا (T). في التصوير بالرنين المغناطيسي السريري، تُستخدم مجالات بقوة تتراوح بين 0.2 و1.5 تسلا.
عندما يوضع المريض في مجال مغناطيسي قوي، تدور جميع البروتونات، وهي ثنائيات أقطاب مغناطيسية، في اتجاه المجال الخارجي (مثل إبرة البوصلة الموجهة نحو المجال المغناطيسي للأرض). بالإضافة إلى ذلك، تبدأ المحاور المغناطيسية لكل بروتون في الدوران حول اتجاه المجال المغناطيسي الخارجي. تسمى هذه الحركة الدورانية المحددة المسير، ويسمى ترددها التردد الرنيني. عندما تمر نبضات تردد راديوي كهرومغناطيسي قصيرة عبر جسم المريض، يتسبب المجال المغناطيسي للموجات الراديوية في دوران العزوم المغناطيسية لجميع البروتونات حول العزم المغناطيسي للمجال الخارجي. ولكي يحدث هذا، يجب أن يكون تردد الموجات الراديوية مساويًا لتردد رنين البروتونات. تسمى هذه الظاهرة بالرنين المغناطيسي. لتغيير اتجاه البروتونات المغناطيسية، يجب أن يتردد المجال المغناطيسي للبروتونات والموجات الراديوية، أي أن يكون لهما نفس التردد.
يُنشأ عزم مغناطيسي صافي في أنسجة المريض: تُمغنط الأنسجة، وتُوجَّه مغناطيسيتها بالتوازي التام مع المجال المغناطيسي الخارجي. تتناسب المغناطيسية طرديًا مع عدد البروتونات في وحدة حجم الأنسجة. العدد الهائل من البروتونات (نوى الهيدروجين) الموجودة في معظم الأنسجة يعني أن العزم المغناطيسي الصافي كبير بما يكفي لتحريض تيار كهربائي في ملف استقبال موجود خارج المريض. تُستخدم إشارات الرنين المغناطيسي المُستحثة هذه لإعادة بناء صورة الرنين المغناطيسي.
تُسمى عملية انتقال إلكترونات النواة من حالة الإثارة إلى حالة التوازن بعملية استرخاء الشبكة المغزلية أو الاسترخاء الطولي. وتتميز بـ T1 - زمن استرخاء الشبكة المغزلية - وهو الوقت اللازم لنقل 63% من النوى إلى حالة التوازن بعد إثارتها بنبضة 90 درجة. كما يتميز T2 - زمن استرخاء الشبكة المغزلية.
هناك عدة طرق للحصول على صور الرنين المغناطيسي المقطعية. وهي تختلف في ترتيب وطبيعة توليد نبضات الترددات الراديوية وطرق تحليل إشارة الرنين المغناطيسي. الطريقتان الأكثر استخدامًا هما الشبكة المغزلية والصدى المغزلي. تحلل الشبكة المغزلية بشكل أساسي وقت استرخاء T1. تحتوي الأنسجة المختلفة (المادة الرمادية والبيضاء في الدماغ، والسائل النخاعي، وأنسجة الورم، والغضاريف، والعضلات، وما إلى ذلك) على بروتونات ذات أوقات استرخاء T1 مختلفة. ترتبط شدة إشارة الرنين المغناطيسي بمدة T1: فكلما كانت T1 أقصر، زادت شدة إشارة الرنين المغناطيسي وظهرت المنطقة المحددة من الصورة أكثر سطوعًا على شاشة التلفزيون. تظهر الأنسجة الدهنية باللون الأبيض في صور الرنين المغناطيسي المقطعية، يليها الدماغ والحبل الشوكي، والأعضاء الداخلية الكثيفة، والجدران الوعائية والعضلات بترتيب تنازلي لشدة إشارة الرنين المغناطيسي. لا ينتج الهواء والعظام والتكلسات إشارة رنين مغناطيسي عمليًا، وبالتالي يتم عرضها باللون الأسود. إن علاقات وقت الاسترخاء T1 هذه تخلق المتطلبات الأساسية لتصور الأنسجة الطبيعية والمتغيرة في عمليات مسح التصوير بالرنين المغناطيسي.
في طريقة أخرى للتصوير بالرنين المغناطيسي، تُسمى صدى الدوران، تُوجَّه سلسلة من نبضات الترددات الراديوية نحو المريض، مما يُؤدي إلى تدوير البروتونات المُسبقة بزاوية 90 درجة. بعد توقف النبضات، تُسجَّل إشارات استجابة الرنين المغناطيسي. مع ذلك، تختلف شدة إشارة الاستجابة بمدة المرحلة الثانية (T2): فكلما قصرت المرحلة الثانية، ضعفت الإشارة، وبالتالي انخفض سطوع التوهج على شاشة التلفزيون. وبالتالي، تكون صورة الرنين المغناطيسي النهائية باستخدام طريقة المرحلة الثانية (T2) معاكسة لصورة المرحلة الأولى (حيث إن الصورة السلبية تُعاكس الصورة الإيجابية).
تُظهر صور الرنين المغناطيسي المقطعية الأنسجة الرخوة بشكل أفضل من التصوير المقطعي المحوسب: العضلات، وطبقات الدهون، والغضاريف، والأوعية الدموية. تستطيع بعض الأجهزة إنتاج صور للأوعية الدموية دون حقن عامل تباين (تصوير الأوعية الدموية بالرنين المغناطيسي). ونظرًا لانخفاض محتوى الماء في أنسجة العظام، فإن هذه الأخيرة لا تُحدث تأثيرًا واقيًا، كما هو الحال في التصوير المقطعي المحوسب بالأشعة السينية، أي أنها لا تتداخل مع صورة الحبل الشوكي، والأقراص الفقرية، وغيرها. وبالطبع، لا تقتصر نوى الهيدروجين على الماء فحسب، بل إنها في أنسجة العظام مثبتة في جزيئات كبيرة جدًا وهياكل كثيفة، ولا تتداخل مع التصوير بالرنين المغناطيسي.
مزايا وعيوب التصوير بالرنين المغناطيسي
تشمل المزايا الرئيسية للتصوير بالرنين المغناطيسي عدم التدخل الجراحي، وعدم التعرض للإشعاع، والطبيعة ثلاثية الأبعاد لالتقاط الصور، والتباين الطبيعي الناتج عن حركة الدم، وعدم وجود أي تشوهات في أنسجة العظام، والتمييز الدقيق للأنسجة الرخوة، والقدرة على إجراء التحليل الطيفي متعدد الأطياف (MP) لدراسات استقلاب الأنسجة داخل الجسم الحي. يتيح التصوير بالرنين المغناطيسي الحصول على صور لطبقات رقيقة من جسم الإنسان في أي مقطع - في المستويات الأمامية والسهمية والمحورية والمائلة. كما يُمكن إعادة بناء صور حجمية للأعضاء، ومزامنة التقاط الصور المقطعية مع تخطيط كهربية القلب.
تشمل العيوب الرئيسية عادةً الوقت الطويل نسبيًا المطلوب للحصول على الصور (عادةً دقائق)، مما يؤدي إلى ظهور آثار من الحركات التنفسية (وهذا يقلل بشكل خاص من فعالية فحص الرئة)، وعدم انتظام ضربات القلب (في فحص القلب)، وعدم القدرة على اكتشاف الحصوات والتكلسات وبعض أنواع أمراض العظام بشكل موثوق، والتكلفة العالية للمعدات وتشغيلها، والمتطلبات الخاصة للأماكن التي توجد فيها الأجهزة (الحماية من التداخل)، وعدم القدرة على فحص المرضى الذين يعانون من الخوف من الأماكن المغلقة، وأجهزة تنظيم ضربات القلب الاصطناعية، والغرسات المعدنية الكبيرة المصنوعة من المعادن غير الطبية.
 [ 8 ]، [ 9 ]، [ 10 ]، [ 11 ]، [ 12 ]، [ 13 ]، [ 14 ]، [ 15 ]
[ 8 ]، [ 9 ]، [ 10 ]، [ 11 ]، [ 12 ]، [ 13 ]، [ 14 ]، [ 15 ]
عوامل التباين للتصوير بالرنين المغناطيسي
في بداية استخدام التصوير بالرنين المغناطيسي، كان يُعتقد أن التباين الطبيعي بين الأنسجة المختلفة يُغني عن استخدام عوامل التباين. وسرعان ما اكتُشف أن اختلاف الإشارات بين الأنسجة المختلفة، أي تباين صورة الرنين المغناطيسي، يُمكن تحسينه بشكل ملحوظ باستخدام عوامل التباين. ومع توفر أول عامل تباين للرنين المغناطيسي (يحتوي على أيونات غادولينيوم بارامغناطيسية) تجاريًا، ازداد محتوى المعلومات التشخيصية للرنين المغناطيسي بشكل ملحوظ. يكمن جوهر استخدام عوامل التباين في الرنين المغناطيسي في تغيير المعلمات المغناطيسية لبروتونات الأنسجة والأعضاء، أي تغيير زمن استرخاء بروتونات T1 وT2. واليوم، توجد عدة تصنيفات لعوامل التباين في الرنين المغناطيسي (أو بالأحرى عوامل التباين - CA).
وفقًا للتأثير السائد على وقت الاسترخاء، يتم تقسيم MR-KA إلى:
- T1-CA، التي تُقصّر T1، وبالتالي تزيد من شدة إشارة MP في الأنسجة. تُسمى أيضًا CA إيجابية.
- عوامل النسخ T2-CA التي تقصر T2، مما يقلل من شدة إشارة الرنين المغناطيسي. هذه عوامل نسخ سالبة.
اعتمادًا على خصائصها المغناطيسية، يتم تقسيم MR-CA إلى بارامغناطيسية وفائقة البارامغناطيسية:
 [ 16 ]، [ 17 ]، [ 18 ]، [ 19 ]، [ 20 ]
[ 16 ]، [ 17 ]، [ 18 ]، [ 19 ]، [ 20 ]
عوامل التباين البارامغناطيسية
تتميز الذرات ذات إلكترون واحد أو أكثر غير متزاوج بخواص بارامغناطيسية. وهذه الأيونات هي أيونات غادولينيوم (Gd)، والكروم، والنيكل، والحديد، والمنغنيز. وقد حظيت مركبات غادولينيوم بأوسع التطبيقات السريرية. ويعود تأثير التباين للغادولينيوم إلى تقصير زمن الاسترخاء T1 وT2. ففي الجرعات المنخفضة، يسود التأثير على T1، مما يزيد من شدة الإشارة. أما في الجرعات العالية، فيسود التأثير على T2، مما يقلل من شدة الإشارة. وتُستخدم البارامغناطيسات الآن على نطاق واسع في الممارسة التشخيصية السريرية.
عوامل التباين الفائقة المغناطيسية
التأثير السائد لأكسيد الحديد فائق المغناطيسية هو تقصير فترة استرخاء T2. مع زيادة الجرعة، تنخفض شدة الإشارة. يمكن أيضًا إدراج المواد المغناطيسية الحديدية، التي تشمل أكاسيد الحديد المغناطيسية الحديدية التي تشبه هيكليًا فيريت المغنتيت (Fe≥...
يعتمد التصنيف التالي على الحركية الدوائية لـ CA (Sergeev PV et al.، 1995):
- خارج الخلية (غير محدد للأنسجة)؛
- الجهاز الهضمي؛
- عضوي (محدد للأنسجة)؛
- الجزيئات الكبيرة، والتي تستخدم لتحديد المساحة الوعائية.
في أوكرانيا، تُعرف أربعة أنواع من مُركّبات التصلب اللويحي بالرنين المغناطيسي (MR-CA)، وهي مُركّبات تصلب لولبي بارامغناطيسي قابل للذوبان في الماء خارج الخلية، ويُستخدم منها غادودياميد وحمض غادوبنتيتيك على نطاق واسع. أما المجموعات المتبقية من مُركّبات التصلب اللويحي (2-4) فتخضع لتجارب سريرية في الخارج.
MR-CA القابل للذوبان في الماء خارج الخلية
الاسم الدولي |
الصيغة الكيميائية |
بناء |
حمض الجادوبنتيتيك |
غادولينيوم ديميغلومين ثنائي إيثيلين ثلاثي أمين خماسي أسيتات ((NMG)2Gd-DTPA) |
خطي، أيوني |
حمض الجادوتيريك |
(NMG)Gd-DOTA |
دوري، أيوني |
غادودياميد |
غادولينيوم ثنائي إيثيلين ثلاثي أمين بنتا أسيتات-ثنائي ميثيل أميد (Gd-DTPA-BMA) |
خطي، غير أيوني |
جادوتيريدول |
Gd-HP-D03A |
دوري، غير أيوني |
يتم إعطاء CA خارج الخلية عن طريق الوريد، ويتم إفراز 98٪ منها عن طريق الكلى، ولا تخترق حاجز الدم الدماغي، ولها سمية منخفضة، وتنتمي إلى مجموعة المواد المغناطيسية.
موانع التصوير بالرنين المغناطيسي
تشمل موانع الاستعمال المطلقة الحالات التي يُشكل فيها الفحص خطرًا على حياة المرضى. على سبيل المثال، وجود غرسات تُفعّل إلكترونيًا أو مغناطيسيًا أو ميكانيكيًا - وهي في المقام الأول أجهزة تنظيم ضربات قلب اصطناعية. قد يُعطّل التعرض لإشعاع الترددات الراديوية من جهاز التصوير بالرنين المغناطيسي عمل جهاز تنظيم ضربات القلب الذي يعمل بنظام الطلب، لأن تغيرات المجالات المغناطيسية قد تُحاكي نشاط القلب. كما قد يُؤدي الجذب المغناطيسي إلى انزلاق جهاز تنظيم ضربات القلب في تجويفه وتحريك الأقطاب الكهربائية. بالإضافة إلى ذلك، يُشكّل المجال المغناطيسي عوائق أمام عمل غرسات الأذن الوسطى المغناطيسية أو الإلكترونية. يُعدّ وجود صمامات القلب الاصطناعية أمرًا خطيرًا، ويُعدّ موانع استعمال مطلقة فقط عند فحصها باستخدام أجهزة التصوير بالرنين المغناطيسي ذات المجالات العالية، وفي حال الاشتباه سريريًا بتلف الصمام. تشمل موانع الاستعمال المطلقة للفحص أيضًا وجود غرسات جراحية معدنية صغيرة (مشابك إيقاف النزيف) في الجهاز العصبي المركزي، لأن إزاحتها بسبب الجذب المغناطيسي تُهدد بالنزيف. يُشكّل وجودها في أجزاء أخرى من الجسم خطرًا أقل، إذ يُساعد التليف وتغليف المشابك بعد العلاج على الحفاظ على ثباتها. ومع ذلك، بالإضافة إلى الخطر المُحتمل، فإن وجود غرسات معدنية ذات خصائص مغناطيسية يُسبب تشوهات تُصعّب تفسير نتائج الدراسة.
موانع التصوير بالرنين المغناطيسي
مطلق: |
نسبي: |
أجهزة تنظيم ضربات القلب |
منبهات أخرى (مضخات الأنسولين، منبهات الأعصاب) |
غرسات الأذن الوسطى المغناطيسية أو الإلكترونية |
غرسات الأذن الداخلية غير المغناطيسية، وصمامات القلب الاصطناعية (في المجالات العالية، إذا كان هناك اشتباه في وجود خلل وظيفي) |
مشابك وقف النزيف للأوعية الدماغية |
مشابك وقف النزيف في أماكن أخرى، قصور القلب غير المعوض، الحمل، الخوف من الأماكن المغلقة، الحاجة إلى مراقبة فسيولوجية |
تشمل موانع الاستعمال النسبية، بالإضافة إلى تلك المذكورة أعلاه، قصور القلب اللا تعويضي، والحاجة إلى مراقبة فسيولوجية (التهوية الميكانيكية، ومضخات التسريب الكهربائية). يُمثل الخوف من الأماكن المغلقة عائقًا أمام الدراسة في 1-4% من الحالات. ويمكن التغلب عليه، من جهة، باستخدام أجهزة ذات مغناطيس مفتوح، ومن جهة أخرى، من خلال شرح مفصل للجهاز ومسار الفحص. لا يوجد دليل على وجود تأثير ضار للتصوير بالرنين المغناطيسي على الجنين، ولكن يُنصح بتجنبه في الأشهر الثلاثة الأولى من الحمل. يُنصح باستخدام التصوير بالرنين المغناطيسي أثناء الحمل في الحالات التي لا تُقدم فيها طرق التصوير التشخيصي غير المؤينة الأخرى معلومات مُرضية. يتطلب فحص التصوير بالرنين المغناطيسي مشاركة أكبر من المريض مقارنةً بالتصوير المقطعي المحوسب، لأن حركات المريض أثناء الفحص لها تأثير أكبر بكثير على جودة الصور، لذلك غالبًا ما يكون فحص المرضى الذين يعانون من أمراض حادة، وضعف الوعي، والحالات التشنجية، والخرف، وكذلك الأطفال، أمرًا صعبًا.

