خبير طبي في المقال
منشورات جديدة
الثآليل التناسلية: الأسباب والأعراض والتشخيص والعلاج
آخر مراجعة: 07.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
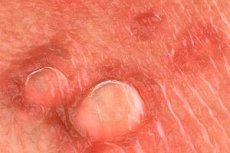
يمكن لأكثر من 20 نوعًا من فيروس الورم الحليمي البشري (HPV) أن يصيب الجهاز التناسلي. معظم حالات عدوى فيروس الورم الحليمي البشري تكون بدون أعراض، أو دون أعراض سريرية، أو غير مكتشفة. عادةً ما تُسبب أنواع فيروس الورم الحليمي البشري 6 أو 11 الثآليل التناسلية المرئية. ترتبط أنواع أخرى من فيروس الورم الحليمي البشري، والتي يمكن عزلها من المنطقة الشرجية التناسلية (مثل الأنواع 16 و18 و31 و33 و35)، ارتباطًا وثيقًا بخلل تنسج عنق الرحم. يمكن تأكيد تشخيص الثآليل التناسلية عن طريق الخزعة، على الرغم من أن الخزعة نادرًا ما تكون ضرورية (مثلًا في الحالات المعقدة، وفشل العلاج القياسي، وتفاقم الحالة السريرية أثناء العلاج، وكبت المناعة، والثآليل المصطبغة/المتصلبة/المتقرحة). لا توجد بيانات تدعم استخدام اختبار الحمض النووي لفيروس الورم الحليمي البشري الخاص بنوع معين في التشخيص الروتيني أو علاج المرضى الذين يعانون من ثآليل تناسلية مرئية.
يمكن أن يُسبب النوعان B و11 من فيروس الورم الحليمي البشري أيضًا ثآليل في المهبل، وعنق الرحم، وداخل مجرى البول، والشرج. تظهر الثآليل الشرجية بشكل رئيسي لدى المرضى الذين يمارسون الجماع الشرجي، وهي تختلف عن الثآليل حول الشرج، والتي قد تظهر لدى الرجال والنساء الذين لا يمارسون الجماع الشرجي. بالإضافة إلى الآفات التناسلية، يمكن أن تُسبب هذه الأنواع من فيروس الورم الحليمي البشري ثآليل في الملتحمة، والبلعوم الأنفي، وتجويف الفم. نادرًا ما يرتبط النوعان 6 و11 من فيروس الورم الحليمي البشري بسرطان الخلايا الحرشفية الغازي في الأعضاء التناسلية الخارجية. وحسب حجمها وموقعها التشريحي، قد تكون الثآليل التناسلية مؤلمة، وسهلة الكدمات، و/أو مُسببة للحكة.
نادرًا ما توجد أنواع فيروس الورم الحليمي البشري 16، 18، 31، 33، 35 في الثآليل التناسلية المرئية، وترتبط بنمو الخلايا الحرشفية داخل الظهارة (سرطان الخلايا الحرشفية الموضعي، ورم بويني حطاطي، وداء كويرات الأحمر، ومرض باوي). ترتبط هذه الأنواع بخلل التنسج داخل الظهارة في المهبل والشرج وعنق الرحم، وسرطان الخلايا الحرشفية. قد يُصاب المرضى الذين يعانون من ثآليل تناسلية مرئية بأنواع متعددة من فيروس الورم الحليمي البشري في وقت واحد.
علاج الثآليل التناسلية
الهدف الأساسي من علاج الثآليل التناسلية المرئية هو إزالة الثآليل التي تُسبب أعراضًا. قد يُؤدي العلاج إلى فترة خالية من الثآليل. غالبًا ما لا تُسبب الثآليل التناسلية أي أعراض. لا يُغير أي من العلاجات المتاحة حاليًا المسار الطبيعي لعدوى فيروس الورم الحليمي البشري أو يقضي عليها. قد تُقلل إزالة الثآليل من قدرتها على العدوى أو لا تُقللها. إذا تُركت الثآليل التناسلية المرئية دون علاج، فقد تختفي من تلقاء نفسها، أو تبقى دون تغيير، أو يزداد حجمها. لا يوجد دليل على أن علاج الثآليل المرئية سيؤثر على تطور سرطان عنق الرحم.
أنظمة علاج الثآليل التناسلية
ينبغي أن يعتمد اختيار علاج الثآليل التناسلية على تفضيلات المريض، والموارد المتاحة، وخبرة مقدم الرعاية الصحية. لا يوجد دواء واحد متوفر حاليًا أكثر فعالية من غيره، أو هو الدواء الأمثل لجميع المرضى.
تشمل خيارات العلاج المتاحة حاليًا للثآليل التناسلية المرئية العلاجات الموضعية التي يطبقها المريض (بودوفيلوكس وإيميكوامود) والعلاجات التي يقدمها مقدم الرعاية الصحية (العلاج بالتبريد، وراتنج بودوفيلين، وحمض ثلاثي كلورو أسيتيك، وحمض ثنائي كلورو أسيتيك، والإنترفيرون) والجراحة. يعاني معظم المرضى من ثآليل تناسلية تتراوح مساحتها بين 0.5 و1.0 سم مربع، وتستجيب لمعظم خيارات العلاج. تشمل العوامل التي قد تؤثر على اختيار العلاج حجم الثآليل وعددها وموقعها وشكلها وتفضيل المريض وتكلفتها وسهولة إعطائها والآثار الجانبية وخبرة مقدم الرعاية الصحية. تُعد خطة أو بروتوكول العلاج أمرًا بالغ الأهمية لأن العديد من المرضى يحتاجون إلى دورة علاجية كاملة بدلاً من جلسة علاجية واحدة. بشكل عام، تستجيب الثآليل الموجودة على الأسطح الرطبة و/أو في طيات الجلد بشكل أفضل للعلاج الموضعي بأدوية مثل حمض ثلاثي كلورو أسيتو أسيتيك (TCA)، وبودوفيلين، وبودوفيلوكس، وإيميكوامود مقارنةً بالثآليل الموجودة على أسطح الجلد الجافة.
إذا لم تُسفر طرق العلاج التي اتبعها الطبيب عن تحسن ملحوظ بعد ثلاث دورات علاجية، أو شفاء تام للثآليل بعد ست دورات علاجية، فيجب تغيير طريقة العلاج. يجب تقييم نسبة المخاطر والفوائد لدورة العلاج بشكل كامل لتجنب الإفراط في شفاء المريض. يجب على الطبيب دائمًا تقييم طرق العلاج الموضعية التي يتبعها المريض، وتعديلها عند الضرورة.
المضاعفات نادرة عند إجراء العلاج بشكل صحيح. يجب تنبيه المرضى إلى شيوع ظهور ندوب قليلة أو مفرطة التصبغ بعد إزالة الثآليل الاستئصالية. أما الندوب الغائرة أو المتضخمة، فهي نادرة، ولكنها قد تحدث إذا لم يكن لدى المريض وقت كافٍ بين الجلسات. نادرًا ما يؤدي العلاج إلى متلازمات ألم مزمنة مُعيقة، مثل ألم الفرج أو فرط الإحساس في موضع العلاج.
الثآليل التناسلية الخارجية، العلاج الموصى به
العلاج الذاتي
بودوفيلوكس، محلول أو جل ٠.٥٪. يمكن للمرضى وضع محلول بودوفيلوكس باستخدام قطعة قطن، أو جل بودوفيلوكس باستخدام إصبع، مرتين يوميًا لمدة ٣ أيام، تليها فترة راحة لمدة ٤ أيام. يمكن تكرار هذه الدورة عند الحاجة، لأربع دورات. يجب ألا تتجاوز المساحة الإجمالية للثآليل المعالجة ١٠ سم٢ ، ويجب ألا يتجاوز إجمالي حجم بودوفيلوكس ٠.٥ مل يوميًا. إذا أمكن، ينبغي على أخصائي رعاية صحية إجراء أول جلسة علاجية لتوضيح كيفية وضع المنتج بشكل صحيح وأي الثآليل يجب علاجها. لم تُثبت سلامة بودوفيلوكس أثناء الحمل.
أو كريم إيميكوامود ٥٪. يُنصح بوضع كريم إيميكوامود بإصبع المريض ليلاً، ثلاث مرات أسبوعيًا، لمدة تصل إلى ١٦ أسبوعًا. يُنصح بغسل المنطقة المصابة بالماء والصابون المعتدل بعد ٦-١٠ ساعات من الاستخدام. يُلاحظ العديد من المرضى اختفاء الثآليل خلال ٨-١٠ أسابيع أو أقل مع هذا العلاج. لم تُثبت سلامة استخدام بودوفيلوكس أثناء الحمل.
العلاج الذي يقوم به الطبيب
العلاج بالتبريد باستخدام النيتروجين السائل أو مسبار التبريد. يُكرر كل أسبوع إلى أسبوعين.
راتنج بودوفيلين، بتركيز 10-25% في صبغة البنزوين. تُوضع كمية صغيرة على كل ثؤلول وتُترك لتجف في الهواء. لتجنب مشاكل الامتصاص الجهازي والسمية، يُوصي بعض الخبراء بالحد من كمية المستحضر (أقل من 0.5 مل بودوفيلين) أو مساحة الثؤلول (10 سم² ) لكل استخدام. ويقترح بعض الخبراء غسل المستحضر بعد 1-4 ساعات من الاستخدام لتجنب تهيج الأنسجة. يُكرر الاستخدام أسبوعيًا عند الحاجة. لم تُثبت سلامة بودوفيلوكس أثناء الحمل.
أو حمض ثلاثي كلورو الأسيتيك (TCA) أو حمض ثنائي كلورو الأسيتيك (DCA) بتركيز 80-90%. ضع كمية قليلة فقط على الثآليل واتركها حتى تجف، حتى يظهر "جليد" أبيض. لإزالة الحمض غير المتفاعل، استخدم مسحوقًا مع بودرة التلك أو بيكربونات الصوديوم (صودا الخبز). كرر الإجراء أسبوعيًا عند الحاجة.
أو الاستئصال الجراحي - الاستئصال الظاهري بالمقص، أو الاستئصال الظاهري بشفرة الحلاقة، أو الكحت، أو الجراحة الكهربائية.
الثآليل التناسلية الخارجية، العلاجات البديلة
إعطاء الإنترفيرون داخل الآفة
أو جراحة الليزر
يمكن للمريض إجراء العلاج بمفرده إذا كان موقع الثآليل يسمح بذلك. يُعد بودوفيلوكس، على شكل محلول أو جل بتركيز 0.5%، غير مكلف نسبيًا وسهل الاستخدام وآمن، ويمكن للمرضى استخدامه في المنزل. بودوفيلوكس دواء مضاد للانقسام يُسبب تدمير الثآليل. لاحظ معظم المرضى ألمًا خفيفًا إلى متوسطًا أو تهيجًا موضعيًا بعد العلاج. أما إيميكويمود فهو مُحفز مناعي موضعي يُعزز إنتاج الإنترفيرون والسيتوكينات الأخرى. قبل اختفاء الثآليل، عادةً ما تحدث تفاعلات التهابية موضعية، غالبًا ما تكون خفيفة أو متوسطة.
يقضي العلاج بالتبريد على الثآليل عن طريق التحلل الخلوي الناتج عن الحرارة، ويتطلب معدات خاصة. عيبه الرئيسي هو أن استخدامه الصحيح يتطلب تحضيرًا جيدًا، والذي غالبًا ما لا يمكن شفاء الثآليل تمامًا بدونه، مما قد يقلل من فعالية الطريقة أو يزيد من خطر حدوث مضاعفات. يحدث الألم أثناء استخدام النيتروجين السائل بسبب النخر، وغالبًا ما تتكون بثور في موقع الاستخدام. على الرغم من أن التخدير الموضعي (سواءً كان موضعيًا أو بالحقن) لا يُستخدم بشكل روتيني، إلا أن استخدامه يُسهّل العلاج عند وجود عدد كبير من الثآليل أو عندما تكون المنطقة المراد تجميدها كبيرة.
يحتوي راتنج بودوفيلين على العديد من المكونات، بما في ذلك ليجنان بودوفيلين، وهو عامل مضاد للانقسام. يُحضّر الراتنج عادةً في صبغة البنزوين بتركيز 10-25%. مع ذلك، يختلف هذا المستحضر اختلافًا كبيرًا في تركيزه ومحتوى مكوناته النشطة وغير النشطة. مدة بقاء مستحضرات بودوفيلين نشطة غير معروفة. من المهم وضع راتنج بودوفيلين بطبقة رقيقة على الثؤلول وتركه يجف في الهواء قبل لمس المنطقة بالملابس. قد يؤدي الاستخدام الكثيف أو عدم تجفيفه بالهواء بشكل كافٍ إلى تهيج موضعي بسبب انتشار الدواء إلى الجلد السليم.
TCCA وBCA مواد كاوية تُدمر الثآليل عن طريق تخثر البروتينات كيميائيًا. تُستخدم هذه المواد على نطاق واسع، ولكن لم تُدرس بشكل كافٍ. تتميز محاليل TCCA بلزوجة منخفضة جدًا (مقارنةً بالماء)، وإذا استُخدمت بكثرة، فقد تنتشر بسرعة، مُلحقةً ضررًا كبيرًا بالأنسجة السليمة المجاورة. يجب وضع مستحضرات TCCA وBCA بحرص شديد وتركها تجف قبل أن يجلس المريض أو يقف. في حال حدوث ألم شديد، يُمكن معادلة الحمض بالصابون أو الصودا.
تتميز إزالة الثآليل جراحيًا بمزايا تُقارن بالطرق الأخرى، إذ يُمكن إزالتها بسرعة، عادةً في زيارة واحدة. ومع ذلك، فهي تتطلب خبرة سريرية واسعة، وبعض المعدات، وفترات علاج أطول. بمجرد استخدام التخدير الموضعي، يُمكن القضاء على الثآليل التناسلية المرئية فعليًا بالجراحة الكهربائية، وفي هذه الحالة لا يتطلب الأمر عادةً أي توقف إضافي للنزيف. كبديل، يُمكن إزالة الثآليل بالاستئصال الظاهري بمقص حاد أو مشرط، أو بالكشط. ولأن معظم الثآليل خارجية، فقد تُعقّد هذه الطريقة بتكوين جرح داخل البشرة. يُمكن تحقيق التوقف عن النزيف بالكي الكهربائي أو باستخدام عوامل إيقاف النزيف الكيميائية مثل محلول كلوريد الألومنيوم. لا تُستطب الغرز في معظم الحالات إذا أُجريت الإزالة الجراحية بشكل صحيح. يُعد العلاج الجراحي الأنسب للمرضى الذين يعانون من عدد كبير أو مساحة واسعة من الثآليل التناسلية. يُمكن استخدام ليزر ثاني أكسيد الكربون والعلاج الجراحي للمرضى الذين يعانون من ثآليل متعددة أو ثآليل داخل الإحليل، خاصةً إذا فشلت العلاجات الأخرى.
استُخدم الإنترفيرون، سواءً كان طبيعيًا أو مُعاد التركيب، لعلاج الثآليل التناسلية جهازيًا (تحت الجلد، أو في موضع بعيد، أو عضليًا) أو داخل الآفة (حقن داخل الآفة). لم يُثبت الاستخدام الجهازي للإنترفيرون فعاليته. أظهر الإنترفيرون المُعطى داخل الآفة فعاليةً ومعدلات عودة مماثلة للطرق الأخرى. يُعتقد أن الإنترفيرون فعالٌ لتأثيراته المضادة للفيروسات و/أو المُحفزة للمناعة. مع ذلك، لا يُنصح باستخدام الإنترفيرون بشكل روتيني نظرًا لعدم ملاءمته، والحاجة إلى زيارات متكررة، وآثاره الجانبية الجهازية المتكررة، على الرغم من فعاليته المماثلة للطرق الأخرى.
نظراً لقلة العلاجات الفعّالة المتاحة، تلجأ بعض العيادات إلى العلاجات المركبة (علاجان أو أكثر في آنٍ واحد لنفس الثؤلول). يعتقد معظم الخبراء أن العلاجات المركبة لا تزيد من فعاليتها، بل قد تزيد من المضاعفات.
ثآليل عنق الرحم
بالنسبة للنساء المصابات بثآليل عنق الرحم الخارجية، يجب استبعاد وجود آفة حرشفية داخل الظهارة (SIL) عالية الدرجة قبل العلاج. يجب أن يُجرى العلاج تحت إشراف أخصائي.
الثآليل المهبلية
العلاج بالتبريد باستخدام النيتروجين السائل. نظرًا لخطر حدوث ثقب وتكوين ناسور، لا يُنصح باستخدام مسبار التبريد في المهبل.
يُوضع ٨٠-٩٠٪ من المستحضر على الثآليل فقط، سواءً كان THUK أو BHUK. يجب وضع المستحضر بكميات صغيرة على الثآليل فقط، مع الاحتفاظ به حتى يجف تمامًا، حتى تظهر طبقة بيضاء. لإزالة الحمض غير المتفاعل، استخدم مسحوقًا مع بودرة التلك أو بيكربونات الصوديوم (صودا الخبز). كرر الإجراء أسبوعيًا عند الحاجة.
أو يُوضع بودوفيلين، بتركيز ١٠-٢٥٪ في صبغة البنزوين، على المنطقة المصابة، ويجب أن تكون جافة قبل إزالة المنظار. خلال جلسة واحدة، يجب معالجة مساحة أقل من ٢ سم مربع. عند الضرورة، يُكرر الإجراء كل أسبوع. نظرًا لاحتمالية الامتصاص الجهازي، يُحذر بعض الخبراء من استخدام بودوفيلين في المهبل. لم تُثبت سلامة استخدام بودوفيلين أثناء الحمل.
الثآليل في فتحة مجرى البول
العلاج بالتبريد باستخدام النيتروجين السائل.
أو
بودوفيلين، ١٠-٢٥٪ في صبغة البنزوين. يجب تجفيف منطقة التطبيق قبل ملامسة الغشاء المخاطي الطبيعي. يُستعمل أسبوعيًا عند الحاجة. لم تُثبت سلامة استخدام بودوفيلين أثناء الحمل.
الثآليل الشرجية
العلاج بالتبريد باستخدام النيتروجين السائل.
يُوضع ٨٠-٩٠٪ من المستحضر على الثآليل، سواءً كان ثوك أو بهوك. يُوضع المستحضر بكميات صغيرة على الثآليل فقط، ويُحفظ حتى يجف، حتى تظهر طبقة بيضاء. لإزالة الحمض غير المتفاعل، يُستخدم مسحوق التلك أو بيكربونات الصوديوم (صودا الخبز). يُكرر الإجراء أسبوعيًا عند الحاجة.
أو الإزالة الجراحية.
ملحوظة: يجب أن يتم علاج الثآليل الموجودة على الغشاء المخاطي للمستقيم تحت إشراف طبيب مختص.
الثآليل الفموية
العلاج بالتبريد باستخدام النيتروجين السائل
أو الإزالة الجراحية.
مراقبة المتابعة
إذا استجابت الثآليل الظاهرة للعلاج بشكل جيد، فلا داعي للمتابعة. يُنصح المرضى بمراقبة تكرار ظهورها، وهو أكثر شيوعًا خلال الأشهر الثلاثة الأولى. ولأن حساسية وخصوصية التشخيص الذاتي للثآليل التناسلية غير معروفة، يُنصح المرضى بالعودة للمتابعة بعد ثلاثة أشهر من العلاج لمراقبة تكرار ظهورها. تُتيح زيارة المتابعة المبكرة متابعة شفاء الثآليل والمضاعفات المحتملة للعلاج، كما تُتيح فرصةً لتثقيف المريضة وتقديم المشورة لها. يُنصح النساء بالخضوع لفحص خلوي دوري. لا يُعد وجود الثآليل التناسلية مؤشرًا على إجراء تنظير المهبل.
إدارة الشركاء الجنسيين
في إدارة المرضى المصابين بالثآليل التناسلية، لا يُعد فحص الشركاء الجنسيين ضروريًا لأن دور إعادة العدوى يبدو ضئيلًا، وفي غياب العلاجات الشافية، فإن العلاجات التي تهدف إلى تقليل خطر انتقال العدوى لا قيمة لها. ومع ذلك، نظرًا لعدم التأكد من القيمة التشخيصية للفحص الذاتي والفحص المتبادل بين الشركاء، يمكن فحص شركاء المرضى المصابين بالثآليل التناسلية لتقييم الثآليل التناسلية وغيرها من الأمراض المنقولة جنسيًا. نظرًا لأن علاج الثآليل التناسلية على الأرجح لا يقضي على فيروس الورم الحليمي البشري، فيجب إخطار المرضى وشركائهم بأنهم قد ينقلون العدوى إلى شركاء جنسيين غير مصابين. قد يقلل استخدام الواقي الذكري من خطر انتقال فيروس الورم الحليمي البشري إلى شريك غير مصاب، ولكنه لا يقضي عليه. يجب تذكير شريكات المرضى المصابين بالثآليل التناسلية بأنه يوصى بإجراء فحص خلوي لسرطان عنق الرحم لجميع النساء النشطات جنسيًا.
ملاحظات خاصة
الحمل
لا ينبغي استخدام إيميكيمود، وبودوفيلين، وبودوفيلوكس أثناء الحمل. ولأن الثآليل التناسلية تميل إلى التكاثر وتصبح هشة أثناء الحمل، يوصي العديد من الخبراء بإزالتها أثناء الحمل. يمكن أن يسبب النوعان 6 و11 من فيروس الورم الحليمي البشري (HPV) داء الورم الحليمي الحنجري لدى حديثي الولادة والأطفال. لا يزال مسار انتقال العدوى (عبر المشيمة، أو أثناء الولادة، أو بعد الولادة) غير واضح. كما أن القيمة الوقائية للولادة القيصرية غير معروفة؛ لذا، لا ينبغي إجراء الولادة القيصرية فقط لغرض منع انتقال عدوى فيروس الورم الحليمي البشري إلى حديثي الولادة. نادرًا ما يُنصح بإجراء الولادة القيصرية لدى النساء المصابات بثآليل تناسلية تعيق مرور الجنين عبر قناة الولادة، أو التي قد تسبب نزيفًا غزيرًا أثناء الولادة المهبلية إذا ما تمركزت في المهبل.
المرضى الذين يعانون من انخفاض المناعة
قد يكون علاج الثآليل التناسلية لدى الأفراد الذين يعانون من ضعف المناعة بسبب عدوى فيروس نقص المناعة البشرية أو لأسباب أخرى أقل فعالية منه لدى ذوي الاستجابات المناعية الطبيعية. وقد يكون تكرار المرض بعد العلاج أكثر شيوعًا. وقد يكون معدل الإصابة بسرطان الخلايا الحرشفية أو ما شابهه من الثآليل التناسلية أعلى في هذه الفئة، ومن المرجح أن يحتاج هؤلاء المرضى إلى خزعة لتأكيد التشخيص.
سرطان الخلايا الحرشفية الموضعي
في حال تشخيص الإصابة بسرطان الخلايا الحرشفية الموضعي، يجب إحالة المريضة إلى أخصائي في هذا المجال. عادةً ما تكون العلاجات الاستئصالية فعالة، ولكن المتابعة الدقيقة ضرورية بعد استخدامها. يوجد خطر تطور هذه الآفات إلى سرطان الخلايا الحرشفية الموضعي، ولكنه على الأرجح منخفض. تتعرض شريكات هؤلاء المرضى لخطر كبير للإصابة بأمراض عنق الرحم.
عدوى فيروس الورم الحليمي البشري التناسلية دون السريرية (بدون الثآليل الخارجية)
تُعدّ عدوى فيروس الورم الحليمي البشري دون السريرية أكثر شيوعًا من الثآليل الخارجية لدى كل من الرجال والنساء. غالبًا ما تُكتشف العدوى في عنق الرحم عن طريق مسحة عنق الرحم، أو تنظير المهبل، أو الخزعة، وفي القضيب، والفرج، ومناطق الأعضاء التناسلية الأخرى عن طريق ظهور بقع بيضاء بعد استخدام حمض الأسيتيك. ومع ذلك، لم يعد يُنصح بالاستخدام الروتيني لحمض الأسيتيك والفحص باستخدام عدسة مكبرة وضوء كاختبارات فحص للثآليل التناسلية "دون السريرية" أو "البيضاء الأسيتيكية". لا يُعدّ ظهور البقع البيضاء بعد استخدام حمض الأسيتيك اختبارًا محددًا لعدوى فيروس الورم الحليمي البشري. وبالتالي، قد تُكتشف العديد من النتائج الإيجابية الكاذبة في الفئات السكانية منخفضة الخطورة عند استخدامه كاختبار فحص. لا تزال خصوصية وحساسية هذا الإجراء قيد التحديد. في حالات خاصة، يجد الأطباء ذوو الخبرة هذا الاختبار مفيدًا في تحديد الثآليل التناسلية المسطحة.
يعتمد التشخيص النهائي لعدوى فيروس الورم الحليمي البشري على الكشف عن الحمض النووي الفيروسي (DNA) أو بروتينات القفيصة. لا يرتبط تشخيص عدوى فيروس الورم الحليمي البشري عن طريق مسحات عنق الرحم عادةً بكشف الحمض النووي لفيروس الورم الحليمي البشري في خلايا عنق الرحم. تُشبه التغيرات الخلوية في عنق الرحم المرتبطة بعدوى فيروس الورم الحليمي البشري تلك التي تُلاحظ في خلل التنسج منخفض الدرجة، وغالبًا ما تتراجع تلقائيًا. تتوفر اختبارات للكشف عن الحمض النووي لبعض أنواع فيروس الورم الحليمي البشري في خلايا عنق الرحم المأخوذة بالكشط، ولكن قيمتها السريرية لإدارة المريضة غير معروفة. لا ينبغي اتخاذ قرارات العلاج بناءً على اختبار الحمض النووي لفيروس الورم الحليمي البشري. لا يُنصح بفحص عدوى فيروس الورم الحليمي البشري التناسلية دون السريرية باستخدام اختبارات الحمض النووي أو الحمض النووي الريبي (RNA) أو حمض الأسيتيك.
علاج
في حال عدم وجود خلل تنسج مصاحب، لا يُنصح بعلاج عدوى فيروس الورم الحليمي البشري دون السريرية المُشخصة بمسحة عنق الرحم، أو تنظير المهبل، أو الخزعة، أو تحضير الجلد أو الغشاء المخاطي بحمض الأسيتيك، أو الكشف عن فيروس الورم الحليمي البشري (الحمض النووي أو الحمض النووي الريبوزي)، لأن التشخيص غالبًا ما يكون غير مؤكد، والعلاج لا يقضي على العدوى. وقد اكتُشف فيروس الورم الحليمي البشري لدى الرجال والنساء في الأنسجة المجاورة بعد العلاج بالليزر لخلل التنسج المرتبط بفيروس الورم الحليمي البشري، وبعد محاولات القضاء على عدوى فيروس الورم الحليمي البشري دون السريرية عن طريق التبخير بالليزر المكثف لمنطقة الشرج والتناسل. في حال وجود خلل تنسج مصاحب، ينبغي أن يعتمد نهج العلاج على درجة خلل التنسج.
إدارة الشركاء الجنسيين
فحص الشركاء الجنسيين ليس ضروريًا. من المرجح أن يكون معظم الشركاء مصابين بعدوى فيروس الورم الحليمي البشري دون السريرية. لا توجد اختبارات فحص عملية لعدوى فيروس الورم الحليمي البشري دون السريرية. قد يقلل استخدام الواقي الذكري من احتمالية نقل العدوى إلى شريك غير مصاب أو شريك جديد؛ ومع ذلك، فإن فترة العدوى غير معروفة. من غير المعروف ما إذا كان المرضى المصابون بعدوى فيروس الورم الحليمي البشري دون السريرية معديين بنفس درجة عدوى المرضى المصابين بالثآليل الخارجية.
 [ 1 ]
[ 1 ]
ما هي الاختبارات المطلوبة؟

