خبير طبي في المقال
منشورات جديدة
الداء النشواني الكبدي
آخر مراجعة: 29.06.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
داء النشواني هو عادةً مرضٌ جهازيٌّ عامٌّ يتميز بتراكم الأميلويد (جليكوبروتين مُحدد) في الأنسجة، وما يتبع ذلك من خللٍ في وظائف الأعضاء الطبيعية. يُعدّ داء النشواني الكبدي أقل شيوعًا بكثير من الكلى والطحال [ 1 ]، ولكنه يُصاحب في أغلب الأحيان تلفًا جهازيًا في الجسم. لا يُمكن لأيٍّ من تقنيات التصوير المُتاحة إثبات وجود الأميلويد بشكلٍ مُحدد. حتى عند الاشتباه سريريًا وإشعاعيًا، يعتمد تشخيص داء النشواني على خزعة الأنسجة لتأكيد وجود رواسب الأميلويد. [ 3 ] العلاج مُعقدٌ وشامل، ويشمل تدابير مثبطة للمناعة وأخرى مُعالجة للأعراض. في الحالات الشديدة، قد يلزم إجراء عملية زرع كبد.
علم الأوبئة
يعتمد نجاح العلاج بشكل مباشر على التشخيص المبكر للمرض، الذي يُسبب تكوّن مُركّب بروتيني-سكري (أميلويد) في مختلف الأعضاء والكبد. وكما تُظهر الممارسة، يصعب الافتراض أو الاشتباه في الإصابة بالداء النشواني، على الرغم من إمكانية تشخيصه وتأكيده. والحقيقة هي أنه في أكثر من 80% من الحالات غير المُشخّصة، يكون المرض مُخفيًا سريريًا بأعراض أمراض الكبد. وتُعدّ الخزعة أكثر طرق التشخيص فعالية.
يُعد داء النشواني الكبدي مشكلة نادرة مقارنةً بداء النشواني الكلوي. في الوقت نفسه، تصاحب جميع حالات آفات الكبد آفات في أعضاء أخرى. غالبًا ما يؤثر المرض بشكل رئيسي على الأجزاء الهيكلية للثالوث الكبدي، مما يُحدد الحد الأدنى من الأعراض وعدم تحديدها. تتجلى الصورة السريرية والمورفولوجية لقصور الخلايا الكبدية وارتفاع ضغط الدم البابي في نوعين من الأمراض المنتشرة وداخل الفصيصات.
يتم تبرير خزعة الكبد عندما يكون تضخم الكبد موجودًا دون أعراض كبدية سابقة وفي غياب متلازمة الكلى.
يُرى تورط الكبد المنتشر في حوالي 25% من الحالات، وفي 75% من المرضى تتأثر المسالك البوابية فقط.
يؤثر داء النشواني الأولي على الكبد في 90% من الحالات، بينما يؤثر داء النشواني الثانوي على الكبد في 47% فقط من الحالات.
يُعدّ تأثر الكبد المنعزل نادرًا للغاية. عادةً ما تُصاب الكلى (حوالي 93% من الحالات)، والطحال (72%)، والقلب (57%)، والبنكرياس (36%)، والغدد الكظرية (29%)، والأمعاء والرئتان (21% لكل منهما) بشكل متزامن.
تُصاب النساء بهذا المرض بمعدل ضعف معدل إصابة الرجال تقريبًا. ويتراوح متوسط العمر المتوقع لمرضى داء النشواني بين 52 و64 عامًا.
الأسباب الداء النشواني الكبدي
يتطور داء النشواني بتكوين وتراكم مركب بروتيني متعدد السكريات - الأميلويد - في أنسجة الكبد. لم تُدرس مشكلة ظهور الآفة الأولية بشكل كافٍ حتى الآن. أما بالنسبة للأمراض الثانوية، فعادةً ما يرتبط ظهورها بالأمراض التالية:
- العمليات المعدية المزمنة (السل، الزهري، داء الشعيات)؛
- العمليات الالتهابية القيحية (التهاب الشغاف الميكروبي، التهاب العظم والنقي، مرض توسع القصبات الهوائية، وما إلى ذلك)؛
- الأمراض الخبيثة (سرطان الدم، سرطان الحشوي، الأورام اللمفاوية الحبيبية).
يُلاحظ الشكل التفاعلي من داء النشواني لدى المرضى المصابين بتصلب الشرايين المصاحب، وأمراض الروماتيزم (داء بيتشيرف، التهاب المفاصل الروماتويدي)، والصدفية، والالتهابات المزمنة، وأمراض الجهاز المناعي المتعددة (بما في ذلك الساركويد). عوامل الخطر الرئيسية: الاستعداد الوراثي، واضطرابات المناعة الخلوية، وفرط غلوبولين الدم.
طريقة تطور المرض
هناك عدد من الافتراضات حول أصل داء النشواني الكبدي. يلتزم معظم المتخصصين بنظرية خلل البروتين، والطبيعة المناعية والطفرية للمرض، بالإضافة إلى التكوين الخلوي المحلي. تتضمن نظرية التكوين الخلوي تغيرات في التفاعلات التي تعمل على المستوى الخلوي (تكوين السلائف الليفية للأميلويد بواسطة مجموعة من الخلايا البلعمية)، على الرغم من أن الأميلويد يتشكل ويتراكم خارج البنى الخلوية.
يعتمد مفهوم خلل البروتين على أن الأميلويد ناتج عن خلل في أيض البروتين. يكمن السبب الرئيسي للمشكلة في خلل بروتين الدم وفرط فيبرينوجين الدم، مما يؤدي إلى تراكم أجزاء البروتين والبارابروتين المشتتة بشكل خشن في البلازما.
وفقًا للتفسير المناعي، يحدث تكوّن الأميلويد نتيجة تفاعل المستضد مع الجسم المضاد، حيث تعمل نواتج تحلل الأنسجة أو البروتينات الغريبة كمستضدات. ويحدث تراكم الأميلويد بشكل رئيسي في منطقة تكوّن الأجسام المضادة والتواجد المفرط للمستضدات.
النسخة الأكثر ترجيحا التي يفكر فيها العلماء هي نظرية الطفرة، والتي تأخذ في الاعتبار مجموعة متنوعة من العوامل المسببة للطفرات والتي يمكن أن تؤدي إلى خلل في تخليق البروتين.
الأميلويد هو بروتين هيبوبروتيني معقد يتكون من بروتينات كروية ولييفية ممزوجة مع عديدات السكاريد. تؤثر تراكمات الأميلويد على الطبقة الداخلية والغلاف الخارجي للشبكة الوعائية، ونسيج الأعضاء المتنيّة، وبنية الغدد، وغيرها. لا تسبب تراكمات الأميلويد أي ضرر وظيفي. أما التراكمات الصغيرة فلا تسبب اضطرابات وظيفية، ولكن مع وجود الأميلويد بكثافة في الكبد، يزداد حجمه، ويغير مظهره، ويؤدي إلى قصور في وظائفه.
يتميز داء النشواني الكبدي بترسب ألياف النشواني في فراغ ديس، والذي يبدأ عادة في المنطقة المحيطة بالبوابة، على الرغم من أنه يكون أحيانًا مركزيًا وقد يترسب أيضًا في الأوعية الدموية الكبدية. [ 4 ]، [ 5 ] في الحالات الشديدة، يؤدي ترسب النشواني إلى ضمور ضغط الخلايا الكبدية، مما يمنع مرور الصفراء، مما يؤدي إلى ركود صفراوي، أو قد يسد الجيوب الأنفية، مما يؤدي إلى ارتفاع ضغط الدم البابي. [ 6 ]، [ 7 ]، [ 8 ]
الأعراض الداء النشواني الكبدي
الصورة السريرية في داء النشواني في الكبد متنوعة، وتعتمد على شدة تراكم الأميلويد، وعلى سماته الكيميائية الحيوية، ومدة العملية المرضية، ودرجة تلف الأعضاء وانتهاك حالتها الوظيفية.
في المرحلة الكامنة من داء النشواني، حيث لا يمكن اكتشاف تراكمات الأميلويد في الكبد إلا بالفحص المجهري، لا تظهر العلامات الأولى للمرض. ومع تفاقم المرض وازدياد العجز الوظيفي فيه، تتفاقم الأعراض.
يزداد سمك الكبد تدريجيًا ويتضخم. قد تختلف طريقة جس الكبد، لكن حوافه تكون ناعمة وغير مؤلمة. نادرًا ما يصاحب المرض ألم في منطقة تحت الضلع الأيمن، وعسر هضم، وتضخم الطحال، واصفرار الجلد والأغشية المخاطية والصلبة، ومتلازمة النزف.
الأعراض الأكثر تميزًا في داء النشواني الكبدي: [ 9 ]، [ 10 ]
- يؤدي تراكم الأميلويد في الكبد إلى تضخم الكبد في 33-92% من المرضى؛
- اليرقان الخفيف
- ارتفاع ضغط الدم البابي؛
- ركود صفراوي متوسط إلى شديد.
نظرًا لأن داء النشواني نادرًا ما يؤثر على عضو واحد فقط، فعادةً ما تكون هناك أعراض إضافية:
- عندما يتطور تلف الكلى إلى متلازمة الكلى وارتفاع ضغط الدم الشرياني مع مزيد من الفشل الكلوي، والوذمة، وأحيانا تجلط الوريد الكلوي، وبيلة الكريات البيضاء، والبيلة الدموية، ونقص بروتين الدم، والآزوتيمية وما إلى ذلك؛
- عندما يتأثر القلب، تتطور حالة مشابهة لاعتلال عضلة القلب التقييدي (اضطرابات النظم، تضخم القلب، زيادة العجز القلبي، الضعف وضيق التنفس، الوذمة، وفي حالات أقل شيوعًا - تراكم السوائل في التجويف البطني والجنبي، التهاب التامور)؛
- في حالة تأثر الجهاز الهضمي، قد يحدث تضخم اللسان، وضعف وحركة المريء، والغثيان وحرقة المعدة، والإمساك أو الإسهال، وما إلى ذلك.
- عندما يتأثر البنكرياس، تظهر أعراض التهاب البنكرياس المزمن؛
- إذا تأثرت الآلية العضلية الهيكلية، تتطور التهاب المفاصل المتماثل، ومتلازمة النفق الرسغي، والاعتلالات العضلية، وإذا تأثر الجهاز العصبي، يتم العثور على اعتلالات الأعصاب، والشلل، وانخفاض ضغط الدم الانتصابي، وزيادة التعرق، والخرف.
إذا انتشر رد الفعل المرضي إلى الجلد، تظهر لويحات شمعية عديدة على الوجه والرقبة وطيات الجلد. من الممكن ظهور أعراض التهاب الجلد العصبي، أو حمى الحرشفية الحمراء، أو تصلب الجلد.
إن الجمع بين الآفات النشوانية المتعددة وتنوع الأعراض يجعل التعرف على داء النشواني الكبدي أكثر صعوبة ويتطلب تشخيصًا شاملاً وكاملاً.
إستمارات
وفقًا لتصنيف منظمة الصحة العالمية، يتم التمييز بين خمسة أنواع من داء النشواني:
- AL (أساسي)؛
- AA (ثانوي)؛
- ATTR (الوراثية والشيخوخة الجهازية)؛
- Aβ2M (في المرضى الذين يخضعون لغسيل الكلى)؛
- AIAPP (في المرضى الذين يعانون من مرض السكري المستقل عن الأنسولين)؛
- AB (لمرض الزهايمر)؛
- AANF (داء النشواني الأذيني الشيخوخي).
هناك داء نشواني موضعي في الكبد، ولكن في أغلب الأحيان يكون عبارة عن آفة جهازية، حيث تشمل العملية المرضية أيضًا الكلى والقلب والطحال والجهاز العصبي، بالإضافة إلى الأعضاء والأنسجة الأخرى.
المضاعفات والنتائج
يؤدي داء النشواني الجهازي تدريجيًا إلى تطور عمليات مرضية حادة قد تؤدي بدورها إلى الوفاة. من بين المضاعفات الأكثر شيوعًا والتي تُهدد الحياة ما يلي:
- الأمراض المعدية المتكررة (البكتيرية والفيروسية)، بما في ذلك الالتهاب الرئوي، والتهاب الحويضة والكلية، والتهاب كبيبات الكلى؛
- الفشل الكبدي والكلوي المزمن؛
- قصور القلب المزمن (قد يسبق احتشاء عضلة القلب)؛
- السكتات الدماغية النزفية.
يحدث تجلط الدم الوريدي نتيجة تراكم البروتينات وترسبها على جدران الأوردة. يضيق تجويف الأوعية المصابة، ويتطور فشل الأعضاء. مع مرور الوقت، وفي ظل فرط بروتين الدم طويل الأمد، قد ينغلق الوعاء الدموي تمامًا. أي من هذه المضاعفات قد يؤدي إلى الوفاة.
التشخيص الداء النشواني الكبدي
في حال الاشتباه بداء النشواني الكبدي، تُجرى الإجراءات التشخيصية بعد استشارات إلزامية من أطباء الجهاز الهضمي والمعالجين، وأطباء الروماتيزم، وأطباء القلب، وأطباء الجلد، وأطباء الأعصاب، وأطباء المسالك البولية. من المهم إجراء تقييم شامل لبيانات التاريخ المرضي والأعراض السريرية، وإجراء تشخيصات مخبرية وتشخيصية شاملة.
تشمل الفحوصات بالضرورة فحص البول والدم. في داء النشواني الكبدي، غالبًا ما يُلاحظ مزيج من كثرة الكريات البيضاء مع بروتينية وبيلة أسطوانية، ونقص بروتين الدم - مع فرط شحميات الدم، وفقر الدم، ونقص صوديوم الدم، ونقص كالسيوم الدم، وانخفاض عدد الصفائح الدموية. تُكتشف البارابروتينات في البول والرحلان الكهربائي في المصل.
تشمل التشخيصات الآلية ما يلي:
- تخطيط كهربية القلب، صدى القلب؛
- الموجات فوق الصوتية على البطن؛
- الأشعة السينية للمعدة والمريء؛
- التصوير بالري، الأشعة السينية بالباريوم؛
- التنظير الداخلي.
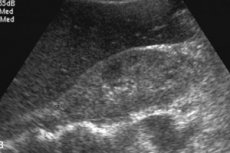
تشمل النتائج الشعاعية لداء النشواني الكبدي تضخم الكبد غير النوعي، وزيادة الصدى على الموجات فوق الصوتية أو الكثافة على التصوير المقطعي المحوسب (CT)، وزيادة شدة إشارة T1 على التصوير بالرنين المغناطيسي (MRI). [ 12 ] يُظهر التصوير الومضاني باستخدام مؤشرات مرتبطة بـ Tc-99m امتصاصًا غير متجانس، ولكنه غير نوعي. [ 13 ]، [ 14 ] وقد ثبت أن GC يزيد من تصلب الكبد المقاس بواسطة التصوير المرن ؛ [ 15 ]، [ 16 ]، [ 17 ] ولكن هناك عدد قليل من التقارير عن الحالات. يُعد التصوير المرن بالرنين المغناطيسي (MRE) حاليًا الطريقة غير الجراحية الأكثر دقة للكشف عن تليف الكبد وتحديد مرحلته، [ 18 ]، [ 19 ] يُعد التصوير المرن بالرنين المغناطيسي مفيدًا في الكشف عن التقدم والاستجابة للعلاج والتنبؤ بتعويض الكبد لدى مرضى تليف الكبد. [ 20 ]
يصعب تشخيص داء النشواني الكبدي بالموجات فوق الصوتية: يُحدد وجود تضخم في الكبد، مع وجود تضخم كبدي أكثر تحديدًا يتجاوز 15 سم. تُجرى خزعة، تحت إشراف الموجات فوق الصوتية، وتُعتبر مؤشرًا حاسمًا للتشخيص. باستخدام إبرة خاصة، تُؤخذ عينة صغيرة من أنسجة الكبد، ثم تُصبغ بصبغة خاصة وتُفحص تحت المجهر، مما يسمح برؤية رواسب النشواني مباشرةً.
لا يُجرى التشخيص النهائي إلا بعد اكتشاف لييفات الأميلويد في أنسجة الكبد وأعضاء أخرى. ويُحدَّد النوع الجيني لداء الأميلويد من خلال فحص وراثي طبي دقيق لشجرة النسب.
تشخيص متباين
ينبغي الاشتباه بالداء النشواني لدى جميع المرضى الذين يعانون من بيلة بروتينية كلوية، واعتلال عضلة القلب التقييدي، واعتلال الأعصاب اللاإرادي أو المحيطي، وتضخم الكبد، حتى في غياب البروتين أحادي النسيلة. يُعدّ تحديد نوع الداء النشواني أمرًا بالغ الأهمية، نظرًا لاختلاف علاج الآفات ذات الأسباب المختلفة.
يتضمن التشخيص النسيجي صبغًا بأحمر الكونغو، يليه فحص مجهري في ضوء مستقطب. يُنصح بأخذ خزعة من عدة عينات نسيجية دفعة واحدة. إذا كانت نتيجة الصبغة إيجابية، يُجرى تحليل مناعي كيميائي باستخدام أجسام مضادة وحيدة النسيلة للبروتينات السلفية لتحديد نوع الأميلويد.
يُجرى تحليل الحمض النووي للتمييز بين داء النشواني الأولي ومختلف أشكاله المحددة وراثيًا. يمكن عزل ألياف النشواني من عينات الخزعة وفصلها إلى أحماض أمينية فردية.
دراسات إضافية لتحديد خلل تنسج الخلايا البلازمية:
- التحليل الكهربائي لبروتينات مصل الدم والبول؛
- اختبار مناعي للسلاسل الخفيفة الحرة؛
- التثبيت المناعي (النقل المناعي) لبروتينات المصل؛
- شفط نخاع العظم وخزعة المنظار.
يعد تشخيص داء النشواني الكبدي عملية طويلة وتتطلب جهدًا كبيرًا وتتطلب اهتمامًا متزايدًا من المتخصصين ومعدات عالية الجودة في العيادات والمختبرات.
من الاتصال؟
علاج او معاملة الداء النشواني الكبدي
تهدف تدابير العلاج إلى تقليل تركيز البروتينات النشوية الموجودة مسبقًا في الدم (القضاء على سبب داء النشواني) ودعم وظائف الكبد الكافية.
يتطلب داء النشواني الثانوي تثبيط العملية الالتهابية (في الأمراض المعدية المزمنة وأمراض المناعة الذاتية). في أمراض المناعة الذاتية، يُنصح باستخدام مُثبِّطات الخلايا. للقضاء على العمليات المعدية المزمنة، غالبًا ما تُزال منطقة الالتهاب جراحيًا. غالبًا ما يُساعد هذا النهج على وقف تفاقم داء النشواني وتحسين وظائف الكبد.
يتطلب داء النشواني الأولي استخدام الأدوية الوقائية الكيميائية وفي بعض الأحيان زراعة نخاع العظم.
توصي المبادئ التوجيهية الحالية باستخدام مزيج من السيكلوفوسفاميد، والبورتيزوميب، والديكساميثازون (CyBorD)، والداراتوموماب كعلاج من الخط الأول للمرضى الذين تم تشخيص إصابتهم حديثًا بمرض AL.
بورتيزوميب مثبط للبروتيزوم. تساهم البروتيزومات في تقليل سمية البروتينات وتنظيم البروتينات التي تتحكم في تطور الخلايا وموت الخلايا المبرمج. تتميز الخلايا البلازمية التي تُنتج الأميلويد بحساسية خاصة لتثبيط البروتيزوم، لاعتمادها عليه لتقليل الآثار السامة للسلاسل الخفيفة ومنع موت الخلايا المبرمج.
داراتوموموماب هو جسم مضاد وحيد النسيلة (mAb) يرتبط بـ CD38، وهو جليكوبروتين غشائي يُعبَّر عنه على سطح الخلايا البلازمية، مُحفِّزًا بذلك موت الخلايا المبرمج. وهو الدواء الوحيد المُعتمد خصيصًا لعلاج داء النشواني AL عند استخدامه مع CyBorD. فعالية CyBorD-daratumumumab عالية جدًا، حيث حقق 78% من المرضى استجابة دموية ملحوظة (تُعرَّف بأنها استجابة كاملة أو استجابة جزئية جيدة جدًا). بلغ متوسط البقاء على قيد الحياة في المجموعة الصغيرة من المرضى الذين تلقوا CyBorD (عدد المرضى = 15) 655 يومًا، مقارنةً بـ 178 يومًا للمرضى الذين تلقوا علاجات أخرى قائمة على ميلفالان-ديكساميثازون (عدد المرضى = 10). 4
ومع ذلك، فإن هذه العلاجات لها آثار جانبية عديدة، بما في ذلك السمية القلبية، مما يؤدي إلى الحاجة إلى خفض الجرعة أو تعليق العلاج، واستخدام استراتيجيات علاجية أخرى أقل فعالية ولكن أكثر قابلية للتحمل.
يتم دراسة عقار Isatuximab، وهو جسم مضاد وحيد النسيلة ضد CD38 يشبه عقار Daratumumab، لعلاج خلل تنسج الخلايا البلازمية الكامن وراء مرض AL.
تُجرى حاليًا دراسة ثلاثة أجسام مضادة وحيدة النسيلة، وهي بيرتاميماب، وCAEL-101، وAT-03، لإزالة ألياف الأميلويد من الأعضاء المريضة. وستُقدم نتائج هذه الدراسات دليلًا مباشرًا على الفرضية القائلة بأن إزالة ألياف ترسب السلسلة الخفيفة من الأعضاء يُحسّن وظائفها. [ 21 ]
لدعم وظائف الكبد، تُوصف أدوية تحتوي على حمض أورسو-ديوكسيكوليك (مثل أورسوسان). يُساعد حمض أورسو-ديوكسيكوليك على تثبيت أغشية الخلايا، ويُقلل من الآثار السلبية للأحماض الدهنية السامة في ركود الصفراء الناتج عن رواسب الأميلويد، ويُساعد على استعادة تدفق الصفراء الطبيعي.
بالإضافة إلى ذلك، العلاج العرضي ودعم عمل الهياكل الحيوية الأخرى مثل الجهاز العصبي والقلب والكلى وما إلى ذلك. يشمل العلاج الداعم للمرضى الذين يعانون من داء النشواني الكبدي جوانب سريرية مختلفة، بما في ذلك علاج قصور القلب، وعدم انتظام ضربات القلب، واضطرابات التوصيل، والانسداد الخثاري، والوجود المصاحب لتضيق الأبهر.
تعتمد العلاجات الأخرى على نوع داء النشواني وأجزاء الجسم المصابة. قد تشمل العلاجات ما يلي: [ 22 ]
- الأدوية التي تخفف الأعراض، مثل مسكنات الألم، أو أدوية الغثيان، أو الأدوية التي تقلل التورم (مدرات البول)؛
- الأدوية لتقليل الأميلويد؛
- غسيل الكلى؛
- زراعة الكبد.
يُنتج الكبد 95% من TTR (ترانسثيريتين، وهو بروتين يشارك في نقل الثيروكسين (T4) وبروتين ربط الريتينول. يُصنع الترانسثيريتين بشكل أساسي في الكبد وهو غني بخيوط بيتا التي تميل إلى التكتل في لييفات أميلويد غير قابلة للذوبان) المقاسة في المصل. لذلك، اقتُرح تاريخيًا (منذ عام 1990) إجراء عملية زرع الكبد كعلاج من الدرجة الأولى للقضاء على المصدر الرئيسي لـ TTR المُسبب للأميلويد لدى المرضى المصابين بالشكل العائلي (ATTRv)، بينما لا يُنصح به في الشكل ATTR-wt. يرتبط زرع الكبد للمرضى الشباب في المراحل المبكرة من المرض بمعدل بقاء مرتفع لمدة 20 عامًا. يبدو أن زرع الكبد أكثر فعالية في بعض الطفرات وأقل فعالية في أخرى، مثل V122I (المرتبط باعتلال عضلة القلب). من الممكن أيضًا إجراء عملية زرع الكبد والقلب معًا في مرضى ATTRv الشباب المصابين باعتلال عضلة القلب، وتشير بيانات الأدبيات حول مجموعة صغيرة من المرضى إلى أن هذا الجمع له تشخيص أفضل من عملية زرع القلب وحدها.
يُمنع مرضى داء النشواني الكبدي تناول الجليكوسيدات القلبية ومضادات الكالسيوم مثل ديلتيازيم أو فيراباميل، لأنها قد تتراكم في الأميلويد. وتُستخدم مثبطات الإنزيم المحول للأنجيوتنسين وحاصرات بيتا بحذر.
في حالة انخفاض ضغط الدم الانتصابي، تُوصف الكورتيكوستيرويدات المعدنية أو الجلوكوكورتيكوستيرويدات، مع الأخذ في الاعتبار أنها قد تُسبب اختلالًا في تعويض قصور القلب. كما يُستخدَم ميدودرين ألفا-أدرينوميميتيك (غوترون) بحذر.
تعتبر مضادات الاختلاج ومضادات الاكتئاب مناسبة في حالات الاعتلال العصبي.
في بعض حالات داء النشواني الكبدي، قد يفكر الأطباء في إجراء عملية زرع العضو.
الوقاية
نظراً لنقص المعلومات حول مسببات داء النشواني الكبدي، لا يستطيع الأخصائيون تطوير وقاية محددة منه. لذلك، تقتصر الجهود الرئيسية على الكشف المبكر عن أي أمراض مزمنة قد تُسبب تطور المرض وعلاجها. في حال وجود حالات داء نشواني من أي نوع في العائلة، يُنصح بزيارة الطبيب بانتظام لإجراء فحوصات طبية.
بشكل عام، تقتصر التدابير الوقائية على القضاء على الأمراض المُعدية في الوقت المناسب، وخاصةً تلك التي تميل إلى التحول إلى أمراض مزمنة. ويتعلق الأمر بمنع تطور مرض السل والتهابات الرئة، وما إلى ذلك. ومن المهم الكشف المبكر عن عدوى العقديات وعلاجها بشكل مناسب، لأنها قد تُسبب أشكالاً مزمنة من الالتهابات المناعية الذاتية. ونعني بذلك التهاب اللوزتين القرمزي، والتهاب العقديات، وما إلى ذلك.
إذا كان المريض يعاني بالفعل من مرض مناعي ذاتي، فيجب عليه استشارة الطبيب بشكل منهجي، ومراقبة نشاط المرض، وتطبيق الأدوية اللازمة حسب وصف الطبيب، وضبط الجرعات حسب المؤشرات.
توقعات
إن تشخيص مرضى داء النشواني الكبدي غير مواتٍ. يتفاقم المرض ببطء ولكن باستمرار، مما يؤدي في النهاية إلى خلل في وظائف الأعضاء المصابة، ويؤدي إلى الوفاة، لا سيما بسبب فشل الأعضاء.
يموت المرضى المصابون بأمراض جهازية بشكل رئيسي نتيجة تطور الفشل الكلوي المزمن، مع أن غسيل الكلى الدموي أو غسيل الكلى البريتوني المستمر يُحسّن في بعض الحالات من تشخيص هؤلاء المرضى. ويمكن مقارنة معدل بقاء مرضى غسيل الكلى الدموي، بغض النظر عن نوعه، بمعدل بقاء الأشخاص المصابين بأمراض جهازية أخرى وداء السكري.
السبب الرئيسي للوفاة أثناء غسيل الكلى هو تطور المضاعفات من الجهاز القلبي الوعائي.
لطالما اعتُبرت زراعة الكبد إحدى الطرق الرئيسية لعلاج هذا المرض، وتُلاحظ أعلى معدلات البقاء على قيد الحياة لدى المرضى الذين لا يتجاوز عمرهم 50 عامًا (بشرط أن تكون العملية المرضية قصيرة الأمد وأن يكون مؤشر كتلة الجسم طبيعيًا). أما المرضى الذين يعانون من داء النشواني الكبدي المصحوب باعتلال الأعصاب المحيطية، فيكون تشخيصهم أسوأ بعض الشيء.

