خبير طبي في المقال
منشورات جديدة
تشخيص مراحل دورة سرطان البروستاتا التشخيصية
آخر مراجعة: 04.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
سريريًا، يتم التمييز بين السرطان الموضعي (T 1-2 ، N 0 ، M 0 )، والسرطان المتقدم موضعيًا (T 3-4 ، N 0-1 ، M 0 ) والسرطان المنتشر (T 1-4 ، N 0-1 ، M 1 ).
يتم تصنيف المرضى الذين يعانون من مراحل سريرية موضعية ومرحلة متقدمة موضعيًا وفقًا لدرجة الخطر (D'Amico A V. et al.، 2003):
- منخفض: المرحلة T 1a-c ؛ مستوى PSA أقل من 10 ig/ml: تصنيف جليسون - 2-5؛ في الخزعة - آفة أحادية الجانب أقل من 50%:
- معتدل: المرحلة T 2a ؛ مستوى PSA أقل من 10 نانوغرام/مل؛ درجة جليسون - 3 + 4 = 7؛ في الخزعة - الآفة الثنائية أقل من 50٪؛
- مرحلة عالية من T 2b ، T 3a-b ؛ مستوى PSA - 10-20 نانوغرام/مل؛ تصنيف جليسون - أكثر من 4 + 3 - 7؛ في الخزعة - تلف أكثر من 50%، غزو عصبي؛
- مرتفع جدًا: المرحلة T 4 ؛ مستوى PSA أعلى من 20 نانوغرام/مل؛ درجة جليسون أعلى من 8؛ تُظهر الخزعة غزوًا للأوعية اللمفاوية.
بعد توضيح التشخيص وتحديد مدى تطور الحالة (موضعية، متقدمة موضعيًا ، أو معممة)، يواجه الطبيب والمريض خيارًا للعلاج. في المجتمع الحديث، تُولي جودة حياة المرضى بعد بدء العلاج أهمية كبيرة. تتوافق جودة الحياة بدون علاج مع مسار المرض الأساسي وتعتمد على تطور العملية السرطانية. تحدث تغيرات في جودة الحياة بشكل رئيسي بعد بدء العلاج واستخدام إحدى الطرق العلاجية أو الجراحية. إن تحديد مرحلة المرض بدقة يسمح ليس فقط باختيار طريقة العلاج الأمثل، بل أيضًا بالتنبؤ بمسار المرض.
إن تحديد مستوى PSA ، بالتزامن مع الصورة السريرية لسرطان البروستاتا وتصنيف الورم وفقًا لمقياس غليسون، يزيد بشكل ملحوظ من محتوى المعلومات لكل مؤشر من المؤشرات المذكورة في تحديد المرحلة المرضية للسرطان. اقترح أ. ف. بارتين وآخرون (1997) جداول تشخيصية تسمح بالتنبؤ بانتشار الورم، واختيار طريقة العلاج، ودرجة تطرفه، وتوقع فعالية العلاج.
لتقييم انتشار الورم، من أكثر الطرق شيوعًا فحص المستقيم الرقمي (DRE)، وفحص المستقيم عبر المستقيم (TRUS)، وتحديد مستوى مستضد البروستاتا النوعي (PSA)، وتصوير العظام الومضاني. عند الضرورة، يُنصح بإجراء التصوير المقطعي المحوسب (CT) أو التصوير بالرنين المغناطيسي (MRI) وأشعة سينية على الصدر.
صُممت جميع طرق التصوير لتحديد مرحلة المرض وتقييم فعالية العلاج. بعد التأكد من التشخيص، يجب على طبيب المسالك البولية توضيح حجم الورم الأولي وحدوده واحتمالية انتشاره أو انتشاره. جميع هذه المؤشرات بالغة الأهمية لتشخيص المرض واختيار طريقة العلاج.
الورم الأولي (T)
أولاً، من الضروري تحديد ما إذا كان الورم يقتصر على غدة البروستاتا (T 1-2 ) أو يمتد إلى ما وراء الكبسولة (T 3-4 ). لا يسمح الفحص الرقمي عادةً بتقييم انتشار الورم. ووفقاً لبعض البيانات، فإن نتائج الفحص الرقمي تتوافق مع نتائج الفحص النسيجي في أقل من 50% من المرضى. ومع ذلك، لا يُنصح بإجراء فحص أكثر تفصيلاً إلا عند اتخاذ قرار العلاج الجذري.
قد يعكس مستوى PSA مدى الورم، ولكنه لا يسمح بتحديد دقيق لمرحلته المورفولوجية. يتيح الجمع بين مستوى PSA ومؤشر غليسون وبيانات الجس تنبؤًا أفضل بالمرحلة المورفولوجية مقارنةً بكل معيار على حدة. تُعدّ قيمة PSA الحر مثيرة للجدل: ففي إحدى الدراسات، ساعد تحديد محتوى PSA الحر في تحديد مرحلة الورم في الأورام الموضعية، لكن دراسات أخرى لم تؤكد ذلك. وحدها الدراسات المتعمقة هي التي ستساعد في حل هذه المشكلة.
تُستخدم الموجات فوق الصوتية عبر المستقيم غالبًا لفحص حالة غدة البروستاتا. لا تكشف هذه الطريقة إلا عن 60% من الأورام، ولا تُظهر دائمًا غزو الكبسولة. يُلاحظ ذلك لدى ما يقرب من 60% من مرضى المرحلة T3 . تشير الموجات فوق الصوتية إلى عملية أقل شيوعًا. تشمل علامات الموجات فوق الصوتية لغزو الكبسولة انتفاخًا وعدم استواء وتمزقًا في محيط الغدة. يُعد غزو الخلايا السرطانية للحويصلات المنوية علامة تشخيصية ضعيفة، ولكن المعلومات المتعلقة بها بالغة الأهمية لاختيار طريقة العلاج. عند إجراء الموجات فوق الصوتية عبر المستقيم، يجب الانتباه إلى بنية الحويصلات (فرط الصدى)، وعدم تناسقها، وتشوهها، وتمددها. كما يُشير فقدان الاستدارة والضغط عند قاعدة الغدة إلى تلف الحويصلات المنوية. هذه العلامات ذاتية تمامًا، لذا من غير المناسب الاعتماد كليًا على بيانات الموجات فوق الصوتية. يشير غزو الحويصلات المنوية إلى خطر كبير للانتكاس الموضعي والنقائل، ويُوصى بأخذ خزعة منها للتوضيح (قبل الجراحة). لا ينبغي أن يبدأ الفحص بهذا الإجراء، ولكن إذا كان خطر الغزو مرتفعًا ويعتمد اختيار العلاج على نتيجة الخزعة، فإن تنفيذه يكون مبررًا. النتيجة السلبية لا تستبعد الغزو المجهري. وكقاعدة عامة، يتم إجراء خزعة للحويصلات المنوية في المرحلة السريرية T 2b وأعلى وكان محتوى PSA أكثر من 10 نانوغرام/مل. وتعتبر النتيجة إيجابية إذا كانت خزعة واحدة على الأقل من قاعدة غدة البروستاتا تحتوي على خلايا ورمية. ليس فقط الدراسات الإضافية، ولكن أيضًا التحليل الشامل لنتائج الخزعة الأولية يسمح بزيادة دقة التحديد السريري للمرحلة (يلعب عدد ومدى بؤر الورم وغزو الكبسولة دورًا). درجة التمايز مهمة أيضًا: مع مؤشر جليسون أقل من 6، يكون الورم موضعيًا في 70٪ من الحالات.
يكون تدفق الدم في غدة البروستاتا المصابة بالسرطان أعلى منه في الغدة الطبيعية أو في حالة تضخمها. بعد الإخصاء، تنخفض شدة تدفق الدم في الغدة. يُعد تطوير خرائط صدى دوبلر لتشخيص ومراقبة سرطان البروستاتا أمرًا واعدًا، ولكن لا توجد حاليًا بيانات موثوقة حول استخدام صدى دوبلر في تحديد مرحلة العملية الموضعية. من الممكن استخدام هذه الطريقة للحصول على مواد إضافية أثناء الخزعة المستهدفة من بؤر الأوعية الدموية المرضية.
تعتمد نتائج تصوير سرطان البروستاتا بشكل مباشر على التجهيزات التقنية للعيادة وخبرة الطبيب المختص. ولذلك، لا تلعب جميع أساليب التصوير الحديثة دورًا حاسمًا، بل دورًا توضيحيًا، ويعتمد اختيار طريقة العلاج على مزيج من بيانات الفحص السريري والدراسات العملية.
يتمتع التصوير بالرنين المغناطيسي بأفضل القدرات لتصوير بنية غدة البروستاتا. المعيار الحديث لفحص أعضاء الحوض باستخدام طريقة التصوير بالرنين المغناطيسي هو استخدام مستشعر داخلي مستقيمي، مما يسمح بالحصول على صورة بأعلى دقة مكانية ممكنة تتراوح بين 0.5 و1 مم. يوفر دفع الهواء إلى المستشعر الداخلي المستقيمي رؤية واضحة لمحفظة البروستاتا، وزوايا المستقيم والبروستاتا، ولفافة دينونفيلييه المستقيمية البروستاتا. لا يحد استخدام المستشعر الداخلي المستقيمي في التصوير بالرنين المغناطيسي من تصوير العقد الليمفاوية الإقليمية (حتى مستوى تشعب الشريان الأورطي البطني). يتميز سرطان البروستاتا بانخفاض شدة الإشارة في الصور المرجحة بـ T، على خلفية إشارة عالية الكثافة من منطقة محيطية ثابتة من الغدة. الشكل غير المنتظم، والانتشار المنتشر مع تأثير الكتلة، والخطوط الضبابية وغير المتساوية هي خصائص مورفولوجية للبؤر منخفضة الشدة في المنطقة المحيطية من غدة البروستاتا، مما يشير إلى طبيعة الورم السرطانية. عند إجراء التباين الديناميكي، تتراكم مادة التباين بسرعة في بؤر السرطان في الطور الشرياني، وتُزال المادة بسرعة، مما يعكس درجة تكوّن الأوعية الدموية، وبالتالي درجة خباثة الورم. كما أن انخفاض شدة الإشارة يُميز بؤر النزيف بعد الخزعة، والتهاب البروستاتا، وفرط تنسج الأنسجة الحميد في المنطقة المحايدة من الغدة، والتغيرات الليفية الندبية، وفرط تنسج العضلات الليفية، وآثار العلاج الهرموني أو الإشعاعي. لا يسمح التصوير بالرنين المغناطيسي بدون تباين ديناميكي بالتمييز الدقيق لمعظم التغيرات والأمراض المذكورة.
كما ذُكر سابقًا، فإن إحدى المهام الرئيسية لأي طريقة تصوير لسرطان البروستاتا هي تحديد حجم آفة الغدة وانتشار الورم خارج الكبسولة. يُعد تحديد حجم الورم أمرًا بالغ الأهمية للتنبؤ. يشير حجم الورم الأقل من 4 سم مكعب إلى نقائل بعيدة، بينما يشير 12 سم مكعب إلى احتمالية عالية جدًا لحدوث نقائل. ووفقًا للدراسات، تتراوح دقة التصوير بالرنين المغناطيسي في الكشف عن بؤر الآفات الورمية في غدة البروستاتا بين 50% و90%. وتتراوح حساسية التصوير بالرنين المغناطيسي في تحديد موقع سرطان البروستاتا بين 70% و80% تقريبًا، بينما لا يمكن الكشف عن البؤر المجهرية للسرطان باستخدام التصوير بالرنين المغناطيسي.
من أهم مزايا تصوير المستقيم بالرنين المغناطيسي القدرة على تحديد مواقع الآفات الورمية في مناطق يصعب الوصول إليها بوسائل التشخيص الأخرى، وتوضيح طبيعة واتجاه نمو الورم. على سبيل المثال، يُمكّن التصوير بالرنين المغناطيسي من الكشف عن الآفات الورمية في الأجزاء الأمامية من المنطقة الطرفية لغدة البروستاتا، والتي يتعذر الوصول إليها بالخزعة عبر المستقيم. وبشكل عام، يُكمّل التصوير بالرنين المغناطيسي بشكل كبير بيانات فحص المستقيم الرقمي (DRE) والفحص عبر المستقيم عبر المستقيم (TRUS) المتعلقة بتحديد موقع الورم.
يتيح تصوير الرنين المغناطيسي داخل المستقيم تصوير كبسولة الغدة، والحزم العصبية الوعائية، والحويصلات المنوية، وقمة الغدة، والضفيرة الوريدية حول البروستاتا، وتحديد الانتشار الموضعي لورم الغدة. تجدر الإشارة إلى أن اختراق الكبسولة يُعدّ علامة مجهرية، وحتى أجهزة الرنين المغناطيسي الحديثة (اللولب داخل المستقيم) غير قادرة على توفير هذه المعلومات. لا يمكن الحصول إلا على بيانات حول النمو خارج كبسولة الغدة.
معايير التشخيص للامتداد خارج المحفظة باستخدام التصوير بالرنين المغناطيسي:
- وجود ورم خارج المحفظة؛
- محيط الغدة غير المتساوي (التشوه، الزاوية)؛
- عدم تناسق الحزم العصبية الوعائية؛
- إزالة الزوايا المستقيمية البروستاتية؛
- اتصال واسع بين الورم والكبسولة.
تُحقق نتائج التصوير بالرنين المغناطيسي أعلى دقة وخصوصية (تصل إلى 95-98%) عند فحص المرضى المعرضين لخطر متوسط أو مرتفع للغزو خارج الكبسولة. يُعتقد أن الغزو خارج الكبسولة (وفقًا لبيانات التصوير بالرنين المغناطيسي) يشير إلى عدم ملاءمة العلاج الجراحي وتوقعات غير مواتية للمرض. لا يؤثر العلاج الهرموني أو الإشعاعي على دقة الكشف عن انتشار ورم البروستاتا خارج الكبسولة. تكمن الصعوبة الرئيسية في الكشف عن بؤر السرطان وانتشار الورم خارج الكبسولة في التباين الكبير في تفسيرات التصوير المقطعي من قِبل مختلف المتخصصين. تتمثل المهمة الأساسية لأخصائي التشخيص الإشعاعي في تحقيق خصوصية تشخيصية عالية (حتى على حساب الحساسية) لتجنب حرمان المرضى الذين يخضعون للجراحة من فرصة العلاج الجذري.
إن تشابه كثافة أنسجة البروستاتا السرطانية والمتضخمة والطبيعية في التصوير المقطعي المحوسب يجعل هذه الطريقة قليلة الفائدة في تقييم الانتشار الموضعي للورم. يُعدّ غزو الحويصلات المنوية أكثر أهمية من غزو الكبسولات، ولكن حتى في هذه الحالة، لا يوفر التصوير المقطعي المحوسب معلومات إلا في الحالات المتقدمة. ومع ذلك، تُستخدم هذه الطريقة بفعالية لتحديد منطقة التأثير قبل العلاج الإشعاعي.
أدى التطور البطيء للتشخيص الإشعاعي في بلدنا إلى تأخر تشخيص سرطان البروستاتا، وبالتالي إلى نقص انتشار الطرق الجذرية لعلاجه (مثل استئصال البروستاتا)، وقلة توفر أجهزة التصوير المقطعي الحديثة، وغياب برامج تدريبية مناسبة لأخصائيي التشخيص الإشعاعي وأطباء المسالك البولية. ورغم انتشار التصوير المقطعي المحوسب والتصوير بالرنين المغناطيسي، إلا أن مستوى تجهيزات العيادات ومستوى تعليم أخصائيي التشخيص الإشعاعي لا يكفيان لجعل المعلومات المُحصل عليها حاسمة في اختيار طريقة علاج مرضى سرطان البروستاتا.
العقد الليمفاوية الإقليمية (N)
يجب تقييم الغدد الليمفاوية الإقليمية فقط عندما يؤثر ذلك بشكل مباشر على استراتيجية العلاج (عادةً عند التخطيط لعلاج جذري). ترتبط مستويات PSA المرتفعة، وأورام T2c -T3a ، وضعف التمايز، والغزو العصبي بارتفاع خطر نقائل الغدد الليمفاوية. يُعتبر تقييم حالة الغدد الليمفاوية بناءً على مستويات PSA غير كافٍ.
استئصال الغدد الليمفاوية (المفتوحة أو بالمنظار) وحده هو الذي يوفر المعلومات اللازمة. أظهرت الدراسات الحديثة لاستئصال الغدد الليمفاوية الموسع أن سرطان البروستاتا لا يؤثر دائمًا على الغدد الليمفاوية السدادية. في الأورام غير المصحوبة بأعراض ومستويات PSA أقل من 20 كجم/مل، يؤكد التصوير المقطعي المحوسب تضخم الغدد الليمفاوية في 1% فقط من الحالات. يُعد استخدام التصوير بالرنين المغناطيسي أو التصوير المقطعي المحوسب مبررًا في حالات ارتفاع خطر النقائل، حيث تصل دقة هذه الطرق إلى 93-96%. ومع ذلك، حتى النتيجة الإيجابية عند استخدامها قد تكون خاطئة، ولا يسمح سوى ثقب العقدة الليمفاوية المشتبه بها برفض استئصال العقد الليمفاوية. وفقًا للتحليل بأثر رجعي، لا يشير حجم العقدة الليمفاوية دائمًا إلى وجود نقائل فيها؛ ويُعتبر عدم تناسق العقد الليمفاوية المصابة علامة أكثر دلالة. حاليًا، يتم تشخيص 2-3% فقط من المرضى الذين خضعوا لاستئصال البروستاتا الجذري لسرطان البروستاتا الموضعي بنقائل إلى العقد الليمفاوية بناءً على الفحص النسيجي بعد الجراحة.
يوصى باستخدام التصوير المقطعي بالإصدار البوزيتروني (PET) والتصوير الومضاني باستخدام الأجسام المضادة الموسومة كطرق للكشف عن النقائل في الغدد الليمفاوية، ولكن استخدامها لا يزال محدودًا بسبب عدم كفاية الحساسية.
يمكن استخدام مخططات بارتين (2001) لتقييم خطر إصابة العقدة الليمفاوية الإقليمية. المخططات هي خوارزميات رياضية تُستخدم لمريض محدد أو مجموعة من المرضى. تسمح هذه الجداول بتحديد احتمال انتشار الورم الموضعي (إلى الكبسولة والحويصلات المنوية) وإصابة العقدة الليمفاوية بناءً على المرحلة السريرية ومستوى PSA ومؤشر غليسون. على وجه الخصوص، تتيح هذه الجداول تحديد مجموعة من المرضى الذين لديهم احتمال منخفض (أقل من 10٪) لنقائل العقدة الليمفاوية (مع مستوى PSA أعلى من 20 نانوغرام / مل، المرحلة T 1-2a ، ومؤشر غليسون 2-6)؛ في هذه المجموعة، قد لا يتم تحديد حالة العقد الليمفاوية قبل العلاج الجذري. يمكن أيضًا تقييم خطر نقائل العقدة الليمفاوية من خلال الكشف عن مناطق الورم ذات التنسج الواضح (4-5 نقاط): إذا تم العثور على هذه المناطق في أربع خزعات أو أكثر أو كانت سائدة في خزعة واحدة على الأقل، فإن الخطر يصل إلى 20-45٪. في مرضى آخرين، لا تتجاوز النسبة 2.5%. لا حاجة لفحوصات إضافية في مثل هذه الحالات.
النقائل البعيدة (م)
في 85% من المرضى الذين يموتون بسبب سرطان البروستاتا، يتم اكتشاف آفات في الهيكل العظمي المحوري. تحدث نقائل العظام بسبب اختراق الخلايا السرطانية لنخاع العظم مع مجرى الدم، مما يؤدي إلى نمو الورم وتحلل الهياكل العظمية. يؤثر انتشار نقائل العظام على التشخيص، واكتشافها المبكر يحذر الطبيب من المضاعفات المحتملة. في 70% من الحالات، يقترن النقائل بزيادة في نشاط إيزوزيم العظام للفوسفاتاز القلوي (ALP). يسمح لنا تحديد نشاط ALP ومستوى PSA في الغالبية العظمى من الحالات باكتشاف نقائل العظام. وفقًا للتحليل متعدد المتغيرات، تتأثر هذه المؤشرات فقط بعدد نقائل العظام. من المهم أن يعكس نشاط إيزوزيم العظام ALP درجة تلف العظام بدقة أكبر من مستوى PSA.
يُعد التصوير الومضاني الطريقة الأكثر حساسية للكشف عن نقائل العظام (وهو أفضل من التصوير الشعاعي وتحديد نشاط الفوسفاتاز القلوي والحمضي). تُستخدم ثنائيات فوسفونات التكنيشيوم بشكل أفضل كدواء صيدلاني مشع، نظرًا لأن تراكمها في العظام يكون أكثر نشاطًا منه في الأنسجة الرخوة. وقد ثبت وجود علاقة بين التقييم شبه الكمي لتلف العظام وبقاء المريض على قيد الحياة. يُمكن الكشف عن النقائل البعيدة في أي عضو، وغالبًا ما تحدث في العقد الليمفاوية غير الإقليمية، والرئتين، والكبد، والدماغ، والجلد. في حالة وجود شكاوى وأعراض مماثلة، تُستخدم الأشعة السينية للصدر، والموجات فوق الصوتية، والتصوير المقطعي المحوسب، والتصوير بالرنين المغناطيسي للكشف عنها. يوضح الرسم التخطيطي أساليب الكشف عن النقائل العظمية المشتبه بها.
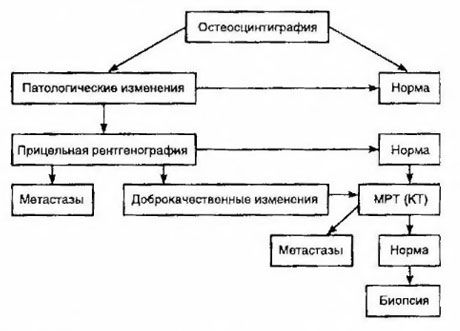
يُعد مستوى PSA المؤشر المخبري الأكثر موثوقية لتحديد درجة انتشار الورم. وقد ثبت أن ارتفاعه عن 100 نانوغرام/مل هو المعيار الوحيد الذي يشير بدقة إلى وجود نقائل بعيدة. يُقلل تحديد مستوى PSA من عدد المرضى الذين يحتاجون إلى تصوير العظام بالومضان. احتمال اكتشاف نقائل العظام مع انخفاض مستوى PSA منخفض جدًا. في حال عدم وجود شكاوى، وكان مستوى PSA الأولي أقل من 20 نانوغرام/مل، يُمكن تجنب الكشف عن الأورام شديدة التمايز والمتوسطة التمايز، باستخدام التصوير الومضاني. في الوقت نفسه، في حالة الأورام ضعيفة التمايز وغزو الكبسولة، يُنصح باستخدام التصوير الومضاني (بغض النظر عن مستوى PSA).


 [
[