خبير طبي في المقال
منشورات جديدة
أسباب الدفتيريا ومسبباتها المرضية
آخر مراجعة: 04.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
الخناق (الدفتيريا) نموذجٌ للأمراض المعدية المُسبِّبة للسموم. في عام ١٨٨٣، أثبت كليبس أن بكتيريا الوتدية الخناقية هي العامل المسبب للخناق. وبعد عام، وجد لوفلر أن هذه البكتيريا لا يمكن استنباتها إلا من تجويف البلعوم الأنفي، واقترح أن تلف الأعضاء الداخلية ناتج عن سمٍّ قابل للذوبان. وبحلول عام ١٨٨٨، أظهر رو ويرسين أن الحيوانات التي حُقِنت براشح معقمة من بكتيريا الوتدية الخناقية تُصاب بأمراض عضوية لا يمكن تمييزها عن تلك المُصاحبة للخناق البشري؛ وهذا يُثبت أن السم الخارجي القوي هو عامل الضراوة الرئيسي.
الخناق (الدفتيريا) هو عدوى تصيب الجهاز التنفسي العلوي غالبًا، وتُسبب الحمى والتهاب الحلق والشعور بالضيق. غالبًا ما يتكون غشاء فيبرين سميك، رمادي مخضر، وهو غشاء كاذب، في موقع (مواقع) العدوى نتيجةً للتأثيرات المشتركة لنمو البكتيريا، وإنتاج السموم، ونخر الأنسجة الكامنة، والاستجابة المناعية للمضيف. وقد أدى إدراك أن تلف الأعضاء الجهازية ناتج عن تأثير سم الخناق إلى تطوير علاج فعال قائم على مضادات السموم لعلاج العدوى الحادة، بالإضافة إلى لقاح توكسيدي عالي الفعالية.
على الرغم من أن التطعيم بالتوكسويد جعل الخناق مرضًا نادرًا في المناطق التي تشترط فيها معايير الصحة العامة التطعيم، إلا أن تفشي الخناق لا يزال يحدث بين الفئات غير المحصنة أو ضعيفة المناعة. في المقابل، حدثت فاشيات واسعة النطاق من الخناق بلغت أبعادًا وبائية في المناطق التي عُلقت فيها برامج التطعيم النشطة.
أنواع أخرى من البكتيريا الوتدية
بالإضافة إلى الكوليرا الخناقية، والكوليرا القرحة، والكوليرا السلية الكاذبة، قد تُسبب الكوليرا الخناقية الكاذبة والكوليرا الجفافية أحيانًا التهابات أنفية بلعومية وجلدية. وتتميز السلالتان الأخيرتان بقدرتهما على إنتاج بيرازيناميداز. في الطب البيطري، تُعتبر الكوليرا الكلوية والكوليرا الكوتشيرية من مسببات الأمراض المهمة، إذ تُسبب التهاب الحويضة والكلية لدى الماشية والالتهابات الكامنة لدى الفئران، على التوالي.
الأسباب
العامل المسبب لمرض الخناق، Corynebacterium diphtheriae، هو قضيب رفيع منحني قليلاً مع سماكة على شكل نادي في الأطراف، ثابت؛ لا يشكل أبواغًا أو كبسولات أو أسواطًا، وهو إيجابي الجرام.
بالإضافة إلى السم، تنتج بكتيريا الخناق الكورينيباكتيريا النورامينيداز، والهيالورونيداز، والهيموليزين، والعوامل النخرية والمنتشرة أثناء عملياتها الحيوية، والتي يمكن أن تسبب نخرًا وتسييلًا للمادة الرئيسية في النسيج الضام.
بناءً على قدرتها على تكوين السموم، تنقسم بكتيريا الخناق إلى بكتيريا سامة وغير سامة.
سُمّ الخناق هو سمّ خارجي بكتيري قوي يُحدد المظاهر السريرية العامة والموضعية للمرض. تُحدَّد سمّية الخناق وراثيًا. لا تُسبِّب البكتيريا الوتدية غير المُسبِّبة للخناق المرض.
وفقًا للخصائص الثقافية والشكلية، تُقسّم جميع أنواع بكتيريا الدفتيريا إلى ثلاثة أنواع: وبيل، وميتيس، وإنترميديوس. لا توجد علاقة مباشرة بين شدة المرض ونوع بكتيريا الدفتيريا. يحتوي كل نوع على سلالات سامة وغير سامة. تُنتج بكتيريا الدفتيريا السامة لجميع الأنواع سمًا متطابقًا. [ 1 ]
البنية والتصنيف وأنواع المستضدات
بكتيريا الخناق الوتدية هي بكتيريا موجبة الجرام، غير متحركة، على شكل عصا. تحتوي السلالات التي تنمو في الأنسجة أو المزارع القديمة في المختبر على بقع دقيقة في جدران الخلايا، مما يسمح بإزالة اللون أثناء صبغ غرام، ويؤدي إلى تفاعل غرام متغير. غالبًا ما تحتوي المزارع القديمة على حبيبات ميتاكروماتية (بولي ميتافوسفات) تتلون باللون الأرجواني المزرق مع أزرق الميثيلين. تشمل سكريات جدار الخلية الأرابينوز والجالاكتوز والمانوز. بالإضافة إلى ذلك، يمكن عزل إستر 6,6'-السام من التريهالوز، والذي يحتوي على أحماض كورينيميكوليك وكورينيميكولينيك بتركيزات متساوية المولات. هناك ثلاثة أنواع مميزة من المزارع: ميتيس، إنترميديوس، غرافيس.
تتطلب معظم السلالات حمضي النيكوتين والبانتوثينيك للنمو؛ ويتطلب بعضها أيضًا الثيامين والبيوتين وحمض البيميليك. لإنتاج سموم الخناق على النحو الأمثل، يجب إضافة الأحماض الأمينية إلى الوسط، ويجب تركه جانبًا.
في وقت مبكر يعود إلى عام ١٨٨٧، وصف لوفلر عزل سلالات عديمة الفوعة (غير مُولِّدة للسم) من بكتيريا الخناق، والتي لم يكن من الممكن تمييزها عن السلالات المُولِّدة للسم المعزولة من مرضى لدى أفراد أصحاء. ومن المُسلَّم به الآن أن سلالات عديمة الفوعة من بكتيريا الخناق يمكن أن تتحول إلى نمط ظاهري مُولِّد للسم بعد العدوى والتحلل بواسطة إحدى عاثيات الوتدية المميزة التي تحمل الجين الهيكلي لسم الخناق، وهو "توكس". ويمكن أن يحدث التحول التحللي للنمط الظاهري غير المُولِّد للسم إلى نمط ظاهري مُولِّد للسم في كلٍّ من الموقع وفي المختبر. ولا يُعد الجين الهيكلي لسم الخناق ضروريًا لكلٍّ من عاثيات الوتدية أو بكتيريا الخناق. وعلى الرغم من هذه الملاحظة، لم يُلاحَظ أي انحراف وراثي لسم الخناق.
طريقة تطور المرض
نقاط دخول العدوى هي الأغشية المخاطية للبلعوم الفموي والأنف والحنجرة، وفي حالات نادرة الأغشية المخاطية للعينين والأعضاء التناسلية، بالإضافة إلى الجلد التالف، وأسطح الجروح أو الحروق، وطفح الحفاضات، وجرح السرة غير الملتئم. عند نقطة الدخول، تتكاثر بكتيريا الخناق الوتدية وتفرز سمومًا خارجية.
يُفرز إفراز غني بالفيبرينوجين، ويتحول إلى فيبرين تحت تأثير الثرومبوكيناز المُفرز أثناء نخر الخلايا الظهارية. ويتكون غشاء فيبريني، وهو علامة مميزة للدفتيريا.
يُعدّ الحمل الأنفي البلعومي بدون أعراض شائعًا في المناطق الموبوءة بالدفتيريا. في الأفراد المعرضين للإصابة، تُسبب السلالات المُولِّدة للسم المرض عن طريق تكاثر وإفراز سم الدفتيريا في البلعوم الأنفي أو آفات الجلد. غالبًا ما تُغطى آفة الدفتيريا بغشاء كاذب يتكون من الفيبرين والبكتيريا والخلايا الالتهابية. يمكن تقسيم سم الدفتيريا بروتينيًا إلى شظيتين: الشظية A الطرفية الأمينية (المجال التحفيزي) والشظية B (مجالات عبر الغشاء وربط المستقبلات). تُحفّز الشظية A عملية ريبوزيل عامل الاستطالة 2 المعتمدة على NAD+ وADP، مما يُثبّط تخليق البروتين في الخلايا حقيقية النواة. ترتبط الشظية B بمستقبل سطح الخلية، وتُسهّل إيصال الشظية A إلى السيتوزول.
تتضمن المناعة الوقائية استجابة الأجسام المضادة لسم الخناق بعد المرض السريري أو لسم الخناق (السم الذي يتم تعطيله بالفورمالديهايد) بعد التحصين.
الاستعمار
لا يُعرف الكثير عن العوامل التي تُتوسط استعمار بكتيريا الدفتيريا الخناقية. ومع ذلك، من الواضح أن عوامل أخرى غير إنتاج سموم الدفتيريا تُساهم في ضراوة المرض. وقد أظهرت الدراسات الوبائية أن نمطًا ليزوتيًا معينًا يمكن أن يستمر في مجموعة سكانية لفترات طويلة. وقد يُستبدل لاحقًا بنمط ليزوتي آخر. ويُفترض أن ظهور نمط ليزوتي جديد وسيطرة هذا النمط الليزوتي في مجموعة سكانية يرتبط بقدرته على الاستعمار والتنافس بفعالية في قطاعه من البيئة الأنفية البلعومية. تستطيع بكتيريا الدفتيريا الخناقية إنتاج إنزيم النورامينيداز، الذي يُحلل حمض السياليك الموجود على سطح الخلية إلى مكوناته: البيروفات وحمض N-أسيتيل نورامينيك. يُعد عامل الحبل السري (6،6'-داي-O-مايكولوويل-α، α'-D-تريهالوز) أحد مكونات سطح بكتيريا الدفتيريا الخناقية، ولكن دوره في استعمار المضيف البشري غير واضح.
إنتاج سموم الدفتيريا
ينتمي الجين الهيكلي لسم الخناق، توكس، إلى عائلة من البكتيريا الوتدية وثيقة الصلة، ويُعدّ فاج بيتا أكثرها دراسة. يتم تنظيم التعبير عن سم الخناق بواسطة مثبط منشط بالحديد، DtxR، والذي يُشفره جينوم الدفتيريا الخناقية. يعتمد التعبير عن السم على الحالة الفسيولوجية للدفتيريا الخناقية. في الظروف التي يصبح فيها الحديد ركيزة تحد من معدل النمو، ينفصل الحديد عن DtxR، ويُنشط جين التسمم، ويتم تصنيع سم الخناق وإفرازه في وسط الزرع بأقصى معدلاته.
سُمّ الخناق قويٌّ بشكلٍ غير عادي؛ فبالنسبة للأنواع الحساسة (مثل البشر، والقرود، والأرانب، وخنازير غينيا)، تُعتبر جرعةٌ ضئيلةٌ تتراوح بين 100 و150 نانوغرام/كغ من وزن الجسم قاتلةً. يتكون سُمّ الخناق من سلسلة بولي ببتيد واحدة من 535 حمضًا أمينيًا. يُظهر التحليل الكيميائي الحيوي، والجينيّ، والتحليل البنيويّ بالأشعة السينية أن السُمّ يتكون من ثلاثة مجالاتٍ بنيوية/وظيفية:
- ADP-ريبوزيل ترانسفيراز الطرفي الأميني (المجال التحفيزي)؛
- منطقة تسهل توصيل المجال التحفيزي عبر غشاء الخلية (المجال عبر الغشاء)؛
- مجال ربط مستقبلات الخلايا حقيقية النواة.
بعد هضم واختزال التربسين الخفيف في ظروف تغيير الطبيعة، يمكن تقسيم سم الخناق تحديدًا عند حلقته الحساسة للبروتياز إلى قطعتين بولي ببتيديتين (أ و ب). القطعة أ هي المكون الطرفي الأميني للسمّ، بوزن 21 كيلو دالتون، وتحتوي على الموقع التحفيزي لريبوزلة عامل الاستطالة 2 (EF-2) بواسطة ADP.
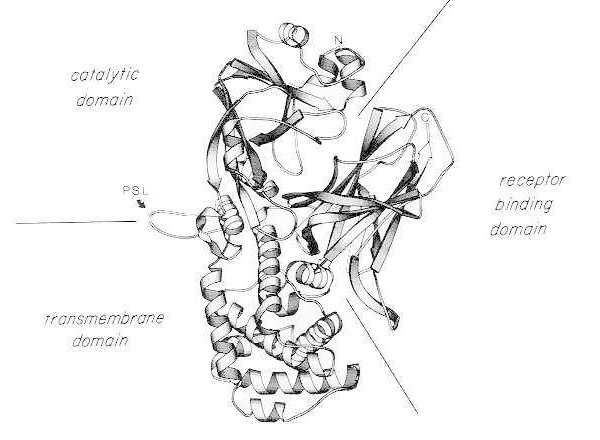
مخطط شريطي للبنية البلورية بالأشعة السينية لسم الخناق أحادي القُسيم. (مُعدَّل من بينيت إم جيه، تشوي إس، آيزنبرغ دي: تبادل النطاقات: تشابك التحالفات بين البروتينات. وقائع الأكاديمية الوطنية للعلوم، الولايات المتحدة الأمريكية، 91: 3127، 1994). يُوضَّح الموقع النسبي للمجالات التحفيزية، والمجالات عبر الغشائية، ومجالات ربط المستقبلات. يمكن تقسيم السم السليم بواسطة بروتيازات شبيهة بالتربسين في Arg190، وArg192، و/أو Arg193، الموجودة في الحلقة الحساسة للبروتياز (PSL). بعد اختزال جسر ثنائي الكبريتيد بين Cys186 وCys201، يمكن تحليل السم إلى شظايا A وB. كما هو موضح الطرف الأميني (N) والطرف الكربوكسيلي (C) للسم السليم. تم إنشاء مخطط الشريط باستخدام برنامج MOLESCRIPT.
يحمل الجزء الطرفي C، الجزء B، المجالات عبر الغشاء ومجالات ربط المستقبلات الخاصة بالسم.
تتضمن عملية تسميم خلية حقيقية النواة بسموم الدفتيريا أربع خطوات مميزة على الأقل:
- ارتباط السم بمستقبلاته على سطح الخلية؛
- تجميع المستقبلات المشحونة في حفر مغلفة واستيعاب السم عن طريق البلعمة الذاتية بوساطة المستقبلات؛ بعد تحميض الحويصلة البلعمة الذاتية بواسطة مضخة بروتون مرتبطة بالغشاء مدفوعة بـ ATP،
- إدخال المجال عبر الغشاء إلى الغشاء وتسهيل توصيل المجال التحفيزي إلى السيتوزول، و
- ADP-ribosylation من EF-2، مما يؤدي إلى قمع لا رجعة فيه لتخليق البروتين.
وقد ثبت أن جزيئًا واحدًا من المجال التحفيزي الذي يتم إدخاله إلى السيتوزول كافٍ ليكون قاتلًا للخلية.
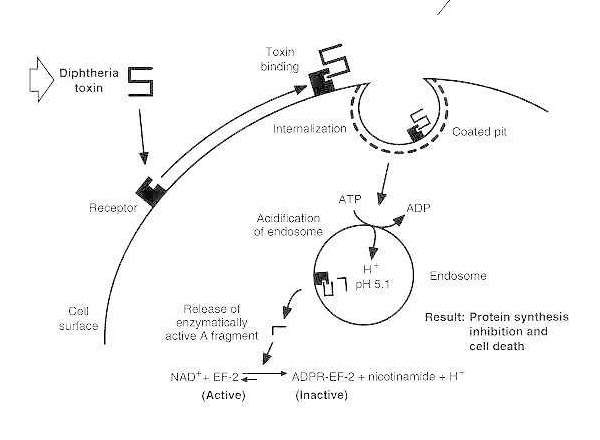
رسم تخطيطي لتسمم الخناق في خلية حقيقية النواة قابلة للإصابة.
يرتبط السم بمستقبل سطح الخلية ويتم إدخاله إلى داخل الخلية عن طريق البلعمة بوساطة المستقبلات؛ وعند تحميض الجسيم الداخلي، يتم إدخال المجال عبر الغشاء في غشاء الحويصلة؛ ويتم توصيل المجال التحفيزي إلى السيتوزول، مما يؤدي إلى تثبيط تخليق البروتين وموت الخلايا.
علم الأوبئة
قبل التطعيم الشامل لسكان الولايات المتحدة الأمريكية بلقاح الدفتيريا، كان الدفتيريا مرضًا يصيب الأطفال عادةً. ومن الجوانب اللافتة للتطعيم الشامل بلقاح الدفتيريا أنه مع ازدياد نسبة السكان الذين لديهم مستويات وقائية من مناعة مضادات السموم (≥ 0.01 وحدة دولية/مل)، يتناقص تواتر عزل السلالات المسببة للسم من السكان. أما اليوم، ففي الولايات المتحدة الأمريكية، حيث اختفى الدفتيريا السريرية تقريبًا تمامًا، يُعد عزل السلالات المسببة للسم من بكتيريا الدفتيريا الخناقية أمرًا نادرًا. ونظرًا لأن العدوى دون السريرية لم تعد مصدرًا للتعرض لمستضد الدفتيريا، ولأن المناعة ضد مضادات السموم تتضاءل ما لم تُعزز، فإن نسبة كبيرة من البالغين (30 إلى 60%) لديهم مستويات مضادات سموم أقل من المستويات الوقائية وهم معرضون للخطر. وفي الولايات المتحدة الأمريكية وأوروبا وأوروبا الشرقية، حدثت حالات تفشي الدفتيريا الأخيرة بشكل رئيسي بين الأفراد الذين يتعاطون الكحول و/أو المخدرات. ضمن هذه المجموعة، يتمتع حاملو الدفتيريا المُسبِّبة للسم بمستوى عالٍ نسبيًا من المناعة المضادة للسم. وقد أدى انهيار تدابير الصحة العامة مؤخرًا في روسيا إلى تحوّل الدفتيريا إلى وباء. وبحلول نهاية عام ١٩٩٤، سُجِّلت أكثر من ٨٠ ألف حالة إصابة وأكثر من ٢٠٠٠ حالة وفاة في روسيا.
غالبًا ما ترتبط حالات تفشي الخناق البؤري بحامل مناعي عاد من منطقة يتوطن فيها الخناق. في الواقع، ارتبطت حالات تفشي الخناق السريري الأخيرة في الولايات المتحدة وأوروبا بمسافرين عائدين من روسيا وأوروبا الشرقية. تنتقل سلالات الدفتيريا المُولِّدة للسم مباشرةً من شخص لآخر عبر الرذاذ المحمول جوًا. ومن المعروف أن السلالات المُولِّدة للسم تستطيع استعمار تجويف البلعوم الأنفي مباشرةً. بالإضافة إلى ذلك، يمكن أن ينتشر الجين المُولِّد للسم بشكل غير مباشر عن طريق إطلاق البكتيريا الوتدية المُولِّدة للسم والتحول المُسَلِّط لبكتيريا الدفتيريا الأصلية غير المُولِّدة للسم في موقعها. [ 5 ]
بالإضافة إلى تحديد النمط الحيوي والليزوتيبي لعزلات بكتيريا الخناق، يُمكن الآن استخدام تقنيات البيولوجيا الجزيئية لدراسة تفشي الخناق. وقد استُخدمت أنماط هضم إنزيم النوكلياز المقيّد للحمض النووي الكروموسومي لبكتيريا الخناق لدراسة تفشي المرض سريريًا، وكذلك استخدام تسلسلات إدخال البكتيريا الوتدية المستنسخة كمسبار جيني.
استُخدم اختبار شيك لسنوات عديدة لتقييم المناعة ضد سمّ الخناق، على الرغم من أنه استُبدل الآن في العديد من المجالات بالاختبار المصلي للأجسام المضادة النوعية لسمّ الخناق. في اختبار شيك، تُحقن كمية صغيرة من سمّ الخناق (حوالي 0.8 نانوغرام في 0.2 مل) داخل الأدمة في الساعد (موقع الاختبار)، ويُحقن 0.0124 ميكروغرام من سمّ الخناق في 0.2 مل داخل الأدمة في موقع الاختبار. تُؤخذ القراءات بعد 48 و96 ساعة. عادةً ما تبلغ تفاعلات الجلد غير النوعية ذروتها بعد 48 ساعة. بعد 96 ساعة، يُشير رد فعل احمراري مع احتمال حدوث نخر في موقع الاختبار إلى عدم كفاية المناعة المضادة للسم لتحييد السم (≤ 0.03 وحدة دولية/مل). يشير الالتهاب في كل من مناطق الاختبار والتحكم بعد 48 ساعة إلى حدوث رد فعل فرط الحساسية لمستحضر المستضد.
إستمارات
تصيب بكتيريا الخناق الوتدية البلعوم الأنفي أو الجلد. تُنتج السلالات المُولِّدة للسم سمًا خارجيًا قويًا قد يُسبب الخناق. تشمل أعراض الخناق التهاب البلعوم والحمى وتورم الرقبة أو المنطقة المحيطة بالآفة الجلدية. تُغطى الآفات الخناقية بغشاء كاذب. ينتشر السم عبر مجرى الدم إلى أعضاء بعيدة، وقد يُسبب الشلل وفشل القلب الاحتقاني. [ 6 ]
هناك نوعان من الخناق السريري: أنفي بلعومي وجلدي. تتراوح أعراض الخناق البلعومي من التهاب بلعومي خفيف إلى نقص الأكسجين بسبب انسداد مجرى الهواء بغشاء كاذب. قد يُسبب تأثر الغدد الليمفاوية العنقية تورمًا شديدًا في الرقبة (خناق رقبة الثور)، وقد يُصاب المريض بحمى (≥ 103 درجة فهرنهايت). عادةً ما تُغطى الآفات الجلدية في الخناق الجلدي بغشاء كاذب رمادي-بني. قد تتطور مضاعفات جهازية مهددة للحياة، أبرزها فقدان الوظيفة الحركية (مثل صعوبة البلع) وفشل القلب الاحتقاني، نتيجةً لتأثير سم الخناق على الخلايا العصبية الحركية الطرفية وعضلة القلب.
يتحكم
تعتمد السيطرة على الخناق على التحصين الكافي بذيفان الخناق: وهو ذيفان يُعطَّل بالفورمالديهايد، ويبقى سليمًا مستضديًا. يُحضَّر هذا الذيفان بحضن ذيفان الخناق مع الفورمالديهايد عند درجة حرارة 37 درجة مئوية في ظروف قلوية. يجب أن يبدأ التحصين ضد الخناق في الشهر الثاني من العمر بثلاث جرعات أولية متتالية، بفاصل زمني يتراوح بين 4 و8 أسابيع، تليها جرعة رابعة بعد عام تقريبًا من آخر جرعة أولية. يُستخدم ذيفان الخناق على نطاق واسع كجزء من لقاح الخناق والسعال الديكي والكزاز (DPT). وقد أظهرت الدراسات الوبائية أن فعالية التحصين ضد الخناق تبلغ حوالي 97%. على الرغم من أن التحصين الشامل ضد الخناق يُمارس في الولايات المتحدة وأوروبا، وأن معدلات تحصين الأطفال كافية، إلا أن نسبة كبيرة من البالغين قد تكون مستويات الأجسام المضادة لديهم أقل من المستويات الوقائية. يجب إعادة تطعيم البالغين بلقاح الدفتيريا كل عشر سنوات. في الواقع، يجب إعطاء جرعة مُعزّزة من لقاح الدفتيريا والكزاز للمسافرين إلى المناطق التي ترتفع فيها معدلات انتشار الدفتيريا (أمريكا الوسطى والجنوبية، وأفريقيا، وآسيا، وروسيا، وأوروبا الشرقية). في السنوات الأخيرة، ساهم استخدام مستحضرات الدفتيريا عالية النقاء للتحصين في الحد من تفاعلات فرط الحساسية الشديدة العرضية. ينبغي إعطاء جرعة معززة من لقاح الدفتيريا والكزاز للمسافرين إلى المناطق التي ترتفع فيها معدلات انتشار الدفتيريا المتوطنة (أمريكا الوسطى والجنوبية، أفريقيا، آسيا، روسيا، وأوروبا الشرقية). في السنوات الأخيرة، قلّل استخدام مستحضرات الدفتيريا عالية النقاء للتحصين من تفاعلات فرط الحساسية الشديدة العرضية.
على الرغم من استخدام المضادات الحيوية (مثل البنسلين والإريثروميسين) كجزء من علاج مرضى الخناق، إلا أن التطعيم السلبي السريع بمضاد سم الخناق هو الأكثر فعالية في تقليل الوفيات. يُعدّ طول عمر النصف لمضاد السم النوعي في مجرى الدم عاملاً هاماً في ضمان فعالية تحييد سم الخناق؛ ومع ذلك، لكي يكون فعالاً، يجب أن يتفاعل مضاد السم مع السم قبل دخوله إلى الخلية.
إعادة هندسة سموم الدفتيريا لتطوير سموم خلوية خاصة بمستقبلات حقيقية النواة
هندسة البروتينات مجالٌ جديدٌ وسريع التطور في علم الأحياء الجزيئي؛ فهو يجمع بين منهجيات الحمض النووي المُعاد التركيب وتخليق الحمض النووي في الطور الصلب لتصميم وبناء جينات كيمرية تتميز منتجاتها بخصائص فريدة. وقد أظهرت دراسات العلاقة بين البنية والوظيفة في سم الخناق بوضوح أن هذا السم بروتينٌ ثلاثي النطاقات: مُحفِّز، وعبر غشائي، ومستقبل. وقد أمكن استبدال نطاق ارتباط المستقبلات الأصلي في سم الخناق وراثيًا بهرمونات وسيتوكينات متعددة الببتيد (مثل: هرمون تحفيز الخلايا الصباغية α-MSH، والإنترلوكين (IL) 2، وIL-4، وIL-6، وIL-7، وعامل نمو البشرة). تجمع البروتينات الكيميرية الناتجة، أو سموم الاندماج، بين خصوصية ارتباط السيتوكين بالمستقبلات والنطاقين عبر الغشائي والتحفيزي للسم. في كل حالة، تبين أن سموم الاندماج تُسمم بشكل انتقائي الخلايا التي تحمل مستقبل الهدف المقابل فقط. أول هذه السموم الاندماجية المعدلة وراثيًا، DAB 389IL-2، قيد التقييم حاليًا في التجارب السريرية البشرية لعلاج الأورام اللمفاوية المقاومة وأمراض المناعة الذاتية التي تلعب فيها الخلايا ذات مستقبلات IL-2 عالية الألفة دورًا مهمًا في التسبب في المرض. [ 7 ] وقد ثبت أن إعطاء DAB 389 IL-2 آمن وجيد التحمل وقادر على إحداث هدأة دائمة للمرض دون آثار جانبية خطيرة. ومن المرجح أن تصبح سموم الاندماج القائمة على سم الخناق عوامل بيولوجية جديدة مهمة لعلاج أورام أو أمراض محددة يمكن فيها استهداف مستقبلات سطح الخلية المحددة.


 [
[