خبير طبي في المقال
منشورات جديدة
الداء الليفي الأرومي الليفي
آخر مراجعة: 05.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
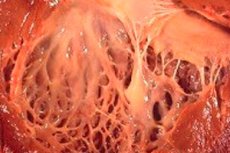
في الطب، يشير مصطلح "التليف المرن" إلى تغيرات في النسيج الضام للجسم الذي يغطي سطح الأعضاء الداخلية والأوعية الدموية، ناجمة عن خلل في نمو الألياف المرنة. في الوقت نفسه، يُلاحظ سماكة في جدران الأعضاء وبنيتها، مما يؤثر سلبًا على وظائف الأجهزة الحيوية في الجسم، وخاصة الجهازين القلبي الوعائي والتنفسي. وهذا بدوره يؤدي إلى تدهور صحة المريض، وخاصة أثناء المجهود البدني، مما يؤثر على جودة الحياة ومدتها.
علم الأوبئة
بشكل عام، يمكن تقسيم الأمراض المصحوبة بتغيرات في النسيج الضام، والتي تؤدي إلى سماكة أغشية الأعضاء الداخلية وحواجزها، إلى مجموعتين: التليف القلبي المرن والتليف الرئوي المرن. يمكن أن يكون مرض القلب خلقيًا ومكتسبًا؛ أما الشكل الرئوي للمرض، فهو مرض مكتسب.
يبدأ التليف الرئوي المرن بالتطور في منتصف العمر (أقرب إلى 55-57 عامًا)، مع أنه في نصف الحالات، يجب البحث عن أصل المرض في مرحلة الطفولة. تتميز هذه الحالة بفترة "خفيفة" لا تظهر فيها أعراض المرض. في الوقت نفسه، لا يُحدد المرض جنس المريض، ويمكن أن يُصيب النساء والرجال على حد سواء. يتميز هذا المرض النادر بتغيرات في أنسجة غشاء الجنب والنسيج الرئوي (الخلايا الوظيفية) في الرئة، وخاصةً في الفص العلوي منها. ونظرًا لعدم وضوح مسببات المرض وتطوره، يُصنف المرض على أنه مرض مجهول السبب. ويُطلق عليه طبيًا اسم "التليف الرئوي الجنبي المرن". [ 1 ]
التليف المرن القلبي هو اسم عام لمرض يصيب أغشية القلب، ويتميز بسماكتها وانخفاض وظائفها. تتميز الأشكال الخلقية لهذا المرض بسماكة منتشرة في الغشاء الداخلي للقلب. وهو نسيج ضام رقيق يبطن تجويف القلب (أقسامه) ويشكل صماماته.
في المرضى البالغين، عادة ما يتم تشخيص الشكل البؤري للمرض، عندما يبدو أن السطح الداخلي للقلب مغطى ببقع من الأنسجة الأقوى والأكثر سمكًا (قد يشمل ليس فقط الألياف المتضخمة، ولكن أيضًا الكتل الخثارية).
في نصف حالات تليف القلب المرن، لا يزداد سمك جدار العضو فحسب، بل يزداد سمك الصمامات أيضًا (الصمام التاجي ثنائي الشرفات بين الأذين والبطين، والصمام الأورطي ثلاثي الشرفات بين البطين الأيسر والشريان الأورطي، والصمام الرئوي بين البطين الأيمن والشريان الرئوي). وهذا بدوره قد يُعطل عمل الصمامات ويُسبب تضيق فتحة الشريان، وهي صغيرة أصلًا مقارنةً بتجاويف القلب الأخرى.
في المصطلحات الطبية، يُطلق على تليف الشغاف اسم تليف الشغاف (تليف ما قبل الولادة، تصلب الشغاف، التهاب الشغاف الجنيني، إلخ). ولكن في كثير من الأحيان، قد تشارك الطبقة العضلية الوسطى من غشاء القلب في هذه العملية أيضًا. [ 2 ]
يمكن أن تُسبب التشوهات في بنية عضلة القلب (الطبقة العضلية للقلب، المكونة من خلايا عضلية)، والطفرات الجينية، والعمليات المعدية الشديدة، شكلاً شائعًا من التليف المرن، عندما لا يقتصر الأمر على الشغاف فحسب، بل يشمل عضلة القلب أيضًا. عادةً، تحدث عمليات خلل التنسج في الشغاف، لأسباب مختلفة، عند حدود تماسه مع الغشاء العضلي، مما يُعطل انقباض هذه الطبقة. في بعض الحالات، يحدث نموٌّ للطبقة الداخلية في عضلة القلب، واستبدال خلايا عضلة القلب بأرومات ليفية وألياف، مما يؤثر على توصيل النبضات العصبية وإيقاع القلب.
يؤدي ضغط الأوعية الدموية في سمك الغشاء القلبي بواسطة عضلة القلب السميكة إلى تعطيل تغذية عضلة القلب (نقص تروية عضلة القلب)، مما قد يؤدي بدوره إلى نخر أنسجة عضلة القلب.
يُطلق على التليف المرن الشغافي مع تلف عضلة القلب اسم التليف المرن تحت الشغاف أو التليف المرن الشغافي.
وبحسب الإحصائيات، في معظم حالات هذا المرض النادر (0.007% فقط من إجمالي عدد المواليد الجدد)، يتم تشخيص تليف البطين الأيسر للقلب، على الرغم من أن العملية تنتشر في بعض الحالات أيضًا إلى البطين الأيمن والأذين، بما في ذلك الصمامات التي تفصل بينهما.
غالبًا ما يصاحب تليف القلب المرن تلف في الأوعية التاجية الكبيرة، المغطاة أيضًا بالنسيج الضام. وفي مرحلة البلوغ، غالبًا ما يحدث هذا على خلفية تصلب الشرايين الوعائي التدريجي.
يتم تسجيل المرض في أغلب الأحيان في البلدان الأفريقية الاستوائية بين السكان ذوي مستوى المعيشة المنخفض، وهو ما يسهله سوء التغذية والالتهابات المتكررة وتناول بعض الأطعمة والنباتات كغذاء.
يُلاحظ أيضًا سماكة الشغاف في المرحلة الأخيرة من التهاب الشغاف الليفي للوفلر، والذي يُصيب الرجال في منتصف العمر بشكل رئيسي. ترتبط آلية هذا المرض أيضًا بعوامل مُعدية تُسبب فرط الحمضات الشديد، وهو أكثر شيوعًا في حالات العدوى الطفيلية الداخلية. في هذه الحالة، تبدأ أنسجة الجسم (وخاصةً عضلة القلب والدماغ) في المعاناة من نقص الأكسجين (نقص الأكسجة). على الرغم من تشابه أعراض تليف القلب الليفي والتهاب الشغاف الليفي للوفلر، إلا أن الأطباء يعتبرونهما مرضين مختلفين تمامًا.
الأسباب داء الأرومة الليفية
يشير مصطلح "التليف المرن" إلى تغيرات في النسيج الضام في الأعضاء الحيوية: القلب والرئتين، والتي تصاحبها اضطرابات في وظائف الأعضاء، وتنعكس على مظهر المريض وحالته الصحية. يعرف الأطباء هذا المرض منذ عقود. وُصف التليف المرن في البطانة الداخلية للقلب (الشغاف) في أوائل القرن الثامن عشر، وبدأت مناقشة تغيرات مماثلة في الرئتين بعد قرنين ونصف. ومع ذلك، لم يتوصل الأطباء بعد إلى اتفاق نهائي حول أسباب الانتشار المرضي للنسيج الضام.
لا يزال السبب الدقيق لاضطراب نمو وتطور الألياف الضامة غير واضح. لكن العلماء حددوا عوامل خطر معينة لهذه التغيرات، معتبرينها أسبابًا محتملة (ولكن ليست نهائية) للمرض.
وهكذا، في تطور مرض التليف الرئوي المرن، الذي يُعتبر مرضًا يصيب البالغين، تُعطى الإصابات المعدية المتكررة في هذا العضو دورًا خاصًا، وهي موجودة لدى نصف المرضى. تُسبب العدوى التهابًا في أنسجة الرئة والجنبة، ويُهيئ الالتهاب طويل الأمد لتحولهما إلى أنسجة ليفية.
لدى بعض المرضى تاريخ عائلي للإصابة بداء الليفية المرنة، مما يشير إلى وجود استعداد وراثي. وقد عُثر على أجسام مضادة ذاتية غير نوعية في أجسامهم، مما يُحفز عمليات التهابية طويلة الأمد ذات أسباب غير معروفة.
يُعتقد أن التغيرات الليفية في أنسجة الرئة قد تكون ناجمة عن مرض الارتجاع المعدي المريئي. مع أن هذه الصلة غالبًا ما تكون غير مباشرة. ويُعتقد أيضًا أن خطر الإصابة بالتليف المرن يكون أعلى لدى المصابين بأمراض القلب والأوعية الدموية أو الخثار الرئوي.
قد يُلاحظ التليف الرئوي المرن لدى الشباب والمراهقات ظهوره خلال فترة الحمل. عادةً ما يكون المرض خفيًا لعشر سنوات أو أكثر، ولكنه قد يظهر مبكرًا، ربما بسبب زيادة الحمل على جسم الأم الحامل والتغيرات الهرمونية، ولكن لا يوجد تفسير دقيق حتى الآن. مع ذلك، لوحظت صورة مشابهة لتطور المرض لدى 30% من المرضى في سن الإنجاب الذين خضعوا للفحص.
الحمل في حد ذاته لا يمكن أن يسبب المرض، لكنه يمكن أن يسرع من تطور الأحداث، وهو أمر محزن للغاية، لأن معدل الوفيات بسبب هذا المرض مرتفع للغاية، ومتوسط العمر المتوقع مع مرض التليف المرن قصير.
في معظم الحالات، يُعزى تليف القلب المرن إلى أمراض الطفولة. يُكتشف هذا العيب الخلقي في فترة ما قبل الولادة لدى الجنين الذي يتراوح عمره بين 4 و7 أشهر، ولكن لا يُمكن تأكيد التشخيص إلا بعد الولادة. يُؤخذ في الاعتبار العديد من العوامل السلبية المُحتملة في التسبب بهذا النوع من المرض: الأمراض المعدية والالتهابية التي تنتقل من الأم إلى الجنين، وتشوهات في نمو أغشية القلب، وضعف إمداد أنسجة القلب بالدم، والطفرات الجينية، ونقص الأكسجين.
يُعتقد أن الفيروسات، من بين أنواع العدوى، تُسهم بشكل كبير في تطور تليف القلب، لأنها تستقر في خلايا الجسم، وتُدمرها، وتُغير خصائص الأنسجة. لا يستطيع الجهاز المناعي غير المُكتمل للجنين توفير الحماية له من هذه المُسببات المرضية، على عكس مناعة الأم الحامل. قد لا تُعاني الأم الحامل من عواقب العدوى الفيروسية، بينما قد تُسبب العدوى داخل الرحم لدى الجنين ظهور تشوهات مُختلفة.
يعتقد بعض العلماء أن الدور الحاسم في التسبب في الشكل المعدي من التليف المرن هو عدوى تصيب الجنين حتى عمر سبعة أشهر. وفي مراحل لاحقة، لا يمكن أن تسبب إلا أمراض القلب الالتهابية (التهاب عضلة القلب، التهاب الشغاف).
يمكن أن تحدث تشوهات في نمو الأغشية والصمامات في القلب بسبب العملية الالتهابية وردود الفعل المناعية الذاتية غير الكافية، ونتيجة لذلك تبدأ خلايا الجهاز المناعي بمهاجمة خلايا الجسم نفسه.
تؤدي الطفرات الجينية إلى تطور غير طبيعي للأنسجة الضامة، لأن الجينات تحتوي على معلومات حول بنية وسلوك البنى البروتينية (على وجه الخصوص، بروتينات الكولاجين والإيلاستين).
قد يكون نقص الأكسجين ونقص التروية في أنسجة القلب نتيجةً لنمو غير طبيعي للقلب. في هذه الحالة، نتحدث عن التليف المرن الثانوي، الناتج عن عيوب خلقية في القلب. وتشمل هذه العيوب التشوهات التي تسبب انسدادًا (ضعفًا في سالكية القلب وأوعيته الدموية):
- تضيق أو تضييق الشريان الأورطي بالقرب من الصمام،
- تضيق أو تضييق قطعي في الشريان الأورطي عند تقاطع قوسه مع قسمه النازل،
- تضيق أو غياب فتحة طبيعية في الشريان الأورطي،
- نقص نمو أنسجة القلب (غالبًا البطين الأيسر، وأقل شيوعًا البطين الأيمن والأذينين)، مما يؤثر على وظيفة ضخ القلب.
هناك رأي مفاده أن التسمم أثناء الحمل يمكن أن يكون أيضًا بمثابة عامل مؤهب لمرض التليف المرن في الجنين.
في فترة ما بعد الولادة، قد يُسهّل تطور تليف القلب المرن الإصابة بالأمراض المعدية والالتهابية في أغشية الأعضاء، واضطرابات الدورة الدموية الناتجة عن الإصابات، والانصمام الخثاري الوعائي، ونزيف عضلة القلب، والاضطرابات الأيضية (زيادة تكوين الفيبرين، واضطرابات استقلاب البروتين والحديد: الداء النشواني، وداء ترسب الأصبغة الدموية). وتؤدي الأسباب نفسها إلى تطور المرض لدى البالغين.
طريقة تطور المرض
النسيج الضام نسيجٌ خاصٌّ في جسم الإنسان، يُشكّل جزءًا من جميع أعضاء الجسم تقريبًا، ولكنه لا يُشارك بفعالية في وظائفها. يُعزى إليه وظائف الدعم والحماية. يُشكّل النسيج الضام نوعًا من الهيكل العظمي (الهيكل، السدى) ويُحدّد الخلايا الوظيفية للعضو، ويضمن شكله وحجمه النهائيين. بفضل قوته الكافية، يحمي النسيج الضام خلايا العضو من التلف والإصابة، ويمنع اختراق مسببات الأمراض، وبمساعدة خلايا البلاعم الخاصة، يمتصّ البنى القديمة: خلايا الأنسجة الميتة، والبروتينات الغريبة، ومكونات الدم الفاسدة، وغيرها.
يمكن تسمية هذا النسيج بالنسيج المساعد، لأنه لا يحتوي على عناصر خلوية تضمن وظائف أعضاء الجسم. ومع ذلك، فإن دوره في حياة الجسم كبير جدًا. كونه جزءًا من أغشية الأوعية الدموية، يضمن النسيج الضام سلامة هذه الهياكل ووظائفها، ويؤدي وظيفة التغذية والتنفس (الاستقلاب) للأنسجة المحيطة بالبيئة الداخلية للجسم.
هناك عدة أنواع من النسيج الضام. يُسمى الغشاء الذي يغطي الأعضاء الداخلية بالنسيج الضام الرخو. وهو مادة شبه سائلة عديمة اللون تحتوي على ألياف كولاجين متموجة وألياف إيلاستين مستقيمة، تنتشر بينها أنواع مختلفة من الخلايا بشكل عشوائي. بعض هذه الخلايا (الخلايا الليفية) مسؤولة عن تكوين البُنى الليفية، بينما تُشكل خلايا أخرى (الخلايا البطانية والخلايا البدينة) مصفوفة شفافة من النسيج الضام وتُنتج مواد خاصة (الهيبارين والهيستامين)، بينما تُوفر خلايا أخرى (الخلايا البلعمية) عملية البلعمة، إلخ.
النوع الثاني من الأنسجة الليفية هو النسيج الضام الكثيف، الذي لا يحتوي على عدد كبير من الخلايا الفردية، وينقسم بدوره إلى نسيجين: أبيض وأصفر. يتكون النسيج الأبيض من ألياف كولاجين متراصة بإحكام (الأربطة، الأوتار، السمحاق)، بينما يتكون النسيج الأصفر من ألياف إيلاستين متشابكة بشكل عشوائي مع شوائب من الخلايا الليفية (جزء من الأربطة، أغشية الأوعية الدموية، الرئتين).
تشمل الأنسجة الضامة أيضًا: أنسجة الدم والدهون والعظام والغضاريف، لكننا لسنا مهتمين بها بعد، لأننا، عند الحديث عن التليف المرن، نعني التغيرات في البُنى الليفية. أما الألياف المرنة والصلبة، فتوجد فقط في الأنسجة الضامة الرخوة والكثيفة.
يتم تنظيم تخليق الخلايا الليفية وتكوين ألياف النسيج الضام منها على مستوى الدماغ. وهذا يضمن ثبات خصائصها (القوة، المرونة، السُمك). إذا تعطل تخليق وتطور الأنسجة المساعدة، لأسباب مرضية (يزداد عدد الخلايا الليفية، ويتغير سلوكها)، يحدث تكاثر لألياف الكولاجين القوية أو تغير في نمو الألياف المرنة (تبقى قصيرة، ملتوية)، مما يؤدي إلى تغير في خصائص غشاء العضو وبعض البنى الداخلية المغطاة بالنسيج الضام. تكتسب هذه الألياف سُمكًا أكبر من اللازم، وتصبح أكثر كثافة وقوة وأقل مرونة، وتشبه النسيج الليفي في الأربطة والأوتار، مما يتطلب جهدًا كبيرًا للتمدد.
لا تتمدد هذه الأنسجة بشكل جيد، مما يحد من حركات الأعضاء (الحركات الإيقاعية التلقائية للقلب والأوعية الدموية، والتغيرات في حجم الرئتين أثناء الشهيق والزفير)، ومن ثم اضطراب إمدادات الدم والأعضاء التنفسية، مما يؤدي إلى نقص الأكسجين.
الحقيقة هي أن إمداد الجسم بالدم يتم بفضل القلب، الذي يعمل كمضخة، ودورتيْن دمويتيْن. الدورة الدموية الرئوية مسؤولة عن إمداد الدم وتبادل الغازات في الرئتين، حيث ينقل الأكسجين إلى القلب مع تدفق الدم، ومنه إلى الدورة الدموية الجهازية، ويوزعه في جميع أنحاء الجسم، موفرًا التنفس للأعضاء والأنسجة.
الغشاء المرن، الذي يحد من انقباض عضلة القلب، يُضعف وظيفة القلب، الذي لا يضخ الدم بكفاءة، ومعه الأكسجين. في حالة تليف الرئتين، تضعف تهويتهما (تكوين الصفيحات)، ومن الواضح أن كمية أقل من الأكسجين تبدأ في دخول الدم، مما يُسهم، حتى مع وظائف القلب الطبيعية، في نقص الأكسجين (نقص الأكسجة) في الأنسجة والأعضاء. [ 3 ]
الأعراض داء الأرومة الليفية
التليف المرن القلبي والرئوي نوعان من الأمراض يتميزان باضطراب في تخليق الألياف في النسيج الضام. يختلف موقعهما، لكن كلاهما قد يُهدد الحياة، إذ يرتبطان بفشل قلبي وتنفسي تدريجي أو حاد.
التليف الرئوي المرن هو نوع نادر من الأمراض الخلالية التي تصيب هذا العضو المهم في الجهاز التنفسي. وتشمل هذه الأمراض أمراضًا مزمنة في أنسجة الرئة مع تلف جدران الحويصلات الهوائية (التهاب، واختلال في بنيتها وبنيتها)، والبطانة الداخلية للشعيرات الدموية الرئوية، وغيرها. وغالبًا ما يُعتبر التليف الرئوي المرن شكلًا نادرًا من الالتهاب الرئوي التدريجي، مع ميل إلى حدوث تغيرات ليفية في أنسجة الرئة والجنبة.
يكاد يكون من المستحيل اكتشاف المرض في بدايته، إذ قد لا يظهر إلا بعد مرور عشر سنوات تقريبًا. تُسمى هذه الفترة بالفترة الواضحة. يمكن اكتشاف بداية التغيرات المرضية التي لم تؤثر بعد على حجم الرئتين وتبادل الغازات بالصدفة، أثناء فحص دقيق للرئتين مرتبطًا بمرض أو إصابة أخرى في الجهاز التنفسي.
يتميز هذا المرض بتطور بطيء للأعراض، لذا قد تتأخر الأعراض الأولى للمرض بشكل ملحوظ منذ بدايته. وتشتد الأعراض تدريجيًا.
أولى علامات المرض التي تستحق الاهتمام هي السعال وضيق التنفس المتزايد. غالبًا ما تكون هذه الأعراض نتيجةً لمرض تنفسي سابق، لذا قد ترتبط بنزلة برد وعواقبها على المدى الطويل. غالبًا ما يُنظر إلى ضيق التنفس على أنه اضطراب قلبي أو تغيرات مرتبطة بالعمر. في النهاية، يُشخص المرض لدى الأشخاص الذين يقتربون من سن الشيخوخة.
قد يرتكب المرضى والأطباء أخطاءً عند فحصهم، مما يؤدي إلى التأخر في اكتشاف مرض خطير. يجدر الانتباه إلى السعال، فهو غير مُنتج في حالة التليف الرئوي، ولكنه لا يُحفّز بمذيبات البلغم والمقشعات، بل تُوقفه مضادات السعال. يُعدّ السعال المُطوّل من هذا النوع عرضًا مُميزًا للتليف الرئوي.
يحدث ضيق التنفس نتيجة فشل تنفسي تدريجي نتيجة سماكة جدران الحويصلات الهوائية والجنبة، وانخفاض حجم وعدد التجاويف السنخية في الرئة (يظهر نسيج الحويصلات الهوائية في الأشعة السينية على شكل قرص العسل). تشتد الأعراض تحت تأثير المجهود البدني، وتكون كبيرة في البداية، ثم خفيفة. ومع تقدم المرض، يتفاقم، مما يؤدي إلى إعاقة المريض ووفاته.
يصاحب تطور مرض التليف المرن تدهور في الحالة العامة: نقص الأكسجين يؤدي إلى الضعف والدوار، وينخفض وزن الجسم (يتطور فقدان الشهية)، وتتغير سلاميات الأظافر إلى نوع أعواد الطبل، ويصبح الجلد شاحبًا وله مظهر مريض.
يُصاب نصف المرضى بأعراض غير محددة، مثل صعوبة التنفس وألم الصدر، وهي أعراض تُميز استرواح الصدر (تراكم الغازات في التجويف الجنبي). قد تحدث هذه الحالة أيضًا نتيجة إصابات، وأمراض رئوية أولية وثانوية، وعلاج غير مناسب، ما يجعل تشخيصها مستحيلًا.
يتميز تليف القلب المرن، بالإضافة إلى نمو النسيج الضام في الرئتين، بما يلي: شحوب الجلد، وفقدان الوزن، والضعف، الذي غالبًا ما يكون على شكل نوبات، وضيق التنفس. كما قد تُلاحظ أيضًا ارتفاع مستمر في درجة الحرارة دون أعراض نزلة برد أو عدوى.
يعاني العديد من المرضى من تغيرات في حجم الكبد، إذ يزداد حجمه دون ظهور أعراض خلل وظيفي. كما يُحتمل حدوث تورم في الساقين والوجه والذراعين ومنطقة العجز.
يُعتبر تفاقم قصور الدورة الدموية المرتبط باضطراب القلب من الأعراض المميزة للمرض. في هذه الحالة، يُشخَّص تسرع القلب (زيادة معدل ضربات القلب، وغالبًا ما يكون مصحوبًا باضطراب نظم القلب)، وضيق التنفس (حتى في غياب النشاط البدني)، وزرقة الأنسجة (تلون مزرق ناتج عن تراكم الكربوكسي هيموغلوبين في الدم، وهو مركب من الهيموغلوبين وثاني أكسيد الكربون نتيجةً لاضطراب تدفق الدم، وبالتالي اضطراب تبادل الغازات).
في هذه الحالة، قد تظهر الأعراض إما فور ولادة طفل مصاب بهذا المرض، أو على مدى فترة من الزمن. عند إصابة الأطفال الأكبر سنًا والبالغين، عادةً ما تظهر علامات قصور القلب الحاد على خلفية عدوى تنفسية، والتي تُعتبر بمثابة مُحفز. [ 4 ]
التليف المرن عند الأطفال
إذا كان التليف الرئوي المرن مرضًا يصيب البالغين، وينشأ غالبًا في مرحلة الطفولة، ولكنه لا يظهر إلا بعد فترة طويلة، فإن مرضًا مشابهًا يصيب بطانة القلب غالبًا ما يظهر حتى قبل ولادة الطفل، ويؤثر على حياته منذ اللحظات الأولى من ولادته. هذا المرض النادر، وإن كان شديدًا، هو سبب تطور قصور القلب الذي يصعب علاجه لدى الرضع، والذي يتوفى الكثير منهم في غضون عامين. [ 5 ]
في أغلب الأحيان، يكون تليف بطانة القلب لدى حديثي الولادة نتيجةً لعمليات مرضية تحدث في جسم الطفل خلال فترة ما قبل الولادة. العدوى المنقولة من الأم، والطفرات الجينية، وتشوهات نمو الجهاز القلبي الوعائي، والأمراض الأيضية الوراثية - كل هذا، وفقًا للعلماء، يمكن أن يؤدي إلى تغيرات في النسيج الضام في أغشية القلب. خاصةً إذا تعرض الجنين الذي يتراوح عمره بين 4 و7 أشهر لعاملين أو أكثر في الوقت نفسه.
على سبيل المثال، مجموعة من التشوهات في نمو القلب والأوعية التاجية (تضيق، رتق، تضيق الأبهر، نمو غير طبيعي لخلايا عضلة القلب، ضعف الشغاف، إلخ)، والتي تُسهم في نقص تروية الأنسجة، مقترنةً بعملية التهابية ناجمة عن عدوى، تُضعف فرص بقاء الطفل على قيد الحياة بشكل أو بآخر. وبينما يُمكن تصحيح عيوب نمو الأعضاء بسرعة، فإن تفاقم التليف المرن لا يُمكن إلا إبطاءه، ولكن لا يُمكن علاجه.
عادةً، يُكتشف تليف القلب لدى الجنين أثناء الحمل من خلال تشخيص الموجات فوق الصوتية في الثلث الثاني أو الثالث من الحمل. أظهرت الموجات فوق الصوتية وتخطيط صدى القلب في الفترة من 20 إلى 38 أسبوعًا فرطًا في صدى القلب، مما يشير إلى سماكة وانضغاط الشغاف (عادةً ما يكون منتشرًا، ونادرًا ما يكون بؤريًا)، وتغير في حجم وشكل القلب (يتضخم العضو ويتخذ شكل كرة أو رصاصة، وتتم تنعيم الهياكل الداخلية تدريجيًا). [ 6 ]
في 30-35% من الحالات، تم اكتشاف التليف المرن قبل الأسبوع السادس والعشرين من الحمل، وفي 65-70% منها في الفترة اللاحقة. في أكثر من 80% من المواليد الجدد، يترافق التليف المرن مع عيوب القلب الانسدادية، أي أنه ثانوي، على الرغم من المراحل المبكرة من اكتشافه. تم اكتشاف تضخم البطين الأيسر لدى نصف الأطفال المصابين، مما يفسر ارتفاع معدل انتشار التليف المرن في هذا الهيكل القلبي تحديدًا. كما تؤدي أمراض الشريان الأورطي وصمامه، التي تم تحديدها لدى ثلث الأطفال المصابين بتكاثر الشغاف، إلى زيادة (توسع) حجرة البطين الأيسر واختلال وظيفته.
في حالة تأكيد الإصابة بتليف القلب المرن باستخدام جهاز، ينصح الأطباء بإنهاء الحمل. وقد تأكدت أعراض المرض لدى جميع الأطفال تقريبًا الذين وُلدوا لرفض أمهاتهم الإجهاض الدوائي. تظهر أعراض قصور القلب، وهي سمة مميزة لتليف القلب المرن، خلال عام (نادرًا في السنة الثانية أو الثالثة من العمر). أما الأطفال المصابون بالشكل المختلط من المرض، فتُكتشف أعراض قصور القلب لديهم منذ الأيام الأولى من حياتهم.
غالبًا ما تتطور الأشكال الخلقية من التليف المرن الأولي والمختلط لدى الأطفال بسرعة، مصحوبة بتطور قصور القلب الحاد. قلة النشاط، وخمول الطفل، ورفضه الرضاعة الطبيعية بسبب التعب السريع، وضعف الشهية، وزيادة التعرق، كلها مؤشرات على اعتلال الصحة. كل هذا يؤدي إلى صعوبة اكتساب الطفل للوزن. يكون جلد الطفل شاحبًا بشكل مؤلم، مع لون مزرق لدى البعض، وغالبًا ما يكون في المثلث الأنفي الشفوي.
تظهر علامات ضعف المناعة، ولذلك يُصاب هؤلاء الأطفال بالتهابات الجهاز التنفسي بسرعة، مما يُعقّد الوضع. أحيانًا، لا يُظهر الطفل أي اضطرابات في الدورة الدموية خلال الأيام والأشهر الأولى من حياته، لكن الالتهابات المتكررة وأمراض الرئة تُصبح مُحفّزًا لتطور قصور القلب الاحتقاني.
أظهرت الفحوصات الصحية الإضافية لحديثي الولادة والأطفال الصغار المشتبه بإصابتهم بالتليف المرن أو الذين شُخِّصوا سابقًا انخفاض ضغط الدم، وتضخم حجم القلب (تضخم القلب)، وأصوات مكتومة عند سماع نبضات القلب، وأحيانًا نفخة انقباضية مميزة لقصور الصمام التاجي، وتسارع القلب، وضيق التنفس. أما عند سماع نبضات الرئتين، فيُظهر وجود أزيز، مما يشير إلى احتقان.
غالبًا ما يؤدي تلف الشغاف في البطين الأيسر إلى إضعاف الطبقة العضلية للقلب (عضلة القلب). يتكون إيقاع القلب الطبيعي من نغمتين متناوبتين إيقاعيًا. في حالة التليف المرن، قد تظهر نغمة ثالثة (وأحيانًا رابعة). يُسمع هذا الإيقاع المرضي بوضوح، ويشبه في صوته مشية الحصان ثلاثية الضربات (العدو)، ولذلك يُسمى إيقاع العدو.
من أعراض التليف المرن لدى الأطفال الصغار ظهور حدبة قلبية. في الواقع، تبقى أضلاع الطفل في فترة ما بعد الولادة المبكرة غير متعظمة، وتتمثل بأنسجة غضروفية. يؤدي ازدياد حجم القلب إلى ضغطه على الأضلاع "اللينة"، مما يؤدي إلى انحناءها واكتسابها شكلًا منحنيًا للأمام بشكل دائم (حدبة قلبية). في حالة التليف المرن لدى البالغين، لا تتشكل حدبة قلبية بسبب قوة وصلابة النسيج العظمي للأضلاع، حتى مع زيادة جميع هياكل القلب.
إن تكوّن الحدبة القلبية بحد ذاته لا يدل إلا على عيب خلقي في القلب دون تحديد طبيعته. ولكنه في كل الأحوال يرتبط بزيادة في حجم القلب وبطينيه.
نادرًا ما يتم تشخيص متلازمة الوذمة في التليف المرن عند الأطفال، ولكن يعاني العديد من الأطفال من تضخم الكبد، والذي يبدأ في البروز بمعدل 3 سم من تحت حافة القوس الضلعي.
إذا كان التليف المرن مكتسبًا (على سبيل المثال، نتيجة لأمراض التهابية في أغشية القلب)، فإن الصورة السريرية غالبًا ما تكون بطيئة التطور. قد تختفي الأعراض تمامًا لبعض الوقت، ثم تظهر علامات خفيفة على ضعف وظائف القلب، مثل ضيق التنفس أثناء المجهود البدني، وزيادة معدل ضربات القلب، والتعب السريع، وانخفاض القدرة على التحمل البدني. بعد ذلك بقليل، يبدأ الكبد بالتضخم، ويظهر الوذمة والدوار.
جميع أعراض داء الليفية المرنة المكتسبة غير محددة، مما يُعقّد تشخيص المرض، إذ يُشبه اعتلال عضلة القلب وأمراض الكبد والكلى. يُشخّص المرض غالبًا في مرحلة قصور القلب الحاد، مما يؤثر سلبًا على نتائج العلاج.
المضاعفات والنتائج
تجدر الإشارة إلى أن تليف القلب والرئتين مرض خطير، ويعتمد مساره على ظروف مختلفة. تُعقّد عيوب القلب الخلقية الحالة بشكل كبير، والتي يمكن علاجها جراحيًا في سن مبكرة، ولكن في الوقت نفسه، يبقى خطر الوفاة مرتفعًا نسبيًا (حوالي 10%).
يُعتقد أنه كلما تطور المرض مبكرًا، زادت خطورة عواقبه. ويؤكد ذلك أن التليف المرن الخلقي في معظم الحالات يكون مساره سريعًا أو حادًا مع تطور سريع لقصور القلب. ويُعتبر ظهور قصور القلب الحاد لدى طفل دون سن 6 أشهر علامة تنبؤية سيئة.
مع ذلك، لا يضمن العلاج استعادة وظائف القلب بشكل كامل، بل يُبطئ فقط من تفاقم أعراض قصور القلب. من ناحية أخرى، يؤدي غياب هذا العلاج الداعم إلى الوفاة خلال أول عامين من حياة الطفل.
إذا اكتُشف قصور القلب في الأيام والأشهر الأولى من حياة الطفل، فمن المرجح ألا ينجو ولو لأسبوع واحد. تختلف الاستجابة للعلاج من طفل لآخر. في غياب أي تأثير علاجي، يكاد يكون الأمل معدومًا. ولكن مع المساعدة المُقدمة، يبقى متوسط العمر المتوقع للطفل المريض قصيرًا (من عدة أشهر إلى عدة سنوات).
عادةً ما تُحسّن جراحة وتصحيح عيوب القلب الخلقية المُسبّبة لتضخم البطين الأيسر الليفي حالة المريض. مع نجاح العلاج الجراحي لتضخم البطين الأيسر والالتزام بتعليمات الطبيب، قد يتطور المرض بشكل حميد: إذ يصبح قصور القلب مزمنًا دون أي علامات تطور. مع أن الأمل في تحقيق هذه النتيجة ضئيل.
أما الشكل المكتسب من تليف القلب المرن، فيصبح مزمنًا بسرعة ويتطور تدريجيًا. قد يُبطئ العلاج الدوائي العملية، لكنه لا يُوقفها.
يبدأ تليف الرئة المرن، بغض النظر عن وقت ظهور التغيرات في أنسجة وأغشية العضو بعد فترة الضوء، بالتطور بسرعة، ويؤدي إلى وفاة الشخص في غضون عامين، مسببًا فشلًا تنفسيًا حادًا. والمؤسف أنه لم يتم تطوير طرق فعالة لعلاج هذا المرض حتى الآن. [ 7 ]
التشخيص داء الأرومة الليفية
تليف عضلة القلب الليفي، الذي تُكتشف أعراضه في أغلب الحالات في سن مبكرة، هو مرض خلقي. إذا استثنينا الحالات النادرة التي بدأ فيها المرض بالتطور في أواخر الطفولة والبلوغ كمضاعفات للإصابات والأمراض الجسدية، يُمكن تشخيص المرض في فترة ما قبل الولادة، أي قبل ولادة الطفل.
يعتقد الأطباء أنه يمكن تحديد التغيرات المرضية في أنسجة الشغاف، وتغيرات شكل قلب الجنين، وبعض خصائصه الوظيفية المميزة لمرض التليف المرن، في وقت مبكر يصل إلى الأسبوع الرابع عشر من الحمل. إلا أن هذه الفترة لا تزال قصيرة نسبيًا، ولا يُستبعد ظهور المرض في وقت لاحق، أقرب إلى الثلث الثالث من الحمل، وأحيانًا قبل الولادة بشهرين. لذلك، يُنصح بإجراء فحوصات بالموجات فوق الصوتية لقلب الجنين، عند مراقبة الحوامل، كل عدة أسابيع.
ما هي العلامات التي يمكن للأطباء من خلالها الاشتباه بالمرض خلال فحص الموجات فوق الصوتية التالي؟ يعتمد الكثير على شكل المرض. غالبًا ما يُشخَّص التليف المرن في منطقة البطين الأيسر، ولكن هذا الهيكل لا يكون متضخمًا دائمًا. يُحدَّد الشكل المتوسع للمرض مع تضخم البطين الأيسر للقلب بسهولة أثناء فحص الموجات فوق الصوتية من خلال الشكل الكروي للقلب، الذي يُمثِّل البطين الأيسر قمته، والزيادة العامة في حجم العضو، وبروز الحاجز بين البطينين نحو البطين الأيمن. لكن العلامة الرئيسية للتليف المرن هي سماكة الشغاف، وكذلك حواجز القلب مع زيادة مميزة في صدى هذه الهياكل، والتي يتم تحديدها من خلال فحص الموجات فوق الصوتية المحدد.
تُجرى الدراسة باستخدام أجهزة خاصة بالموجات فوق الصوتية مزودة ببرامج متخصصة في أمراض القلب. لا يُسبب تخطيط صدى قلب الجنين أي ضرر للأم أو للجنين، بل يُتيح تحديد التغيرات التشريحية في القلب، بالإضافة إلى تحديد حالة الأوعية التاجية، ووجود جلطات دموية فيها، وتغيرات في سمك أغشية القلب.
يتم وصف تخطيط صدى القلب للجنين ليس فقط في حالة وجود انحرافات أثناء فك تشفير نتائج الموجات فوق الصوتية، ولكن أيضًا في حالة إصابة الأم بالعدوى (وخاصة الفيروسية)، وتناول الأدوية القوية، والاستعداد الوراثي، ووجود اضطرابات التمثيل الغذائي، وكذلك أمراض القلب الخلقية عند الأطفال الأكبر سنًا.
يمكن لتخطيط صدى القلب للجنين أيضًا الكشف عن أشكال خلقية أخرى من التليف المرن. على سبيل المثال، التليف المرن في البطين الأيمن، وهي عملية واسعة الانتشار تُلحق الضرر بالبطين الأيسر والهياكل المجاورة له في آن واحد: البطين الأيمن، وصمامات القلب، والأذينين، والأشكال المركبة من التليف المرن، والتليف المرن الشغافي لعضلة القلب مع سماكة في البطانة الداخلية للبطينين وإصابة جزء من عضلة القلب في العملية المرضية (عادةً ما يترافق مع تخثر في الجدار).
إن تشخيص تليف بطانة القلب في مرحلة ما قبل الولادة يكون سيئًا للغاية، لذا ينصح الأطباء بإنهاء الحمل في هذه الحالة. يُستبعد احتمال التشخيص الخاطئ بإجراء فحص متكرر بالموجات فوق الصوتية لقلب الجنين، والذي يُجرى بعد أربعة أسابيع من الفحص الأول الذي كشف عن المرض. من الواضح أن القرار النهائي بإنهاء الحمل أو استمراره يعود للوالدين، ولكن يجب أن يدركا نوع الحياة التي يُحكمان على الطفل بها.
لا يُكتشف تليف بطانة القلب دائمًا أثناء الحمل، خاصةً مع عدم تسجيل جميع الحوامل في عيادة صحة المرأة والخضوع للتشخيص الوقائي بالموجات فوق الصوتية. لا يؤثر مرض الجنين في الرحم تقريبًا على حالة الحامل، لذا غالبًا ما تُصبح ولادة طفل مريض مفاجأة غير سارة.
في بعض الحالات، يعلم كلٌّ من الوالدين والأطباء بمرض الطفل بعد عدة أشهر من ولادته. في هذه الحالة، قد لا تُظهر فحوصات الدم المخبرية أي شيء، باستثناء زيادة تركيز الصوديوم (فرط صوديوم الدم). لكن نتائجها تُفيد في إجراء التشخيص التفريقي لاستبعاد الأمراض الالتهابية.
لا يزال هناك أمل في التشخيص الآلي. تخطيط القلب الكهربائي (ECG) ليس مؤشرًا دقيقًا في حالة التليف المرن. يساعد على تحديد اضطرابات القلب والتوصيل الكهربائي لعضلة القلب، ولكنه لا يحدد أسباب هذه الاضطرابات. وبالتالي، فإن أي تغير في جهد تخطيط القلب (عادةً ما يكون أقل من قيمته الحقيقية في سن مبكرة، وعلى العكس، يكون مرتفعًا بشكل مفرط في سن متقدمة) يشير إلى اعتلال عضلة القلب، والذي قد يرتبط ليس فقط بأمراض القلب، بل أيضًا باضطرابات التمثيل الغذائي. يُعد تسرع القلب أحد أعراض أمراض القلب. وإذا تأثر كلا البطينين، فقد يبدو تخطيط القلب طبيعيًا بشكل عام. [ 8 ]
التصوير المقطعي المحوسب (CT) هو أداة غير جراحية ممتازة للكشف عن تكلس القلب والأوعية الدموية واستبعاد التهاب التامور. [ 9 ]
قد يكون التصوير بالرنين المغناطيسي مفيدًا في الكشف عن التليف المرن لأن الخزعة غازية. يشير وجود حافة منخفضة الكثافة في تسلسل تروية عضلة القلب وحافة شديدة الكثافة في تسلسل التعزيز المتأخر إلى التليف المرن.[ 10 ]
ولكن هذا لا يعني أن نتخلى عن الدراسة، لأنها تساعد على تحديد طبيعة عمل القلب ودرجة تطور قصور القلب.
عند ظهور أعراض قصور القلب واستشارة المريض للطبيب، يُوصف له أيضًا: تصوير الصدر بالأشعة السينية، أو التصوير المقطعي المحوسب أو التصوير بالرنين المغناطيسي للقلب، أو تخطيط صدى القلب (EchoCG). في الحالات المشكوك فيها، يُلجأ إلى خزعة من أنسجة القلب، ثم فحص نسيجي. يُعد التشخيص خطيرًا للغاية، لذا يتطلب اتباع نفس النهج في التشخيص، مع أن العلاج لا يختلف كثيرًا عن العلاج العرضي لأمراض القلب التاجية وقصور القلب.
لكن حتى هذا الفحص الدقيق لن يكون مفيدًا إذا لم تُستخدم نتائجه في التشخيص التفريقي. يمكن استخدام نتائج تخطيط كهربية القلب للتمييز بين التليف المرن الحاد والتهاب عضلة القلب مجهول السبب، والتهاب التامور النضحي، وتضيق الأبهر. في الوقت نفسه، لن تُظهر الفحوصات المخبرية علامات التهاب (مثل زيادة عدد كريات الدم البيضاء، وزيادة معدل ترسيب كريات الدم الحمراء، إلخ)، ولن تُظهر قياسات درجة الحرارة ارتفاعًا في درجة الحرارة.
يساعد تحليل أصوات القلب والنفخات، والتغيرات في حجم الأذينين، ودراسة التاريخ المرضي على التمييز بين التليف المرن الشغافي وقصور الصمام التاجي المعزول وعيوب الصمام التاجي.
يُفيد تحليل البيانات السيكولوجية في التمييز بين التليف المرن وضيق القلب والأبهر. في حالة تضيق الأبهر، يُنصح أيضًا بالاهتمام بالحفاظ على نظم الجيوب الأنفية وغياب الانسداد الخثاري. لا تُلاحظ اضطرابات نظم القلب وترسب الخثرات في التهاب التامور النضحي أيضًا، ولكن يتجلى المرض بارتفاع في درجة الحرارة والحمى.
تكمن الصعوبة الأكبر في التمييز بين التليف المرن الشغافي واعتلال عضلة القلب الاحتقاني. في هذه الحالة، يكون التليف المرن، على الرغم من أنه لا يصاحبه في معظم الحالات اضطرابات توصيل قلبية واضحة، أقل فعالية في العلاج.
في حالة وجود أمراض مشتركة، من الضروري الانتباه لأي انحرافات تُكتشف أثناء تصوير القلب بالأشعة المقطعية أو بالموجات فوق الصوتية، لأن العيوب الخلقية تُعقّد مسار التليف المرن بشكل كبير. إذا تم اكتشاف التليف المرن الشغافي المشترك في فترة ما داخل الرحم، فمن غير المناسب الحفاظ على الحمل، ومن الأفضل إنهاؤه.
تشخيص التليف المرن الرئوي
يتطلب تشخيص التليف الرئوي المرن معرفة ومهارات معينة من الطبيب. والحقيقة أن أعراض المرض متباينة للغاية. فمن جهة، تشير إلى أمراض الرئة الاحتقانية (سعال غير مصحوب ببلغم، ضيق في التنفس)، ومن جهة أخرى، قد تكون أيضًا مظهرًا من مظاهر أمراض القلب. لذلك، لا يقتصر تشخيص المرض على ذكر الأعراض والفحص السمعي فقط.
تساعد فحوصات دم المريض على استبعاد أمراض الرئة الالتهابية، ولكنها لا تقدم معلومات عن التغيرات الكمية والنوعية في الأنسجة. يساعد وجود علامات كثرة الحمضات على التمييز بين المرض والتليف الرئوي، الذي يتشابه في أعراضه، ولكنه لا ينفي أو يؤكد وجود التليف المرن.
وتعتبر الدراسات الآلية أكثر دلالة: تصوير الصدر بالأشعة السينية والفحص المقطعي لأعضاء الجهاز التنفسي، وكذلك التحليلات الوظيفية، والتي تتكون من تحديد أحجام الجهاز التنفسي، والقدرة الحيوية للرئتين، والضغط في العضو.
في حالة تليف الرئة المرن، يجدر الانتباه إلى انخفاض وظيفة التنفس الخارجي، والذي يُقاس بقياس التنفس. يؤثر انخفاض التجاويف السنخية النشطة بشكل كبير على السعة الحيوية للرئتين (VCL)، كما يؤثر سماكة جدران الهياكل الداخلية على سعة انتشار العضو (DCL)، مما يضمن وظائف التهوية وتبادل الغازات (بمعنى آخر، امتصاص ثاني أكسيد الكربون من الدم وإطلاق الأكسجين).
العلامات المميزة لتليف النسيج الجنبي هي مزيج من تدفق الهواء المحدود إلى الرئتين (الانسداد) وضعف توسع الرئة أثناء الاستنشاق (التقييد)، وتدهور وظيفة الجهاز التنفسي الخارجي، وارتفاع ضغط الدم الرئوي المعتدل (زيادة الضغط في الرئتين)، والتي يتم تشخيصها في نصف المرضى.
تُظهر خزعة أنسجة الرئة تغيرات مميزة في البنية الداخلية للعضو. وتشمل هذه التغيرات: تليف غشاء الجنب والنسيج الحشوي، مصحوبًا بتمدد جدران الحويصلات الهوائية، وتراكم الخلايا الليمفاوية في منطقة الحواجز السنخية المضغوطة، وتحوّل الخلايا الليفية إلى نسيج عضلي غير طبيعي، ووجود سائل وذمي.
يُظهر التصوير المقطعي تلفًا في الرئتين في الأقسام العلوية على شكل بؤر انضغاط جنبي وتغيرات هيكلية في النسيج الحشوي. يُشبه النسيج الضام المتضخم في الرئتين النسيج العضلي في اللون والخصائص، إلا أن حجم الرئتين يتناقص. توجد تجاويف هوائية كبيرة (أكياس) في النسيج الحشوي. من السمات المميزة توسع بؤري (أو منتشر) غير رجعي في القصيبات الهوائية والقصيبات الهوائية (توسع القصبات الهوائية بالشد) وانخفاض موضع قبة الحجاب الحاجز.
تكشف الفحوصات الإشعاعية عن وجود مناطق "زجاجية" و"رئة قرص العسل" لدى العديد من المرضى، مما يشير إلى عدم انتظام تهوية الرئتين نتيجة وجود بؤر ضغط الأنسجة. يعاني حوالي نصف المرضى من تضخم في الغدد الليمفاوية والكبد.
يجب التمييز بين التليف المرن الرئوي والتليف الناجم عن العدوى الطفيلية وزيادة الحمضات المصاحبة لها، والتليف المرن الشغافي، وأمراض الرئة مع ضعف التهوية وصورة "رئة قرص العسل"، ومرض التهاب النسيج الخلوي X المناعي الذاتي (أحد أشكال هذا المرض مع تلف الرئة يسمى مرض هاند شولر كريستيان)، ومظاهر الساركويد والسل الرئوي.
علاج او معاملة داء الأرومة الليفية
يُعتبر داء الليفية المرنة، أينما وُجد، مرضًا خطيرًا وغير قابل للشفاء تقريبًا. لا يُمكن استعادة التغيرات المرضية في غشاء الجنب والنسيج الرئوي بالأدوية. حتى استخدام الأدوية الهرمونية المضادة للالتهابات (الكورتيكوستيرويدات) مع موسعات الشعب الهوائية لا يُعطي النتيجة المرجوة. تُساعد موسعات الشعب الهوائية على تخفيف حالة المريض قليلًا، وتخفيف متلازمة الانسداد، لكنها لا تؤثر على العمليات التي تحدث في الرئتين، لذا يُمكن استخدامها كعلاج داعم فقط.
العلاج الجراحي لمرض التليف الرئوي المرن غير فعال أيضًا. العملية الوحيدة التي يمكن أن تُغير الوضع هي زراعة الأعضاء من متبرع. لكن للأسف، فإن زراعة الرئة لها نفس التشخيص غير المواتي. [ 11 ]
وفقًا لعلماء أجانب، يُعدّ التليف المرن أيضًا أحد المضاعفات الشائعة لزراعة الخلايا الجذعية من الرئة أو نخاع العظم. في كلتا الحالتين، تحدث تغيرات في ألياف النسيج الضام للرئتين، مما يؤثر على وظيفة التنفس الخارجي.
يتطور المرض دون علاج (ولا يوجد علاج فعال حاليًا)، ويموت حوالي 40% من المرضى بسبب فشل الجهاز التنفسي في غضون عام ونصف إلى عامين. كما أن متوسط العمر المتوقع لمن يبقون في المستشفى محدود للغاية (حتى 10-20 عامًا)، وكذلك قدرتهم على العمل. ويصبح الشخص معاقًا.
يُعتبر تليف القلب المرن مرضًا غير قابل للشفاء طبيًا، خاصةً إذا كان عيبًا خلقيًا. عادةً، لا يعيش الأطفال حتى سن الثانية. لا يمكن إنقاذهم إلا من خلال عملية زرع قلب، وهي في حد ذاتها عملية صعبة ذات درجة عالية من المخاطر وعواقب غير متوقعة، خاصةً في هذه السن المبكرة.
لدى بعض الأطفال، يُمكن تصحيح عيوب القلب الخلقية جراحيًا لتجنب تفاقم حالة الطفل المريض. في حالة تضيق الشريان، يُركَّب مُوسِّع وعائي - تحويلة (مجازة الشريان الأبهر التاجي). في حالة تمدد البطين الأيسر للقلب، يُعاد شكله بسرعة. لكن حتى هذه العملية لا تضمن بقاء الطفل دون زراعة قلب. ينجو حوالي 20-25% من الأطفال، ويعانون من قصور القلب طوال حياتهم، أي أنهم لا يُعتبرون أصحاء.
إذا كان المرض مكتسبًا، فمن الجدير النضال من أجل حياة الطفل بمساعدة الأدوية. ولكن من المهم أن نفهم أنه كلما ظهر المرض مبكرًا، زادت صعوبة مكافحته.
يهدف العلاج الدوائي إلى مكافحة تفاقم قصور القلب والوقاية منه. تُوصف للمرضى الأدوية القلبية التالية:
- مثبطات الإنزيم المحول للأنجيوتنسين (ACE)، والتي تؤثر على ضغط الدم وتحافظ عليه ضمن الحدود الطبيعية (كابتوبريل، إينالابريل، بينازيبريل، إلخ.)،
- حاصرات بيتا المستخدمة لعلاج اضطرابات نظم القلب وارتفاع ضغط الدم ومنع احتشاء عضلة القلب (أنابريلين، بيسوبرولول، ميتوبرولول)،
- جليكوسيدات القلب، والتي عند استخدامها لفترة طويلة من الزمن، لا تدعم فقط عمل القلب (زيادة محتوى البوتاسيوم في الخلايا العضلية القلبية وتحسين توصيل عضلة القلب)، ولكنها قادرة أيضًا على تقليل درجة سماكة الشغاف إلى حد ما (ديجوكسين، جيتوكسين، ستروفانثين)،
- مدرات البول الموفرة للبوتاسيوم (سبيرونولاكتون، فيروشبيرون، ديكريز)، تمنع الوذمة النسيجية،
- العلاج المضاد للتخثر بمضادات التخثر (كارديوماجنيل، ماجنيكور)، والذي يمنع تكوين جلطات الدم واضطرابات الدورة الدموية في الأوعية التاجية.
في الشكل الخلقي من التليف المرن الشغافي، لا يعزز العلاج الداعم التعافي، ولكنه يقلل من خطر الوفاة بسبب قصور القلب أو الانصمام الخثاري بنسبة 70-75%. [ 12 ]
الأدوية
كما نرى، لا يختلف علاج تليف الشغاف القلبي عمليًا عن علاج قصور القلب. في كلتا الحالتين، يأخذ أطباء القلب في الاعتبار شدة اعتلال القلب. ويعتمد وصف الأدوية على حالة المريض، مع مراعاة عمر المريض، والأمراض المصاحبة، ونوع ودرجة قصور القلب.
في علاج تليف الشغاف المكتسب، تُستخدم أدوية من خمس مجموعات. لنأخذ دواءً واحدًا من كل مجموعة.
"إينالابريل" دواء من مجموعة مثبطات الإنزيم المحول للأنجيوتنسين، يُنتج على شكل أقراص بجرعات مختلفة. يزيد هذا الدواء من تدفق الدم التاجي، ويُوسّع الشرايين، ويُخفّض ضغط الدم دون التأثير على الدورة الدموية الدماغية، ويُبطئ ويُقلّل من توسّع البطين الأيسر للقلب. يُحسّن الدواء تدفق الدم إلى عضلة القلب، مُخفّفًا آثار نقص التروية، ويُخفّف تخثر الدم بشكل طفيف، ويمنع تكوّن الجلطات الدموية، وله تأثير مُدرّ للبول طفيف.
في حالة قصور القلب، يُوصف الدواء لفترة تزيد عن ستة أشهر أو بشكل دائم. يبدأ الدواء بجرعة دنيا (2.5 ملغ)، ثم تزداد تدريجيًا بمقدار 2.5-5 ملغ كل 3-4 أيام. الجرعة الدائمة هي التي يتحملها المريض جيدًا وتحافظ على ضغط الدم ضمن المعدل الطبيعي.
الجرعة اليومية القصوى هي ٤٠ ملغ. يمكن تناولها مرة واحدة أو تقسيمها على جرعتين.
إذا انخفض ضغط الدم عن المعدل الطبيعي، تُخفَّض الجرعة تدريجيًا. لا ينبغي إيقاف العلاج بإينالابريل فجأةً. يُنصح بتناول جرعة صيانة مقدارها 5 ملغ يوميًا.
هذا الدواء مخصص لعلاج المرضى البالغين، ويمكن وصفه أيضًا للأطفال (لم تُثبت سلامته رسميًا، ولكن في حالة التليف المرن، تكون حياة المريض الصغير على المحك، لذا تُؤخذ نسبة المخاطرة في الاعتبار). لا يُوصف مثبط الإنزيم المحول للأنجيوتنسين للمرضى الذين يعانون من عدم تحمل مكونات الدواء، أو المصابين بالبورفيريا، أو أثناء الحمل، أو الرضاعة الطبيعية. يُمنع استخدام إينالابريل إذا كان المريض قد أصيب سابقًا بوذمة كوينك أثناء تناول أي من أدوية هذه المجموعة.
يجب توخي الحذر عند وصف الدواء للمرضى الذين يعانون من أمراض مصاحبة: أمراض الكلى والكبد الشديدة، فرط بوتاسيوم الدم، فرط الألدوستيرونية، تضيق الصمام الأبهري أو التاجي، أمراض النسيج الضام الجهازية، نقص تروية القلب، أمراض الدماغ، داء السكري.
عند العلاج بهذا الدواء، يُنصح بتجنب استخدام مدرات البول التقليدية لتجنب الجفاف وتأثير خافض قوي لضغط الدم. يتطلب الاستخدام المتزامن مع مدرات البول الموفرة للبوتاسيوم تعديل الجرعة، نظرًا لارتفاع خطر الإصابة بفرط بوتاسيوم الدم، والذي بدوره يُسبب عدم انتظام ضربات القلب، والنوبات، وانخفاض قوة العضلات، وزيادة الضعف، وما إلى ذلك.
عادةً ما يكون دواء "إينالابريل" جيد التحمل، ولكن قد يعاني بعض المرضى من آثار جانبية. أكثرها شيوعًا: انخفاض حاد في ضغط الدم يصل إلى الانهيار، صداع ودوار، اضطرابات في النوم، زيادة التعب، فقدان التوازن والسمع والبصر بشكل قابل للعكس، طنين في الأذن، ضيق في التنفس، سعال بدون بلغم، تغيرات في تركيبة الدم والبول، والتي عادةً ما تشير إلى خلل في وظائف الكبد والكلى. من الآثار الجانبية المحتملة: تساقط الشعر، انخفاض الرغبة الجنسية، أعراض "الهبات الساخنة" (الشعور بحرارة وخفقان، احتقان في جلد الوجه، إلخ).
"بيسوبرولول" هو حاصر بيتا ذو تأثير انتقائي، وله تأثيرات خافضة لضغط الدم ومضادة لنقص التروية، ويساعد في مكافحة أعراض تسرع القلب وعدم انتظام ضرباته. وهو دواء اقتصادي على شكل أقراص، يمنع تطور قصور القلب في حالة تليف بطانة القلب. [ 13 ]
كما هو الحال مع العديد من الأدوية الأخرى الموصوفة لأمراض القلب التاجية وقصور القلب الاحتقاني، يُوصف بيسوبرولول لفترة طويلة. يُنصح بتناوله صباحًا قبل أو أثناء الوجبات.
أما الجرعات الموصى بها، فتُختار بشكل فردي بناءً على قراءات ضغط الدم والأدوية الموصوفة بالتوازي مع هذا الدواء. في المتوسط، تتراوح الجرعة الواحدة (واليومية أيضًا) بين 5 و10 ملغ، ولكن مع ارتفاع طفيف في الضغط، يمكن خفضها إلى 2.5 ملغ. أما الجرعة القصوى التي يمكن وصفها لمريض ذي كلى سليمة فهي 20 ملغ، ولكن فقط مع ارتفاع ضغط الدم المستمر.
لا يمكن زيادة الجرعات المحددة إلا بإذن الطبيب. أما في حالات أمراض الكبد والكلى الشديدة، فتُعتبر 10 ملغ الجرعة القصوى المسموح بها.
في العلاج المعقد لقصور القلب الناتج عن خلل في وظيفة البطين الأيسر، والذي غالبًا ما يحدث مع التليف المرن، تُختار الجرعة الفعالة بزيادة الجرعة تدريجيًا بمقدار 1.25 ملغ. في هذه الحالة، يُبدأ بأقل جرعة ممكنة (1.25 ملغ)، ثم تُزاد الجرعة على فترات أسبوع واحد.
عند وصول الجرعة إلى 5 ملغ، تُزاد الفترة إلى 28 يومًا. بعد 4 أسابيع، تُزاد الجرعة بمقدار 2.5 ملغ. بالالتزام بهذه الفترة وهذا المعدل، تصل الجرعة إلى 10 ملغ، والتي سيضطر المريض إلى تناولها لفترة طويلة أو بشكل مستمر.
إذا كانت هذه الجرعة غير مُتَحَمَّلة، تُخفَّض تدريجيًا إلى مستوى مُريح. كما يجب عدم إيقاف العلاج بحاصرات بيتا فجأةً.
لا ينبغي وصف الدواء في حالة فرط الحساسية للمواد الفعالة والمساعدة في الدواء، قصور القلب الحاد والمتعاوض، الصدمة القلبية، كتلة الأذيني البطيني من الدرجة 2-3، بطء القلب، انخفاض ضغط الدم باستمرار وبعض أمراض القلب الأخرى، الربو القصبي الشديد، انسداد الشعب الهوائية، اضطرابات الدورة الدموية الطرفية الشديدة، الحماض الأيضي.
يجب توخي الحذر عند وصف العلاجات المعقدة. لذلك، لا يُنصح بدمج بيسوبرولول مع بعض الأدوية المضادة لاضطراب النظم (مثل الكينيدين، الليدوكايين، الفينيتوين، إلخ)، ومضادات الكالسيوم، وأدوية خفض ضغط الدم المركزي.
الأعراض والاضطرابات المزعجة المحتملة أثناء العلاج ببيسوبرولول: زيادة التعب، والصداع، والهبات الساخنة، واضطرابات النوم، وانخفاض ضغط الدم، والدوار عند النهوض من السرير، وفقدان السمع، وأعراض الجهاز الهضمي، واضطرابات الكبد والكلى، وانخفاض القدرة الجنسية، وضعف العضلات، وتشنجات. يشكو المرضى أحيانًا من اضطرابات الدورة الدموية الطرفية، والتي تتجلى في انخفاض درجة الحرارة أو تنميل الأطراف، وخاصةً أصابع اليدين والقدمين.
في حالة وجود أمراض مصاحبة في الجهاز القصبي الرئوي والكلى والكبد ومرض السكري، فإن خطر الآثار الجانبية يكون أعلى، مما يشير إلى تفاقم المرض.
"ديجوكسين" جليكوسيد قلبي شائع ورخيص الثمن، مستخلص من نبات قفاز الثعلب، ويُصرف بوصفة طبية فقط (على شكل أقراص) ويجب استخدامه تحت إشراف طبي. يُجرى العلاج بالحقن في المستشفى خلال تفاقم مرض القلب التاجي وقصور القلب الاحتقاني، وتُوصف الأقراص باستمرار بجرعات ضئيلة الفعالية، نظرًا لتأثيره السام والمخدر.
يتمثل التأثير العلاجي في تغيير قوة وسعة انقباضات عضلة القلب (مما يمنح القلب الطاقة، ويدعمه في حالات نقص التروية). كما أن للدواء تأثيرًا موسّعًا للأوعية الدموية (مُخفّفًا للاحتقان) ومُدرًا للبول، مما يُساعد على تخفيف التورم وتقليل شدة فشل الجهاز التنفسي، الذي يُتمثّل في ضيق التنفس.
إن خطورة الديجوكسين وغيره من الجليكوسيدات القلبية تكمن في أنه في حالة تناول جرعة زائدة منها، فإنها قد تؤدي إلى حدوث عدم انتظام في ضربات القلب بسبب زيادة استثارة عضلة القلب.
في حالة تفاقم قصور القلب الاحتقاني، يُوصف الدواء على شكل حقن، وتُختار الجرعة المناسبة لكل حالة على حدة، مع مراعاة شدة الحالة وعمر المريض. عند استقرار الحالة، يُستبدل الدواء بالأقراص.
عادةً، الجرعة القياسية المفردة من الدواء هي 0.25 ملغ. يمكن أن يتراوح تواتر الإعطاء من مرة إلى خمس مرات يوميًا على فترات متساوية. في المرحلة الحادة من قصور القلب الاحتقاني، يمكن أن تصل الجرعة اليومية إلى 1.25 ملغ. عندما تستقر الحالة بشكل دائم، يلزم تناول جرعة صيانة مقدارها 0.25 ملغ (أو أقل في كثير من الأحيان 0.5 ملغ) يوميًا.
عند وصف الدواء للأطفال، يُؤخذ وزن المريض في الاعتبار. تُحسب الجرعة الفعالة والآمنة بواقع 0.05-0.08 ملغ لكل كيلوغرام من وزن الجسم. ولكن لا يُوصف الدواء باستمرار، بل لمدة تتراوح بين يوم وسبعة أيام.
يجب أن يصف الطبيب جرعة جليكوسيد القلب، مع مراعاة حالة المريض وعمره. في الوقت نفسه، يُعدّ تعديل الجرعات بشكل مستقل أو تناول دواءين لهما هذا التأثير في آن واحد أمرًا بالغ الخطورة.
لا يُوصف "ديجوكسين" لعلاج الذبحة الصدرية غير المستقرة، واضطرابات نظم القلب الشديدة، وحصار القلب الأذيني البطيني من الدرجة 2-3، وانسداد القلب، ومتلازمة آدامز-ستوكس-مورغاني، وتضيق الصمام ثنائي الشرفات المعزول وتضيق الأبهر، والتشوهات الخلقية في القلب، ومتلازمة وولف-باركنسون-وايت، واعتلال عضلة القلب الانسدادي الضخامي، والتهاب بطانة القلب، والتهاب عضلة القلب المحيطي، وتمدد الأوعية الدموية الأبهرية الصدرية، وفرط كالسيوم الدم، ونقص بوتاسيوم الدم، وبعض الأمراض الأخرى. قائمة موانع الاستعمال طويلة جدًا وتشمل متلازمات متعددة الأعراض، لذا لا يمكن اتخاذ قرار استخدام هذا الدواء إلا من قِبل طبيب مختص.
للديجوكسين أيضًا آثار جانبية. تشمل هذه الآثار اضطرابات في نظم القلب (نتيجةً لاختيار جرعة خاطئة أو تناول جرعة زائدة)، وفقدان الشهية، والغثيان (غالبًا مع القيء)، واضطرابات في الأمعاء، وضعفًا شديدًا وإرهاقًا شديدًا، وصداعًا، وظهور "ذباب" أمام العينين، وانخفاضًا في مستوى الصفائح الدموية، واضطرابات تخثر الدم، وردود فعل تحسسية. غالبًا ما يرتبط ظهور هذه الأعراض وغيرها بتناول جرعات كبيرة من الدواء، ونادرًا ما يرتبط بالعلاج طويل الأمد.
"سبيرونولاكتون" مضادٌّ للكورتيكويدات المعدنية. له تأثيرٌ مُدِرٌّ للبول، إذ يُعزز إخراج الصوديوم والكلور والماء، مع احتباس البوتاسيوم، الضروري لوظائف القلب الطبيعية، إذ تعتمد وظيفته التوصيلية بشكلٍ رئيسي على هذا العنصر. يُساعد على تخفيف الوذمة، ويُستخدم كعلاجٍ مُساعد في حالات قصور القلب الاحتقاني.
في حالة قصور القلب الاحتقاني، يُوصف الدواء حسب مرحلة المرض. في حالة تفاقم الحالة، يُمكن وصف الدواء على شكل حقن وأقراص بجرعة تتراوح بين 50 و100 ملغ يوميًا. عند استقرار الحالة، تُوصف جرعة صيانة تتراوح بين 25 و50 ملغ لفترة طويلة. في حال اختلال توازن البوتاسيوم والصوديوم، مما يؤدي إلى انخفاض في الأول، يُمكن زيادة الجرعة حتى يصل تركيز العناصر النزرة إلى المستوى الطبيعي.
في طب الأطفال، يتم حساب الجرعة الفعالة على أساس نسبة 1-3 ملغ من سبيرونولاكتون لكل كيلوغرام من وزن جسم المريض.
وكما نرى، هنا أيضًا، فإن اختيار الجرعة الموصى بها هو أمر فردي، كما هو الحال مع وصف العديد من الأدوية الأخرى المستخدمة في أمراض القلب.
من موانع استخدام مُدرّات البول: زيادة البوتاسيوم أو انخفاض مستويات الصوديوم في الجسم، أو انقطاع التبول (انقطاع البول)، أو أمراض الكلى الحادة المصحوبة بضعف في الأداء. لا يُوصف هذا الدواء للحوامل والمرضعات، وكذلك لمن يعانون من عدم تحمل مكوناته.
يجب توخي الحذر عند استخدام الدواء في المرضى الذين يعانون من كتلة القلب الأذيني البطيني (قد تتفاقم)، وزيادة الكالسيوم (فرط كالسيوم الدم)، والحماض الأيضي، ومرض السكري، وعدم انتظام الدورة الشهرية، وأمراض الكبد.
قد يُسبب تناول الدواء صداعًا، ونعاسًا، وفقدانًا للتوازن وتنسيق الحركات (ترنح)، وتضخمًا في الغدد الثديية لدى الرجال (تثديًا)، وعجزًا جنسيًا، وتغيرات في طبيعة الدورة الشهرية، وخشونة في الصوت، ونموًا مفرطًا للشعر لدى النساء (كثرة الشعر)، وألمًا في المنطقة فوق المعدة، واضطرابات في الجهاز الهضمي، ومغصًا معويًا، وخللًا في وظائف الكلى، واختلالًا في توازن المعادن. كما يُحتمل حدوث ردود فعل جلدية وحساسية.
عادةً ما تُلاحظ الآثار الجانبية عند تجاوز الجرعة المطلوبة. قد يحدث وذمة عند عدم كفاية الجرعة.
"ماجنيكور" دواءٌ يمنع تكوّن جلطات الدم، ويعتمد على حمض أسيتيل الساليسيليك وهيدروكسيد المغنيسيوم. يُعدّ من العلاجات الفعّالة المضادة للتخثر الموصوفة لقصور القلب. له تأثيرٌ مسكنٌ للألم، ومضادٌ للالتهابات، ومضادٌ للصفيحات، ويؤثر على وظيفة الجهاز التنفسي. يُخفّف هيدروكسيد المغنيسيوم من التأثير السلبي لحمض أسيتيل الساليسيليك على الغشاء المخاطي في الجهاز الهضمي.
في حالة تليف عضلة القلب الليفي، يُوصف الدواء وقائيًا، لذا يُلتزم بالجرعة الفعالة الدنيا وهي 75 ملغ، أي ما يعادل قرصًا واحدًا. في حالة نقص تروية القلب الناتج عن تكوّن خثرة وما يليه من تضيّق في تجويف الأوعية التاجية، تكون الجرعة الأولية قرصين، وجرعة المداومة تعادل الجرعة الوقائية.
إن تجاوز الجرعة الموصى بها يزيد بشكل كبير من خطر النزيف الذي يصعب إيقافه.
يتم وصف الجرعات للمرضى البالغين نظرًا لحقيقة أن الدواء يحتوي على حمض أسيتيل الساليسيليك، والذي قد يؤدي استخدامه في سن أقل من 15 عامًا إلى عواقب وخيمة.
لا يوصف الدواء للمرضى في مرحلة الطفولة والمراهقة المبكرة، في حالة عدم تحمل حمض أسيتيل الساليسيليك والمكونات الأخرى للدواء، الربو "الأسبرين" (في التاريخ)، التهاب المعدة التآكلي الحاد، قرحة هضمية، أهبة النزف، أمراض الكبد والكلى الشديدة، في حالة قصور القلب الشديد.
خلال فترة الحمل، يُوصف ماجنيكور فقط في حالات الضرورة القصوى، وفي الثلثين الأول والثاني من الحمل فقط، مع مراعاة الآثار السلبية المحتملة على الجنين ومسار الحمل. أما في الثلث الثالث من الحمل، فلا يُنصح بهذا العلاج، إذ يُسهم في تقليل انقباض الرحم (مخاض مُطوّل) وقد يُسبب نزيفًا حادًا. قد يُصاب الجنين بارتفاع ضغط الدم الرئوي وخلل في وظائف الكلى.
تشمل الآثار الجانبية للدواء أعراضًا في الجهاز الهضمي (عسر الهضم، وآلام في المنطقة الشرسوفية والبطن، مع احتمال حدوث نزيف معدي مع تطور فقر الدم الناجم عن نقص الحديد). ومن المحتمل حدوث نزيف في الأنف واللثة وأعضاء الجهاز البولي عند تناول الدواء.
قد تُسبب الجرعة الزائدة دوخة وإغماءً وطنينًا في الأذنين. ردود الفعل التحسسية شائعة، خاصةً في حالات فرط الحساسية للساليسيلات. مع ذلك، نادرًا ما يُلاحظ حدوث صدمة تأقية وفشل تنفسي.
ينبغي اختيار الأدوية في العلاج المركب والجرعات الموصى بها لكل حالة على حدة. ويجب توخي الحذر الشديد عند علاج الحوامل والمرضعات والأطفال وكبار السن.
الطب التقليدي والمعالجة المثلية
تليف القلب المرن مرض خطير وشديد، يتميز بمسار تقدمي مميز، وفرص شفاءه شبه معدومة. من الواضح أن العلاج الفعال لهذا المرض بالعلاجات الشعبية مستحيل. لا يمكن استخدام وصفات الطب التقليدي، التي تعتمد في معظمها على العلاج بالأعشاب، إلا كعلاج مساعد وبإذن الطبيب، لتجنب تعقيد التشخيص الضعيف أصلًا.
أما بالنسبة للمعالجات المثلية، فلا يُحظر استخدامها، ويمكن أن تكون جزءًا من علاج شامل لقصور القلب. ومع ذلك، في هذه الحالة، لا نتحدث عن العلاج بقدر ما نتحدث عن منع تطور قصور القلب الاحتقاني.
يجب أن يصف هذه الأدوية طبيب متخصص في الطب المثلي، ومسألة إمكانية إدراجها في العلاج المعقد تقع ضمن اختصاص الطبيب المعالج.
ما هي الأدوية المثلية التي تساعد في تأخير تطور قصور القلب في حالة التليف المرن؟ في حالات قصور القلب الحاد، يلجأ المعالجون المثليون إلى الأدوية التالية: الزرنيخ الألبوم، أنتيمونيوم طرطريكوم، كاربو فيجيتابيليس، حمض الأكساليكوم. على الرغم من تشابه دواعي الاستعمال، يعتمد الأطباء عند اختيار دواء فعال على المظاهر الخارجية لنقص التروية، مثل الزرقة (درجتها وانتشارها)، وطبيعة متلازمة الألم.
في حالة قصور القلب الاحتقاني، قد يتم تضمين ما يلي في العلاج الصيانة: Lachesis وNayu، Lycopus (في المراحل الأولية من تضخم القلب)، Laurocerasus (لضيق التنفس أثناء الراحة)، Latrodectus mactans (لأمراض الصمامات)، مستحضرات الزعرور (مفيدة بشكل خاص لآفات بطانة القلب).
في حالة ضربات القلب القوية، قد يصف الطبيب ما يلي لعلاج الأعراض: Spigelia، Glonoinum (لسرعة القلب)، Aurum metallicum (لارتفاع ضغط الدم).
لتخفيف شدة ضيق التنفس، يُنصح باستخدام: الغرندليا، والإسفنجيا، واللاهيجيس. لتخفيف آلام القلب، يُنصح باستخدام: الصبار، والشمع، والنايا، والنحاس، وللتخفيف من القلق في هذه الحالة، يُنصح باستخدام الأكونيتوم. في حالة الإصابة بالربو القلبي، يُنصح باستخدام: الديجيتاليس، واللوروسيراسوس، والليكوبس.
الوقاية
الوقاية من التليف المرن المكتسب في القلب والرئتين تتمثل في الوقاية من الأمراض المعدية والالتهابية وعلاجها في الوقت المناسب، وخاصةً تلك التي تُلحق الضرر بالأعضاء الحيوية. يُساعد العلاج الفعال للمرض الأساسي على الوقاية من عواقبه الخطيرة، ومنها التليف المرن. وهذا سبب وجيه للاهتمام بصحتك وصحة الأجيال القادمة، وهو ما يُسمى بالعمل من أجل مستقبل صحي وعمر مديد.
توقعات
تُعتبر تغيرات النسيج الضام المرتبطة بتليف القلب والرئة غير قابلة للعكس. على الرغم من أن بعض الأدوية قد تُقلل من سُمك الشغاف إلى حد ما مع العلاج طويل الأمد، إلا أنها لا تضمن الشفاء التام. مع أن هذه الحالة ليست قاتلة دائمًا، إلا أن تشخيصها لا يزال ضعيفًا نسبيًا. يبلغ معدل البقاء على قيد الحياة لمدة أربع سنوات 77%. [ 14 ]
كما ذكرنا سابقًا، فإن أسوأ تشخيص هو الشكل الخلقي من تليف القلب المرن، حيث تظهر أعراض قصور القلب في الأسابيع والأشهر الأولى من حياة الطفل. لا يمكن إنقاذ الطفل إلا من خلال عملية زرع قلب، وهي بحد ذاتها عملية محفوفة بالمخاطر في هذه المرحلة المبكرة، ويجب إجراؤها قبل بلوغ الطفل عامين. عادةً ما لا يعيش هؤلاء الأطفال طويلًا.
العمليات الأخرى تُجنّب الطفل الموت المُبكّر (وليس دائمًا)، لكنها لا تُشفيه تمامًا من قصور القلب. تحدث الوفاة مع ضعف المعاوضة وتطور فشل الجهاز التنفسي.
يعتمد تشخيص تليف الأنسجة الرئوية المرن على خصائص المرض. إذا تطورت الأعراض بسرعة، تكون احتمالية الإصابة ضئيلة للغاية. أما إذا تطور المرض تدريجيًا، فقد يعيش المريض ما بين 10 و20 عامًا، حتى يحدث فشل تنفسي بسبب تغيرات في الحويصلات الهوائية في الرئتين.
يمكن تجنب العديد من الأمراض التي يصعب علاجها باتخاذ إجراءات وقائية. في حالة تليف القلب، يتمثل الهدف الرئيسي في الوقاية من العوامل التي قد تؤثر على نمو قلب الجنين ودورته الدموية (باستثناء الاستعداد الوراثي والطفرات، التي يعجز الأطباء عن مواجهتها). إذا تعذر تجنبها، يساعد التشخيص المبكر على تحديد الحالة المرضية في مرحلة يمكن فيها إنهاء الحمل، وهو أمر يُعتبر في هذه الحالة إجراءً إنسانيًا.

