خبير طبي في المقال
منشورات جديدة
الورم الأرومي الأرومي العظمي
آخر مراجعة: 04.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
تتزايد حالات الإصابة بالأورام السرطانية باستمرار في العالم. ومن بين آفات الجهاز الهيكلي، يُعد ورم الخلايا العملاقة (أو أوستيوكلاستوما) الأكثر شيوعًا، وهو ورم حميد عرضة للخباثة، قادر على إتلاف مجموعة متنوعة من عظام الهيكل العظمي. [ 1 ] تستمر الصورة السريرية الأولية للمرض دون أن يُلاحظها أحد، ولكن مع مرور الوقت، يلفت تورم منطقة عظمية منفصلة الانتباه: يزداد الورم تدريجيًا ودون ألم. علاج هذا المرض جراحي، ويتضمن إزالة ورم الخلايا العملاقة من داخل الأنسجة السليمة. مع العلاج في الوقت المناسب، تُعتبر نتائج المرض مُشجعة. [ 2 ]
علم الأوبئة
قدم الجراح الفرنسي أوغست نيلاتون أول وصف مفصل لهذا الورم في القرن التاسع عشر. أُدرج تكوين الخلايا العملاقة ضمن فئة اعتلالات العظام الليفية. أُطلق على هذا المرض مُسميات مُختلفة: الورم البني، والورم العملاق، وورم ناقض العظم، واعتلال العظام الليفي الموضعي، وساركوما الخلايا العملاقة. وقد أدخل البروفيسور روساكوف مُصطلح "ورم الخلايا العظمية الناقضة" في المصطلحات الطبية.
لا يشكك المتخصصون اليوم في أصل ورم الخلايا العظمية الناقصة، الذي يُعد من أكثر أورام العظام شيوعًا. يصيب هذا المرض الرجال والنساء بنفس المعدل تقريبًا. وهناك أوصاف لأمراض عائلية ووراثية.
يمكن أن يتطور ورم الخلايا العظمية في أي عمر تقريبًا. وتُعرف حالات اكتشاف الورم لدى الرضع بعمر سنة واحدة وكبار السن بعمر 70 عامًا. ووفقًا للإحصاءات، فإن ما يقرب من 60% من مرضى هذا الورم تتراوح أعمارهم بين 20 و30 عامًا.
ينتمي ورم الخلايا العظمية الناقصة إلى فئة الأورام المنفردة، وعادةً ما يكون وحيدًا. نادرًا ما تتطور هذه البؤر في أنسجة العظام المجاورة. غالبًا ما ينتشر الورم إلى العظام الأنبوبية الطويلة (حوالي 75% من الحالات)، بينما تُصاب العظام الصغيرة والمسطحة بنسبة أقل.
تُصاب العظام الأنبوبية الطويلة بشكل رئيسي في منطقة الكردوس (في مرحلة الطفولة - في منطقة الكردوس). لا يُلاحظ نمو ورم في أنسجة الغضروف المفصلي والغضروف المشاشيّ. وفي حالات نادرة، يُصيب المرض منطقة الجسم (أقل من 1% من الحالات).
يشكل ورم الخلايا العظمية في عظام الوجه أكثر من 20% من جميع الأورام الموجودة في هذا الموقع.
يُفرّق المتخصصون الطبيون بين أورام الخلايا العظمية الخبيثة والحميدة. ويُعدّ الورم الخبيث نادرًا في مرحلة الطفولة.
الأسباب الأورام الأرومية العظمية
لا يستطيع الأطباء تحديد سبب واضح لتطور ورم الخلايا العظمية الناقضة. يُعتقد أن ظهور المرض قد يتأثر بما يلي:
- العمليات الالتهابية التي تؤثر على العظام والغشاء السمحاقي؛
- إصابة مؤلمة أو إصابات متكررة في نفس منطقة العظام؛
- الإشعاعات المتكررة؛
- اضطراب تكوين العظام خلال فترة ما قبل الولادة.
في حوالي سبع من أصل عشر حالات، يؤثر ورم الخلايا العظمية على العظام الأنبوبية الطويلة، لكنه يمكن أن ينتشر إلى الأوتار والأنسجة الرخوة القريبة.
إذا تطور المرض في منطقة الوجه والفكين، فغالبًا ما يكون السبب إصابة عظمية أو عملية معدية - على سبيل المثال، بعد خلع الأسنان أو استئصالها. وفي حالات نادرة، يُسجل ظهور ورم في منطقة الشظية والظنبوب والأضلاع والعمود الفقري.
غالبًا ما تُصاب النساء بالتهاب المفاصل الروماتويدي في اليدين والقدمين وعظام الفخذ والركبة، مع تكوّن ورم الخلايا العملاقة الزلالية الوترية المنتشر. يبدو هذا الورم كثيفًا بين الأنسجة الرخوة، ويتمركز بالقرب من الأوتار. ينتشر الورم تدريجيًا إلى العظم المفصلي، مُتلفًا إياه ومُدمرًا إياه.
بشكل عام، تعتبر أسباب أورام الخلايا العظمية هي التالية:
- تغيرات في التوازن الهرموني؛
- أمراض الغدد الصماء؛
- التعرض للمخاطر المهنية والعادات السيئة؛
- سوء التغذية؛
- الاستخدام الخاطئ أو لفترات طويلة لبعض الأدوية؛
- الآفات الطفيلية؛
- الإقامة لفترة طويلة في المناطق المشعة.
من الممكن أن يتحول ورم الخلايا العظمية الحميد إلى ورم خبيث تحت تأثير:
- إصابات متكررة في أجزاء العظام المتغيرة مرضيًا؛
- التغيرات الهرمونية القوية (على سبيل المثال، أثناء الحمل)؛
- الإشعاع المتكرر.
العوامل المذكورة أعلاه لا تؤدي بالضرورة إلى تطور المرض، ولكنها قد يكون لها تأثير سلبي على الأشخاص المهيئين لتطور ورم الخلايا العظمية.
عوامل الخطر
غالبًا ما يتطور ورم الخلايا العظمية لدى المرضى الذين تزيد أعمارهم عن عشر سنوات. أما لدى الأطفال دون سن الخامسة، فنادرًا ما يحدث هذا المرض.
يزداد خطر الإصابة بالورم تحت تأثير العوامل التالية:
- الظروف البيئية غير المواتية، ووجود المخاطر المهنية والمنزلية، والتسممات، والأمراض المعدية المزمنة، والإصابة بالطفيليات.
- تاريخ الأمراض الأورامية، والعلاج الإشعاعي السابق (خاصة العديد من الدورات)، والتعرض للإشعاع بطرق أخرى (بما في ذلك العيش أو العمل في مناطق خطرة إشعاعيًا).
- إصابات متكررة، كسور، كدمات، شقوق العظام.
- العوامل الوراثية، التغيرات أو الطفرات الجينية، تشخيص الإصابة بالسرطان لدى الأقارب المقربين.
- عيوب العظام الخلقية، واضطرابات البنية الهيكلية.
في كثير من الأحيان، لا يُنظر إلى العامل البيئي كسبب رئيسي، بل يُنظر إليه عبثًا: فالمشاكل البيئية تؤثر بشكل مباشر على جودة الهواء، والمنتجات الغذائية، ونظام المياه في المنطقة، مما يؤثر سلبًا على الصحة. وتُلاحظ الآثار الضارة للأشعة فوق البنفسجية عند زيارة الشواطئ والمسابح المفتوحة لفترات طويلة وبانتظام، مما يؤدي إلى حروق الشمس.
كما نجد تأثير المواد المسرطنة والإشعاعية في العديد من الصناعات الخطرة التي تستخدم مواد كيميائية مثل النيكل والأسبستوس وحمض الكبريتيك والزرنيخ، فضلاً عن معالجة المعادن والبلاستيك.
طريقة تطور المرض
ورم الخلايا العملاقة هو آفة عظمية معقدة حميدة نسيجيًا، نادرًا ما تتكرر، مع أنه مصدرٌ للنقائل الحميدة، ويتحول غالبًا إلى ساركوما بعد التعرض للإشعاع. في غياب أصل نسيجي واضح، يُسمى ورم الخلايا العملاقة بهذا الاسم نظرًا لمظهره النسيجي المميز.
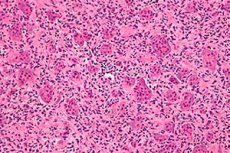
الوصف المورفولوجي النموذجي هو آفة خلايا سترومالية وحيدة النواة حميدة، مع وفرة من الخلايا العملاقة الحميدة الشبيهة بالخلايا الناقضة للعظم. تُظهر الدراسات المناعية النسيجية والجزيئية لأنسجة ورم الخلايا الناقضة للعظم وجود مجموعتين من الخلايا السترومالية، إحداهما تتكون من خلايا مغزلية متكاثرة تُمثل علامات على أصلها العظمي، [ 3 ] و[ 4 ]، بينما تتكون المجموعة الأخرى من خلايا متعددة الأضلاع تتصبغ بمستضدات الخلايا الوحيدة/البلعمية CD14+/CD68+. [ 5 ]
السمات المرضية الرئيسية لورم الخلايا العظمية:
- يتضمن الورم نوعين من الخلايا: الخلايا العملاقة متعددة النوى والخلايا أحادية النواة الصغيرة؛
- في أغلب الأحيان تتأثر الأجزاء البعيدة من عظم الفخذ، والجزء القريب من قصبة الساق، والجزء البعيد من عظم الكعبرة، وكذلك عظام الحوض والكتف (في حالات أقل - العمود الفقري)؛
- الآفة معزولة ومنفردة في الغالب؛
- الورم يقع في الغدة الصنوبرية أو الكردوس، ويتضخم بشكل كبير، ويتشوه على شكل درنة كبيرة أو نصف كرة؛
- تصل العملية المرضية إلى الغضروف المفصلي وتتوقف؛
- ينمو الورم في جميع الاتجاهات، ولكن النمو الرئيسي يلاحظ على طول محور العظم الطويل باتجاه عظمة الساق؛
- يتزايد البعد العرضي قطريًا أكثر من ثلاث مرات؛
- في النوع الخلوي من ورم الخلايا العظمية، يتكون الورم من حجرات منفصلة عن بعضها البعض بواسطة حواجز كاملة وجزئية (مثل رغوة الصابون أو أقراص العسل غير المنتظمة)؛
- يوجد تباعد في القشرة، وتورم من الداخل، وترقق، وعدم وجود طبقات السمحاق؛
- إذا كان حجم الورم العظمي كبيرًا، يتم امتصاص القشرة، ويحيط الورم بكبسولة رقيقة تتكون من جدران الغرف السطحية؛
- في المتغير العظمي التحللي، لا يوجد نمط حجرة، عيب العظم متجانس؛
- عيب هامشي على شكل صحن؛
- يُلاحظ إعادة امتصاص الطبقة القشرية، وتصبح القشرة أكثر حدة عند خط الضرر، دون تقويض أو تقويض الطبقات السمحاقية؛
- العيب له ملامح واضحة؛
- يتم ملاحظة الكسور المرضية في 12٪ من المرضى.
يصيب ورم الخلايا العظمية الناقضة مناطق غنية بنخاع العظم النقوي. غالبًا ما تُكتشف انحناءات واضحة وقصر في العظم، خاصةً في حالات تأخر التشخيص والعلاج. في معظم الحالات، يكون موقع الورم شاذًا، مع تدمير الغالبية العظمى من لقم العظام. يُلاحظ إشعاعيًا وصول الورم إلى الطبقة العظمية تحت الغضروفية. في نصف الحالات تقريبًا، يُصاب الطرف المفصلي للعظم بأكمله، مما يؤدي إلى تورمه وتدمير الطبقة القشرية، ويمتد الورم إلى ما وراء حدود العظم.
في الوقت الحاضر، نادرًا ما يُعتبر ورم الخلايا العظمية ورمًا حميدًا: يتم تصنيفه على أنه ورم عدواني، وذلك في المقام الأول بسبب عدم القدرة على التنبؤ به واحتمالية الإصابة بالخباثة.
الأعراض الأورام الأرومية العظمية
تتشابه المظاهر السريرية في الطفولة والشيخوخة تقريبًا. لا تُكتشف العلامات الأولى فورًا، إذ يتطور ورم الخلايا العظمية الكامن في البداية، ولا يُمكن تشخيصه إلا بعد مرور عام تقريبًا على بدء نموه.
يُقسّم الخبراء الأعراض إلى عامة وموضعية. عادةً ما تُصاحب أورام الخلايا العظمية الخبيثة علامات عامة، بينما تُوجد علامات موضعية في الأورام الحميدة.
لا تعتمد الأعراض العامة على مكان العظم المصاب:
- ألم شديد في منطقة نمو الورم؛
- وخز الجس، مما يدل على نمو الورم وتدمير قطعة العظام؛
- ظهور شبكة من الأوعية فوق البؤرة المرضية؛
- زيادة ثابتة في الانتفاخ؛
- تزايد الألم مع نمو الورم؛
- ضعف وظيفة العضلات والمفاصل بالقرب من المنطقة المصابة؛
- تضخم الغدد الليمفاوية القريبة؛
- الضيق العام والتعب؛
- ارتفاع درجة حرارة الجسم؛
- فقدان الشهية وفقدان الوزن؛
- اللامبالاة والعجز.
ترتبط الأعراض الموضعية بموقع العظم المصاب. على سبيل المثال، إذا تطور ورم الخلايا العظمية الناقضة في أحد الفكين، يضطرب تناسق الوجه تدريجيًا. يبدأ المريض بمواجهة صعوبات في الكلام والمضغ، وأحيانًا تتخلخل الأسنان وتتساقط. في الحالات الشديدة، تتكون مناطق نخرية ونواسير.
تظهر 90% من أورام الخلايا العملاقة موقعًا نموذجيًا في المشاش. غالبًا ما يمتد الورم إلى العظم تحت الغضروفي المفصلي أو حتى يلامس الغضروف. نادرًا ما يتأثر المفصل و/أو محفظته. في الحالات النادرة التي يحدث فيها ورم ناقض للعظم عند الطفل، من المرجح أن يكون الآفة في الكردوس. [ 6 ]، [ 7 ] المواقع الأكثر شيوعًا بالترتيب التنازلي هي عظم الفخذ البعيد، والظنبوب القريب، والكعبرة البعيدة، والعجز. [ 8 ] تنشأ 50% من أورام ناقضة العظم في منطقة الركبة. تشمل المواقع الشائعة الأخرى رأس الشظية، وعظم الفخذ القريب، وعظم العضد القريب. موقع الحوض نادر. [ 9 ]، [ 10 ] من المعروف أن تعدد المراكز، أو الظهور المتزامن لورم ناقض للعظم في مواقع هيكلية مختلفة، يحدث ولكنه نادر للغاية. [ 11 ]، [ 12 ]
إذا تطور ورم الخلايا العظمية الناقضة في الساقين، تتغير مشية المريض، ومع مرور الوقت، تضمر عضلات الطرف السفلي المصاب، ويصبح المشي صعبًا. في بعض الحالات، تحدث عمليات عظمية ضمورية، ويصبح العظم أرق. تحدث كسور مرضية، مصحوبة بمتلازمة ألم شديد وتورم في الأنسجة. قد تحدث مضاعفات على شكل نزيف، وأورام دموية، ونخر في الأنسجة الرخوة.
إذا تطور ورم الخلايا العظمية في منطقة عظم العضد أو عظم الفخذ، فإن المهارات الحركية لسلاميات الأصابع والوظيفة العامة للطرف المصاب تكون ضعيفة.
عندما يصبح الورم خبيثًا، تتفاقم حالة المريض. ومن العلامات الجديرة بالملاحظة:
- يزداد الألم في المنطقة المصابة من العظم؛
- الورم ينمو بشكل مطرد؛
- يتم تدمير أنسجة العظام، وتتوسع منطقة هذا التدمير؛
- يفقد بؤرة الورم حدودها الواضحة؛
- يتم تدمير الطبقة القشرية.
لا يمكن رؤية مثل هذه التغييرات إلا من قبل متخصص عند إجراء التشخيص الآلي.
تتميز أورام الخلايا العظمية الناقضة الحميدة بمسار تدريجي كامن أو بدون أعراض. تحدث متلازمة الألم فقط أثناء تطور المرض؛ وبعد عدة أشهر، يبدأ المريض بالشعور بألم منتشر. لدى العديد من المرضى، يكون أول مؤشر على المرض هو الكسر المرضي. عند التشخيص، يعاني حوالي 12% من مرضى أورام الخلايا العظمية الناقضة حاليًا من كسر مرضي. [ 13 ]، [ 14 ] يُعتقد أن وجود كسر مرضي يشير إلى مرض أكثر عدوانية مع ارتفاع خطر التكرار الموضعي والانتشار النقيلي. [ 15 ]
عندما يصبح الورم العظمي الناقص العظم خبيثًا، يُصبح الورم، الذي كان بالكاد يُلاحَظ سابقًا، مؤلمًا، وتُلاحَظ علامات تهيج في النهايات العصبية. إذا كان الورم خبيثًا في المقام الأول، يُصاحبه ألم شديد ومُنهك، مع تفاقم سريع في الأعراض العصبية.
ورم الخلايا العظمية عند الأطفال
غالبًا ما تختلف العلامات السريرية للأشكال المختلفة من أورام الخلايا العظمية الخبيثة الحميدة. لا تظهر الأعراض في الأشكال الكيسية لفترة طويلة، وفي 50% من الحالات لا تُكتشف إلا بعد حدوث كسر مرضي. يُكتشف نمو الورم مع تكاثر شديد داخل الأنسجة العظمية، مع ظهور متلازمة الألم. لا يحدث بروز جزء من العظم إلا مع تكاثر واضح: يعاني المريض من توسع في شبكة الأوردة، وحركة محدودة للمفاصل. يتميز الشكل الانحلالي من أورام الخلايا العظمية الخبيثة بنمو أسرع، وظهور مبكر للألم، ولكن تقل احتمالية حدوث التقلصات.
في أغلب الأحيان، يصيب ورم الخلايا العظمية الناقضة في مرحلة الطفولة الكردوس العلوي لعظمي العضد والفخذ. وفي حالات أقل شيوعًا، تُلاحظ الآفات في الكردوس السفلي للفخذ، وعظمي الظنبوب والشظية. في الشكل الانحلالي، من الممكن تدمير غضروف المشاش مع انتشاره إلى المشاش، دون اختراق المفصل (حيث يبقى الغضروف المفصلي سليمًا). أما في الشكل الكيسي النشط، فيُلاحظ نمو الورم في الجزء المركزي من الجسم العظمي، مع ترقق حاد في الطبقة القشرية وتورم العظام.
غالبًا ما تكون أورام الخلايا العظمية الناقصة لدى الأطفال حميدة، ولكنها قد تُسبب أيضًا تدميرًا عظميًا كبيرًا. عندما ينمو غضروف المشاش، يتباطأ نمو منطقة الأطراف، وقد تحدث كسور مرضية، والتهاب مفصل كاذب مع عيب عظمي واضح، ومتلازمة الألم.
في حالة الورم الخبيث، يتكون ورم من نوع الساركوما العظمية، ويتميز بنمو سريع وتدمير واضح للعظام. للتشخيص التفريقي، يخضع الأطفال لفحص نسيجي.
مراحل
يميز الخبراء بين المرحلة التحللية والمرحلة الخلوية الإسفنجية لتطور ورم الخلايا العظمية.
- المرحلة الخلوية الإسفنجية تتميز بتكوين بؤر تدمير أنسجة العظام المفصولة بأقسام.
- تتميز المرحلة الانحلالية بتكوين بؤرة تدميرية مستمرة، متمركزة بشكل غير متماثل بالنسبة لمحور العظم المركزي. ومع نمو الورم، يمكن أن ينتشر إلى كامل المقطع العرضي للعظم.
من العلامات النموذجية لورم الخلايا العظمية الناقضة انفصال البؤرة المصابة عن الجزء السليم من العظم. تُفصل قناة نخاع العظم عن الورم بواسطة صفيحة غلق.
إستمارات
اعتمادًا على المعلومات السريرية والإشعاعية والسمات المورفولوجية، يتم التمييز بين الأنواع الأساسية التالية من أورام الخلايا العظمية:
- يُلاحظ النوع الخلوي بشكل رئيسي لدى المرضى في منتصف العمر وكبار السن. يتطور الورم ببطء، ليكشف في النهاية عن نفسه كتورم كثيف ذي سطح عقدي، دون إمكانية فصله عن العظم السليم. عند تمركزه في منطقة الفك، يتخذ الأخير شكلًا مغزليًا. لا يتغير موضع الأسنان. يتميز النسيج الذي يغطي ورم الخلايا العظمية الخلوي بفقر الدم. يُلاحظ بالتصوير الشعاعي وجود ظل من عدد كبير من التكوينات الكيسية والخلوية، منفصلة عن بعضها البعض بحواجز. لا يوجد أي رد فعل من السمحاق.
- يُسبب الشكل الكيسي من ورم الخلايا العظمية الناقضة في البداية إحساسًا بالألم. عند جس الورم، تكون بعض مناطقه مرنة، ويُلاحظ عرض "طقطقة الرق". يصبح العظم فوق الورم أرق، وله شكل أملس ومحدب وقبّي الشكل. في الصورة الشعاعية، تشبه الآفة كيسًا سنّيًا أو ورمًا مينايًا.
- يُعدّ النوع الانحلالي من الأمراض نادرًا نسبيًا، خاصةً لدى الأطفال والمراهقين. ينمو الورم بسرعة كبيرة. على خلفية ترقق الطبقة القشرية، يظهر الألم: يبدأ في البداية بالانزعاج أثناء الراحة، ثم عند جس المنطقة المصابة. يُلاحظ توسع في شبكة الأوعية الدموية فوق موقع الورم. عندما يتركز الورم في منطقة الفك، تصبح الأسنان ملتوية ومتحركة. من المحتمل حدوث كسور مرضية. تظهر منطقة غير منظمة من التنوير في الصورة الشعاعية.
وفقًا لدرجة الخباثة، يتم تقسيم أورام الخلايا العظمية إلى حميدة (بدون خلل خلوي)، وخبيث أولي، وخبيث (متحول من ورم حميد).
اعتمادًا على التوطين، يتم التمييز بين أنواع الأمراض التالية:
- الشكل المحيطي لورم الخلايا العظمية على الفك العلوي لا يحتوي على أي ميزات مورفولوجية خاصة ويقع على اللثة.
- يقع الشكل المركزي داخل بنية العظم، وعلى عكس الشكل المحيطي، يحتوي على مناطق نزفية تُسبب اللون البني للورم. ويمثل الورم تكتل واحد.
- يقع ورم العظم العظمي في الفك السفلي في سماكة النسيج العظمي، في منطقة الأضراس والضواحك. يستمر نمو الورم لعدة سنوات (في المتوسط من 3 إلى 10 سنوات)، مصحوبًا بخلل في وظيفة المفصل الصدغي الفكي.
- يتجلى ورم الخلايا العظمية في الفك العلوي ببروز منطقة الفك المصابة، وتخلخل الأسنان، وعدم تناسق الوجه. ينمو الورم ببطء وبدون ألم.
- ورم الخلايا العظمية العظمية في عظم الفخذ هو أكثر الأمراض شيوعًا، ويصيب منطقة نمو العظام: المدور الكبير، وعنق ورأس عظم الفخذ. وفي حالات نادرة، يُصاب المدور الصغير (بشكل معزول). ويصاحب هذا المرض ألم، وتشوه في العظام، وكسور مرضية.
- غالبًا ما يتطور ورم الخلايا العظمية في عظمة الحرقفة عند قاعدتها. من الممكن أيضًا أن يُصيب الغضروف على شكل حرف Y مع تدمير الفرع الأفقي لعظمة العانة أو الفرع النازل لعظمة الإسك. تكون الحالة المرضية في البداية بدون أعراض، ثم يظهر الألم عند بذل مجهود، ثم العرج.
المضاعفات والنتائج
إن أسوأ عواقب أورام الخلايا العظمية الحميدة هي تحولها إلى ورم خبيث. يُعدّ ورم الخلايا العملاقة الخبيث نادرًا؛ إذ كشف تحليل للدراسات عن نسبة حدوث 1.6% من الأورام الخبيثة الأولية و2.4% من الأورام الخبيثة الثانوية. يُكتشف نمو تسللي، وتُصاب العقد الليمفاوية الأقرب، وقد ينتشر الورم النقيلي. [ 16 ]
الورم العظمي الخبيث ذو الخلايا العملاقة قادر على إنتاج الأنواع التالية من النقائل:
- ساخن (يتطور بسرعة، ويدمر الأنسجة المحيطة بنشاط)؛
- بارد (بدون تطور محدد، موجود لفترة طويلة في حالة غير نشطة، ولكن لديه القدرة على التحول إلى "ساخن")؛
- أخرس (موجود في حالة من عدم الحيوية ويتم اكتشافه بالصدفة).
يمكن أن يحدث ورم الخلايا العظمية الخبيثة في ثلاثة أشكال:
- يحتفظ الورم الخبيث الأولي بنوع بنيته الأساسية، ولكن هناك عدم نمطية للعناصر أحادية النواة ووجود الانقسام الفتيلي فيها.
- خباثة ورم حميد في المقام الأول مع تطور ساركوما الخلايا المغزلية أو ساركوما العظام.
- الخباثة بعد علاج سابق، وخاصةً بعد التدخلات غير الجذرية أو العلاج الإشعاعي غير المنطقي. في هذه الحالة، غالبًا ما يتطور ساركوما الخلايا متعددة الأشكال مع نقائل رئوية.
يُعتبر الورم العظمي الناقض الخبيث عمومًا ساركوما عالي الدرجة؛ [ 17 ] ومع ذلك، تشير البيانات من الدراسات إلى أن الورم العظمي الناقض الخبيث يتصرف مثل الساركوما منخفضة أو متوسطة الدرجة. [ 18 ] يحدث النقائل في 1-9% من المرضى المصابين بالورم العظمي الناقض، وقد ربطت بعض الدراسات السابقة بين حدوث النقائل والنمو العدواني والتكرار الموضعي. [ 19 ]، [ 20 ]
بعد التدخلات الجراحية، يتم توزيع المرضى الذين يعانون من قدرة محدودة أو مفقودة على العمل على مجموعة الإعاقة المناسبة.
التشخيص الأورام الأرومية العظمية
لتشخيص ورم الخلايا العظمية، من الضروري استخدام الطرق التالية:
- - استجواب المريض، والفحص الدقيق وجس المنطقة المصابة من العظم، ودراسة التاريخ المرضي؛
- التشخيص المختبري والأدواتي والدراسات المورفولوجية.
عند تحديد تاريخ الحالة المرضية، يُولي الطبيب اهتمامًا للأعراض الأولية للورم، ووجود الألم وطبيعته، والأمراض والإصابات السابقة، والعلاج السابق، والحالة العامة. من المهم أيضًا توضيح حالة الجهاز البولي، والتناسلي، والجهاز التنفسي، والكبد والكلى، والعقد اللمفاوية، وإجراء تشخيص بالموجات فوق الصوتية للأعضاء الداخلية.
يُوصى لجميع المرضى بإجراء فحوصات دم وبول، لتحديد البروتين والكسور، وأحماض السياليك، والفوسفور، والكالسيوم. من الضروري تحديد النشاط الأنزيمي للفوسفاتاز، وإجراء اختبار ثنائي الفينيل، وتقييم البروتين التفاعلي-سي، وما إلى ذلك. تجدر الإشارة إلى أن المؤشرات المخبرية لأورام العظام عادةً ما تكون غير محددة، ولكنها قد تساعد في التشخيص التفريقي. على سبيل المثال، في حالة ورم الخلايا العظمية الخبيثة، من الممكن حدوث تغيرات مثل زيادة عدد كريات الدم البيضاء، وتسارع معدل ترسيب كرات الدم الحمراء، وانخفاض بروتين الدم والحديد غير الهيموغلوبيني، وزيادة أحماض السياليك والفوسفاتاز القلوي. يظهر أوكسي برولين وهيكسوكيناز في البول. ترتفع مستويات الفوسفور والكالسيوم في مصل الدم.
تشمل الدراسات التقليدية للاشتباه في الإصابة بورم الخلايا العظمية الناقضة للأنسجة، الأشعة السينية العامة والموجهة، والتصوير المقطعي. تتيح الأشعة السينية تحديد موقع المرض وحجمه وطبيعته بدقة أكبر، بالإضافة إلى تحديد انتشاره إلى الأعضاء والأنسجة المحيطة. يتيح التصوير المقطعي المحوسب فحص التدمير المرضي العميق وتحديد حجم الآفة داخل العظم. ومع ذلك، يُعتبر التصوير بالرنين المغناطيسي أكثر إفادة: فبناءً على المعلومات التي يتم الحصول عليها أثناء الدراسة، يمكن للأطباء تجميع صورة مكانية، بما في ذلك صورة ثلاثية الأبعاد.
أثناء الفحص المورفولوجي، تُدرس المادة المأخوذة من خلال الشفط وخزعة النتوءات، أو مناطق العظام المُستأصلة مع ورم الخلايا العظمية الناقضة. تُجرى خزعة الوخز باستخدام إبر خاصة، ويُثقب الورم تحت مراقبة الأشعة السينية.
أثناء فحص العظام الأنبوبية الطويلة بالأشعة السينية، وُجد لدى المرضى بؤرة تدميرية تحللية للعظم، متمركزة بشكل شاذ في منطقة المشاش. في الديناميكيات، ينتشر المرض نحو الغضروف المفصلي، وكذلك نحو الكردوس العظمي، ويمكن أن يشغل المقطع العرضي بأكمله (وهو أمر شائع في أورام الخلايا العظمية الناقضة لرأس الشظية والكعبرة). تكون الطبقة القشرية رقيقة للغاية ومتورمة، وغالبًا ما يُكتشف تدمير جزئي. في الورم الحميد، لا يوجد تفاعل سمحاقي. تكون الحدود بين الورم والمادة الإسفنجية غير واضحة. في الغالبية العظمى من الحالات، تكون الحدود المتصلبة غائبة.
في حالات تلف النخاع الشوكي، يقع الورم في جسم الفقرة في 80% من الحالات. قد يتأثر الجسم الذي يحتوي على القوس والناتئ، وأحيانًا تشمل العملية المرضية عدة فقرات، وأجزاء ضلعية، والمفصل العجزي الحرقفي. قد تكون البؤر المدمرة ذات بنية خلوية أو انحلالية.
عند دراسة الصور الطبقية على التصوير المقطعي المحوسب، يُحدَّد تدمير القوس مع النتوءات العرضية، وهو ما لا يمكن رؤيته بالأشعة السينية العادية. يسمح لنا استخدام التصوير بالرنين المغناطيسي بفحص تأثير الورم على الحبل الشوكي. [ 21 ]، [ 22 ]
يُعرَّف ورم الخلايا العظمية الخبيثة الأولي في الصورة الشعاعية بأنه بؤرة تدميرية انحلالية ذات حدود غير واضحة. في بعض الحالات، يكون الهيكل خشنًا وشبكيًا. يحدث تورم في منطقة العظم المصابة، وترقق شديد في الطبقة القشرية، مع تدميرها لاحقًا. تكون الصفيحة القشرية غير متجانسة من الداخل. من المحتمل حدوث تفاعل سمحاقي.
في حالة التحول الخبيث لورم الخلايا العظمية الناقضة الحميد في البداية، يُكشف عن بنية شبكية كبيرة أو صغيرة أو انحلالية للبؤرة التدميرية. تكون منطقة العظم المصابة "متورمة"، وتكون الطبقة القشرية رقيقة جدًا، ذات حدود غير متساوية على الجانب الداخلي. من المحتمل حدوث تلف قشري. يتميز رد فعل السمحاق (ذروة كودمان الضعيفة) بالتهاب السمحاق البصلي.
ولكشف احتمالية وجود نقائل، يتم وصف التصوير بالموجات فوق الصوتية للمساعدة في دراسة حالة الأعضاء الداخلية.
المرحلة الأخيرة في تشخيص أورام العظام هي التحديد النسيجي والفحص الخلوي للمسحات. تُؤخذ المادة عن طريق الخزعة (الفتح أو الوخز).
تشخيص متباين
تتطلب أورام الخلايا العظمية الحميدة تمييزها عن جميع الأمراض التي تُظهر علامات كيس عظمي أو انحلال نسيجي في التصوير الشعاعي. وتشمل هذه الأمراض:
- خلل التنسج الليفي؛
- الساركوما العظمية الانحلالية؛
- خلل تنسج العظم جار الدرقية؛
- بؤرة مرض السل العظمي؛
- كيس عظمي تمددي.
في حال وجود آفات عظمية كبيرة ومتفاقمة، يُشتبه في وجود ورم عضلي عظمي. يتميز هذا الورم بغياب هشاشة العظام المحيطة، وتلف العظام من الكردوس، واختراق متأخر للمرض إلى المشاش.
من الممكن التفريق بين خلل التنسج العظمي جار الدرقية وورم الخلايا العظمية فقط باستخدام التصوير الشعاعي والدراسات الكيميائية الحيوية.
قد تنشأ صعوبات أثناء تشخيص أورام الخلايا العظمية الأنبوبية الطويلة، وكذلك عند التمييز بين المرض والأورام الساركومية العظمية أو التكوينات الكيسية (العظمية أو الوعائية).
يقع الكيس التمددي بشكل رئيسي في الجسم العظمي أو الكردوس. في حالة وجود هذا الكيس في مكان غير مركزي، يُلاحظ تورم موضعي في العظم، وطبقة قشرية رقيقة: يمتد الورم على طول العظم، وقد يحتوي على جزيئات كلسية. في حالة وجوده في مكان مركزي، ينتفخ الجسم العظمي أو الكردوس بشكل متماثل، وهو ما لا يحدث في حالة ورم الخلايا العظمية الناقضة.
في مرحلة الطفولة، قد يُخلط بين ورم الخلايا العظمية الناقضة وخلل التنسج العظمي الليفي أحادي الشكل. في هذه الحالة، يكون العظم مشوهًا، ويقصر (وأحيانًا يطول)، ولكنه لا يتورم، كما هو الحال في ورم الخلايا العظمية الناقضة. يؤثر خلل التنسج العظمي الليفي بشكل رئيسي على الكردوس والجسم العظمي للعظام الأنبوبية. قد تزداد سماكة الطبقة القشرية، وتتشكل مناطق متصلبة حول مناطق التدمير. عملية النمو بطيئة وغير مؤلمة.
إذا كان ورم الخلايا العظمية يؤثر على الفك السفلي، فيجب التمييز بين المرض ورم الأسنان، وورم ليفي عظمي، وورم أدامانتيني، وكيس الأسنان.
من الاتصال؟
علاج او معاملة الأورام الأرومية العظمية
يهدف العلاج إلى تقليل المضاعفات وتحسين وظيفة العظم المصاب؛ وكان هذا العلاج يُجرى تقليديًا عن طريق كحت داخل الآفة مع حشو التجويف. أما التقنيات الحديثة، مثل التثبيت باستخدام أسمنت العظام، فتُعدّ مُشجعة لأنها تُساعد في إعادة البناء وتُقلل من تكرار الإصابة موضعيًا.[ 23 ]
الطريقة الوحيدة للتخلص تمامًا من ورم الخلايا العظمية هي من خلال الجراحة: يتم إزالة الورم، مما يمنع المزيد من الضرر للعظام.
تُكشط أورام الخلايا العظمية الصغيرة بعناية باستخدام مكشطة خاصة. ويُستبدل العيب العظمي الناتج بزراعة ذاتية. في حالة الأورام الكبيرة، يُجرى استئصال العظم متبوعًا بجراحة تجميلية. [ 24 ]، [ 25 ]، [ 26 ]
ونظرًا للمعدل المرتفع (25-50%) للتكرار الموضعي بعد الكحت وترقيع العظام، فقد تم تشجيع الجراحين على تحسين إجراءاتهم الجراحية باستخدام المواد المساعدة الكيميائية أو الفيزيائية مثل النيتروجين السائل، والأسمنت الأكريليكي، والفينول، وبيروكسيد الهيدروجين، والعلاج الكيميائي الموضعي أو العلاج الإشعاعي.[ 27 ]،[ 28 ] وقد ثبت أن العلاج المساعد الموضعي يساعد في السيطرة على معدل التكرار.[ 29 ]
إذا كان المريض، لأي سبب كان، ممنوعًا من التدخل الجراحي، يُوصف له العلاج الإشعاعي. فبمساعدة الإشعاع، يُمكن إيقاف نمو الورم وتدمير بنيته. [ 30 ]
ومن الممكن أيضًا استخدام التقنيات التالية:
- إعطاء أدوية ستيرويدية داخل الآفة. هذه الطريقة حديثة نسبيًا ولم تُستخدم منذ فترة طويلة. من خلال الحقن، يُمكن تحقيق نتائج إيجابية مع أورام الخلايا العظمية الناقضة الصغيرة: يتقلص حجم الورم. في بعض الأحيان، في نهاية العلاج، تُصبح الآفة أكثر عتامة للأشعة السينية مقارنةً بمنطقة العظام المحيطة بها.
- إدخال ألفا-إنترفيرون. بناءً على نظرية المنشأ الوعائي لأورام الخلايا العظمية الناقضة، طبّق المتخصصون حقن ألفا-إنترفيرون. يتميز هذا الدواء بقدرة مضادة لتكوّن الأوعية الدموية، أي أنه يُبطئ نموها. وقد أثبتت هذه الطريقة فعاليتها لدى حوالي 50% من المرضى، إلا أنها نادرة الاستخدام نسبيًا، وذلك بسبب كثرة آثارها الجانبية، مثل الصداع، وتدهور الصحة العامة، والإرهاق الشديد، وضعف القدرة على العمل.
لعلاج أورام الخلايا العظمية الخبيثة (الأولي أو الثانوي)، يُستخدم التدخل الجراحي فقط، والذي يشمل استئصال الورم مع منطقة العظم. قبل العملية وبعدها، يُوصف للمريض علاج إشعاعي وكيميائي.
يمكن علاج أورام العظام غير القابلة للجراحة (على سبيل المثال، بعض أورام العجز والحوض) عن طريق قسطرة إمداد الدم لها.
- العلاج المضاد لـ RANKL
تُفرط الخلايا العملاقة في التعبير عن وسيط رئيسي في تكوين الخلايا الناقضة للعظم: مستقبل RANK، والذي يُحفَّز بدوره بواسطة السيتوكين RANKL، الذي تُفرزه الخلايا السدوية. وقد أسفرت دراسات دينوسوماب، وهو جسم مضاد وحيد النسيلة يرتبط تحديدًا بمستقبل RANKL، عن نتائج علاجية مبهرة، مما أدى إلى اعتماده من قِبل إدارة الغذاء والدواء الأمريكية (FDA). [ 31 ]، [ 32 ] يُخصَّص دينوسوماب في المقام الأول للمرضى المعرضين لخطر كبير لتكرار المرض بعد الجراحة الأولية والتكرار الموضعي.
العلاج الجراحي
تشير دراسات مختلفة إلى أن الاستئصال الواسع يرتبط بانخفاض خطر تكرار المرض محليًا مقارنة بالكحت داخل الآفة وقد يزيد من معدل البقاء على قيد الحياة دون تكرار المرض من 84% إلى 100%.[ 33 ]،[ 34 ]،[ 35 ] ومع ذلك، يرتبط الاستئصال الواسع بمعدل أعلى من المضاعفات الجراحية ويؤدي إلى ضعف وظيفي، والذي يتطلب عادةً إعادة البناء.[ 36 ]،[ 37 ]،[ 38 ]
إذا كان ورم الخلايا العظمية موضعيًا في العظام الأنبوبية الطويلة، فقد يتم استخدام التدخلات الجراحية التالية:
- يُجرى الاستئصال الهامشي باستخدام تقنية الاستئصال الجزئي أو الذاتي في حالة أورام الخلايا العظمية الحميدة، التي تنمو ببطء، ولها بنية خلوية، وتقع على محيط النتوء العظمي. ويُمكن التثبيت بمسامير معدنية.
- إذا امتد نتوء الورم إلى منتصف العظم القطري، يُزال ثلثا اللقمة وجزء من الجسم مع السطح المفصلي. يُملأ العيب بطعم غضروفي. تُستخدم مسامير ربط قوية. يُوصل الطعم بالطبقة القشرية للعظم المضيف بشكل مائل لتجنب هبوط المفصل.
- في حال تلف النتوء العظمي أو وجود كسر مرضي، يُجرى استئصال قطعي مع تفكيك المفصل واستبدال العيب بطعم خيفي. يُثبّت بقضيب على أسمنت.
- في حالة الكسر المرضي وسرطان الخلايا العظمية الخبيثة في الجزء القريب من عظم الفخذ، يتم إجراء جراحة استبدال مفصل الورك بالكامل.
- عند إزالة الأجزاء الطرفية المفصلية لمفصل الركبة، تُستخدم عملية زرع نصف مفصلي مع تثبيت قوي. ويمكن إجراء تركيبات اصطناعية كاملة فردية مع جذع ممتد من التيتانيوم، ثم العلاج الإشعاعي.
- إذا كان الورم العدواني موضعيًا في الطرف البعيد من قصبة الساق، يُجرى استئصال مع تثبيت مفصل الكاحل. في حالة تلف عظم الكاحل، يُلجأ إلى استئصال العظم مع تثبيت مفصلي تطويلي وفقًا لـ Zatsepin.
- إذا كان التركيز المرضي موضعيًا في العمود الفقري العنقي، يُجرى الوصول الأمامي إلى الفقرات. ويمكن الوصول الأمامي الجانبي مع الفصل الدقيق بين البلعوم والجانب الأمامي من الفقرات وقاعدة الجمجمة.
- على مستوى الفقرات الصدرية الأولى والثانية ، يُستخدم نهج أمامي مع شق مائل لعظم القص حتى الفراغ الوربي الثالث. تُدفع الأوعية الدموية للأسفل بحرص. إذا كانت الإصابة تقع في الفقرات الصدرية الثالثة إلى الخامسة، يُجرى نهج أمامي جانبي واستئصال للضلع الثالث. يُدفع لوح الكتف للخلف دون قطع العضلات. قد تنشأ صعوبات عند الوصول إلى الأسطح الأمامية للفقرات العجزية العلوية. يُستخدم نهج أمامي جانبي خلف الصفاق الأيمن، مع فصل دقيق للأوعية الدموية والحالب.
- إذا تم اكتشاف تدمير شديد للفقرات، أو انتشار الورم إلى الأقواس في العمود الفقري الصدري والقطني العجزي، يتم إجراء التثبيت عبر العمود الفقري وعبر الصفيحة مع إزالة الفقرات المصابة وتقويمها ذاتيًا.
- إذا وُجد ورم الخلايا العظمية الناقضة في عظم العانة وعظم الإسك، تُزال المنطقة المصابة ضمن حدود الأنسجة السليمة دون الحاجة إلى زراعة عظام. أما إذا تأثر الجزء السفلي وسقف الحُقّ، فيُوصى بإزالته مع استبدال العظم البلاستيكي للعيب لاحقًا.
- في حال تلف العجز والفقرة القطنية الخامسة ، تُزال الأجزاء المصابة من الخلف وتُثبّت باستخدام التثبيت عبر القدم. ثم يُزال الورم خلف الصفاق، ثم تُجرى عملية ترقيع عظمي.
الوقاية
لا توجد إجراءات وقائية محددة للوقاية من أورام الخلايا العظمية المنجلية. للوقاية، ينصح المتخصصون بإجراء فحص بالأشعة السينية بانتظام كل سنة إلى سنتين للكشف المبكر عن هذه الأورام وعلاجها.
إذا اكتشف الشخص أي ضغط في العظام، يجب عليه استشارة الطبيب على الفور: معالج، أو أخصائي تقويم العظام، أو أخصائي أورام، أو أخصائي إصابات، أو أخصائي فقرات.
وتشمل التوصيات الطبية الإضافية ما يلي:
- تجنب الإصابات والتسممات، وتناول الطعام بشكل سليم ومغذي، وممارسة النشاط البدني؛
- استشارة الطبيب في الوقت المناسب، بما في ذلك فيما يتعلق بأمراض الجهاز العضلي الهيكلي؛
- تأكد من زيارة الطبيب وإجراء فحص تشخيصي في حال ظهور أي نمو جديد ذو أصل غير معروف.
توقعات
في مرضى أورام الخلايا العظمية الناقضة، تعتمد نتيجة المرض على عوامل عديدة، مثل خصائص تطور الورم، وخباثته أو حميدته، وموقعه، وانتشاره، وتوقيت العلاج، وغيرها. في السنوات الأخيرة، أصبحت نتائج علاج أورام العظام الخبيثة أكثر تقدمًا. يستخدم الأطباء نهجًا علاجيًا مشتركًا، وعند الضرورة، باستخدام العلاج الكيميائي المكثف. في الوقت نفسه، تتجاوز نسبة المرضى المتعافين تمامًا 70%.
يقول الخبراء إن التشخيص يكون إيجابيًا إذا أُزيل الورم العظمي الناقض للعظم جراحيًا بالكامل ولم تحدث انتكاسات. يسعى الجراحون، كلما أمكن، إلى إجراء عمليات الحفاظ على الأعضاء مع ترقيع العظام في نفس الوقت، وفي بعض الحالات فقط يكون الأمر متعلقًا بتدخلات تشويهية، وبعدها لا يعود الشخص قادرًا على القيام ببعض الأنشطة: فيضطر إلى تغيير نمط حياته. في مثل هذه الحالات، يفهم الأطباء مصطلح "التعافي" على أنه "غياب الأورام". يحتاج هؤلاء المرضى إلى إعادة تأهيل طويلة الأمد، ورعاية تقويم العظام، وأحيانًا مساعدة نفسية.

