خبير طبي في المقال
منشورات جديدة
علاج الإنتان الحاد والصدمة الإنتانية
آخر مراجعة: 04.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
لا يمكن علاج تعفن الدم بفعالية إلا بالتطهير الجراحي الكامل لمكان العدوى والعلاج المناسب بالمضادات الحيوية. يُعدّ عدم كفاية العلاج الأولي بالمضادات الحيوية عامل خطر للوفاة لدى مرضى تعفن الدم. لا يمكن الحفاظ على حياة المريض، ومنع اختلال وظائف الأعضاء، والقضاء عليها إلا من خلال الرعاية المركزة المُستهدفة.
الهدف الرئيسي منه هو تحسين نقل الأكسجين في ظل زيادة استهلاكه، وهو أمر شائع في حالات الإنتان الشديد والصدمة الإنتانية. يُطبّق هذا العلاج من خلال دعم هيموديناميكي وتنفسي.
دعم الدورة الدموية
العلاج بالتسريب
يُعد العلاج بالتسريب أحد الإجراءات الأولية للحفاظ على ديناميكا الدم، والأهم من ذلك، الحفاظ على النتاج القلبي. وتتمثل مهامه الرئيسية لدى مرضى الإنتان فيما يلي:
- استعادة التروية الكافية للأنسجة،
- تصحيح اضطرابات التوازن الداخلي،
- تطبيع عملية التمثيل الغذائي الخلوي،
- انخفاض في تركيز وسطاء الشلال الإنتاني والمواد الأيضية السامة.
في حالة الإنتان المصحوب بفشل العديد من الأعضاء والصدمة الإنتانية، يحاولون تحقيق القيم التالية للمؤشرات المهمة بسرعة (خلال أول 6 ساعات):
- الهيماتوكريت >30%،
- إدرار البول 0.5 مل/(كجم/ساعة)،
- تشبع الدم في الوريد الأجوف العلوي أو الأذين الأيمن >70%،
- متوسط ضغط الدم >65 ملم زئبق،
- CVP 8-12 ملم زئبق
إن الحفاظ على هذه القيم عند المستوى المحدد يُحسّن بقاء المريض على قيد الحياة (فئة الدليل ب). تُوسّع مراقبة الدورة الدموية باستخدام قسطرة سوان-غانز وتقنية PICCO (التخفيف الحراري عبر الرئة وتحليل موجات النبض) إمكانيات مراقبة وتقييم فعالية العلاج الديناميكي الدموي، ولكن لا يوجد دليل على أنها تُحسّن بقاء المريض على قيد الحياة.
يتم اختيار قيمة التحميل المسبق الأمثل بشكل فردي، إذ من الضروري مراعاة درجة تلف الخلايا البطانية، وحالة التصريف اللمفاوي في الرئتين، والوظيفة الانبساطية للبطينين، وتغيرات الضغط داخل الصدر. ويتم اختيار حجم العلاج بالتسريب بحيث لا يتجاوز ضغط الدم الرئوي (PCWP) ضغط الدم الرئوي في البلازما (للوقاية من اعتلال الكلية الرئوي) مع زيادة في ثاني أكسيد الكربون. بالإضافة إلى ذلك، تُؤخذ في الاعتبار المعايير التي تميز وظيفة تبادل الغازات في الرئتين (paO2 و paO2 / FiO2 ) والتغيرات في الصورة الشعاعية.
في العلاج بالتسريب كجزء من العلاج المستهدف لتسمم الدم والصدمة الإنتانية، يتم استخدام المحاليل البلورية والغروانية مع نتائج متطابقة تقريبًا.
لجميع وسائط التسريب مزايا وعيوب. واليوم، بناءً على نتائج الدراسات التجريبية والسريرية، لا يوجد سبب لتفضيل نوع معين.
- على سبيل المثال، لتصحيح كافٍ لعودة الوريد ومستوى التحميل المسبق، من الضروري إعطاء حجم من البلورات أكبر بمقدار 2-4 مرات من حجم الغرويات، وهو ما يرتبط بخصائص توزيع المحلول في الجسم. بالإضافة إلى ذلك، يرتبط تسريب البلورات بخطر أكبر لوذمة الأنسجة، وتأثيرها الديناميكي الدموي أقصر من تأثير الغرويات. في الوقت نفسه، فإن البلورات أرخص، ولا تؤثر على إمكانية التخثر ولا تثير تفاعلات تأقية. بناءً على ما سبق، يتم تحديد التركيب النوعي لبرنامج التسريب بناءً على خصائص المريض، مع مراعاة درجة نقص حجم الدم، ومرحلة متلازمة DIC، ووجود وذمة محيطية وتركيز الألبومين في مصل الدم، وشدة إصابة الرئة الحادة.
- يُنصح باستخدام بدائل البلازما (دكسترين، مستحضرات الجيلاتين، نشا هيدروكسي إيثيل) في حالات نقص خلايا سرطان الخلايا القاعدية الحاد. تتميز نشويات هيدروكسي إيثيل ذات درجة استبدال 200/0.5، و130/0.4، و130/0.42 بميزة محتملة على الدكسترين نظرًا لانخفاض خطر تسرب الغشاء وعدم وجود تأثير سريري ذي دلالة على وقف النزيف.
- قد يزيد إعطاء الألبومين في الحالات الحرجة من خطر الوفاة. تكون الزيادة في تركيز الألبومين أثناء التسريب مؤقتة، ثم في ظل زيادة نفاذية الأوعية الشعرية (متلازمة "تسرب الشعيرات الدموية")، يحدث تسرب إضافي للألبومين. من الممكن أن يكون نقل الألبومين مفيدًا فقط إذا كان تركيزه في المصل أقل من 20 غ/ل، ولم تظهر أي علامات "تسرب" إلى النسيج الخلالي.
- يُستخدم الكرايوبلازما لعلاج اعتلال تخثر الدم وانخفاض قدرة الدم على التخثر.
- ينبغي الحد من الاستخدام الواسع النطاق لكتلة خلايا الدم الحمراء من المتبرع نظرًا لارتفاع خطر حدوث مضاعفات مختلفة (مثل التهاب الأوعية الدموية النزفية، وردود الفعل التحسسية، وغيرها). ووفقًا لمعظم الخبراء، يتراوح الحد الأدنى لتركيز الهيموجلوبين لدى مرضى الإنتان الشديد بين 90 و100 غم/لتر.
تصحيح انخفاض ضغط الدم
يتطلب انخفاض ضغط التروية تفعيلًا فوريًا للأدوية التي تزيد من توتر الأوعية الدموية و/أو وظيفة التقلص العضلي للقلب. يُعدّ الدوبامين أو النورإبينفرين من الأدوية الأساسية لتصحيح انخفاض ضغط الدم لدى مرضى الصدمة الإنتانية.
يزيد الدوبامين (الدوبمين) بجرعة أقل من 10 ميكروغرام/كجم × دقيقة من ضغط الدم، وذلك أساسًا عن طريق زيادة ثاني أكسيد الكربون، وله تأثير ضئيل على المقاومة الوعائية الجهازية. عند الجرعات العالية، يغلب تأثيره الأدرينالي ألفا، مما يؤدي إلى تضيق الأوعية الدموية الشريانية. أما عند جرعة أقل من 5 ميكروغرام/كجم × دقيقة، فيحفز الدوبامين مستقبلات الدوبامين في الأوعية الكلوية والمساريقية والتاجية، مما يؤدي إلى توسع الأوعية الدموية وزيادة الترشيح الكبيبي وإفراز الصوديوم.
يزيد النورإبينفرين من متوسط ضغط الدم الشرياني ويزيد من ترشيح الكبيبات. يؤدي تحسين ديناميكا الدم الجهازية تحت تأثيره إلى تحسين وظائف الكلى دون الحاجة إلى جرعات منخفضة من الدوبامين. وقد أظهرت دراسات السنوات الأخيرة أن استخدامه بشكل منفرد، مقارنةً بجرعات عالية من الدوبامين، يؤدي إلى انخفاض ملحوظ إحصائيًا في معدل الوفيات.
الأدرينالين دواءٌ أدريناليّ ذو آثار جانبية هيموديناميكية هي الأكثر وضوحًا. يؤثر الأدرينالين، حسب الجرعة، على معدل ضربات القلب، ومتوسط ضغط الدم الشرياني، والنتاج القلبي، ووظيفة البطين الأيسر، وتوصيل الأكسجين واستهلاكه . ومع ذلك، قد يحدث تسرع القلب، وتدهور تدفق الدم في الأعضاء، وفرط لاكتات الدم في آنٍ واحد. لذلك، يقتصر استخدام الأدرينالين على حالات المقاومة التامة للكاتيكولامينات الأخرى.
الدوبوتامين هو الدواء الأمثل لزيادة توصيل واستهلاك أول أكسيد الكربون والأكسجين عند مستويات طبيعية أو مرتفعة. ونظرًا لتأثيره الرئيسي على مستقبلات بيتا-1 الأدرينالية، فهو أكثر فعالية من الدوبامين في زيادة هذه المعايير.
أظهرت الدراسات التجريبية أن الكاتيكولامينات، بالإضافة إلى دعمها للدورة الدموية، يمكنها تنظيم مسار الالتهاب الجهازي من خلال التأثير على تخليق الوسطاء الرئيسيين بتأثير بعيد. تحت تأثير الأدرينالين والدوبامين والنورادرينالين والدوبوتامين، تُقلل الخلايا البلعمية المُنشَّطة من تخليق وإفراز عامل نخر الورم ألفا (TNF-a).
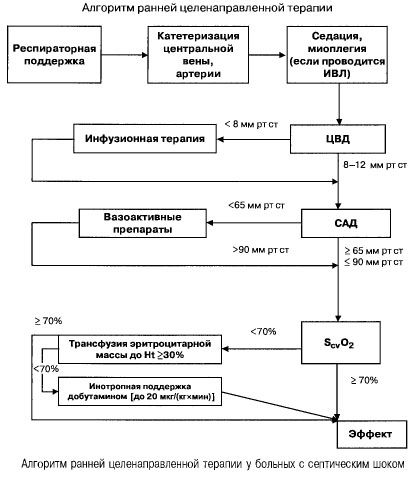
يتم اختيار العوامل الأدرينالية وفقًا للخوارزمية التالية:
- مؤشر القلب 3.5-4 لتر/(الحد الأدنى × م 2 )، SvO 2 >70% - الدوبامين أو النورإبينفرين،
- مؤشر القلب <3.5 لتر/(الدقيقة × م 2 )، SvO 2 <70% - الدوبامين (إذا كان ضغط الدم الانقباضي <70 مم زئبق - مع النورإبينفرين أو الدوبامين).
 [ 1 ]، [ 2 ]، [ 3 ]، [ 4 ]، [ 5 ]، [ 6 ]، [ 7 ]، [ 8 ]
[ 1 ]، [ 2 ]، [ 3 ]، [ 4 ]، [ 5 ]، [ 6 ]، [ 7 ]، [ 8 ]
دعم الجهاز التنفسي
تُعد الرئتان من أوائل الأعضاء المستهدفة في العملية المرضية في حالة الإنتان. يُعد الفشل التنفسي الحاد أحد أهم أسباب اختلال وظائف الأعضاء المتعددة. تتوافق مظاهره السريرية والمخبرية في حالة الإنتان مع الإصابة الحادة بالعدوى، ومع تطور العملية المرضية - متلازمة الضائقة التنفسية الحادة (ARDS). تُحدد مؤشرات التهوية الميكانيكية في حالات الإنتان الشديد بناءً على شدة الفشل التنفسي الحشوي (ARF أو ARDS). معيارها هو مؤشر التنفس:
- <200 - يوصى بالتنبيب الرغامي والدعم التنفسي،
- >200 - يتم تحديد القراءات بشكل فردي.
إذا كان المريض واعيًا أثناء التنفس التلقائي مع دعم الأكسجين، ولم يكن هناك جهد كبير على التنفس وتسارع واضح في القلب (معدل ضربات القلب أقل من ١٢٠ نبضة في الدقيقة)، وكانت القيمة الطبيعية لثاني أكسيد الكبريت العائد الوريدي أكبر من ٩٠٪، فيمكن عندها الامتناع عن نقله إلى جهاز التنفس الاصطناعي. مع ذلك، من الضروري مراقبة حالة المريض بعناية. تبلغ القيمة المثلى لثاني أكسيد الكبريت حوالي ٩٠٪. ويمكن الحفاظ عليها باستخدام طرق مختلفة لتوصيل الغاز (أقنعة الوجه، قسطرة الأنف) بتركيزات غير سامة (FiO2 أقل من ٠.٦). يُمنع استخدام جهاز التنفس الاصطناعي غير الجراحي في حالات الإنتان (الفئة ب).
يجب تجنب التهوية الميكانيكية عالية الحجم (VO = 12 مل/كجم)، إذ يزيد إفراز السيتوكينات من الرئتين في هذه الحالات، مما يؤدي إلى تفاقم حالة MOF. من الضروري الالتزام بمفهوم التهوية الميكانيكية الآمنة، وهو أمر ممكن إذا استوفيت الشروط التالية (فئة الدليل أ):
- DO <10 مل/كجم،
- نسبة غير مقلوبة بين الشهيق والزفير،
- ذروة ضغط مجرى الهواء <35 سم H2O،
- FiO2 <0.6 .
يتم اختيار معلمات دورة التنفس حتى يتم تحقيق التهوية الميكانيكية الكافية، ومعاييرها هي paO2 > 60 مم زئبق، SpO2 > 88-93٪، pvO2 35-45 مم زئبق، SvO2 > 55٪.
من الطرق الفعّالة لتحسين تبادل الغازات إجراء التهوية الاصطناعية في وضعية الانبطاح (الفئة ب). يُعدّ هذا الوضع فعالاً لدى المرضى الذين يعانون من حالات حادة، إلا أن تأثيره في خفض معدل الوفيات على المدى الطويل ضئيل إحصائياً.
الدعم الغذائي
يُعدّ تقديم الدعم الغذائي الاصطناعي عنصرًا هامًا في العلاج، وهو من الإجراءات الإلزامية، إذ عادةً ما يصاحب ظهور متلازمة فشل الأعضاء المتعددة في حالات الإنتان أعراض فرط الأيض. في هذه الحالة، تُلبّى احتياجات الطاقة من خلال تدمير الهياكل الخلوية الذاتية (الأكل الذاتي)، مما يُفاقم خلل وظائف الأعضاء ويزيد من التسمم الداخلي.
يُعتبر الدعم الغذائي وسيلةً للوقاية من الإرهاق الشديد (نقص البروتين والطاقة) في ظلّ زيادة ملحوظة في الإسهال والأيض. يُسهم إدراج التغذية المعوية ضمن العلاج المُكثّف في منع حركة البكتيريا المعوية، وخلل التوازن البكتيري، وزيادة النشاط الوظيفي للخلايا المعوية، وتعزيز الخصائص الوقائية للغشاء المخاطي المعوي. تُقلّل هذه العوامل من درجة التسمم الداخلي وخطر حدوث مضاعفات معدية ثانوية.
حساب الدعم الغذائي:
- القيمة الغذائية - 25-35 سعرة حرارية/(كجم من وزن الجسم × يوم)،
- كمية البروتين - 1.3-2.0 جم / (كجم من وزن الجسم × يوم)،
- كمية الكربوهيدرات (الجلوكوز) - أقل من 6 جم / كجم / يوم،
- كمية الدهون - 0.5-1 جم / كجم / يوم،
- ثنائيات الببتيد الجلوتامين 0.3-0.4 جم/كجم/يوم،
- الفيتامينات - المجموعة اليومية القياسية + فيتامين ك (10 ملغ/يوم) + فيتامينات ب 1 وب 6 (100 ملغ/يوم) + فيتامينات أ، ج، هـ،
- العناصر الدقيقة - المجموعة اليومية القياسية + الزنك (15-20 ملغ/يوم + 10 ملغ/يوم في وجود براز رخو)،
- الإلكتروليتات - Na+، K+، Ca2+ وفقًا لحسابات التوازن والتركيز في البلازما.
إن البدء المبكر بالدعم الغذائي (24-36 ساعة) أكثر فعالية من البدء في اليوم الثالث أو الرابع من العلاج المكثف (فئة الدليل ب)، وخاصة مع التغذية عن طريق الأنبوب المعوي.
في حالات الإنتان الشديد، لا توجد مزايا للتغذية المعوية أو الوريدية؛ فمدة خلل وظائف الأعضاء ومدة الدعم التنفسي والانقباضي متساوية، ومعدلات الوفيات متساوية. بناءً على ما سبق، تُعدّ التغذية المعوية المبكرة بديلاً أقل تكلفة من التغذية الوريدية. كما أن استخدام الخلطات الغنية بالألياف الغذائية (البريبايوتكس) للتغذية الأنبوبية يُقلل بشكل كبير من حدوث الإسهال لدى مرضى الإنتان الشديد.
لتخليق البروتين بفعالية في الجسم، من المهم الحفاظ على نسبة الأيض "النيتروجين الكلي (جم) - السعرات الحرارية غير البروتينية (كيلو كالوري)" = 1-(110-130). الحد الأقصى لجرعة الكربوهيدرات هو 6 جم/كجم من وزن الجسم يوميًا، لأن تناول جرعات كبيرة يُهدد بارتفاع سكر الدم وتنشيط عملية الهدم في العضلات الهيكلية. يُنصح بتناول مستحلبات الدهون على مدار الساعة.
موانع الدعم الغذائي:
- الحماض الأيضي غير المعوض،
- عدم تحمل الفرد لوسائل الدعم الغذائي،
- نقص حجم الدم الشديد غير المتعافى،
- صدمة مقاومة - جرعة الدوبامين >15 ميكروجرام/(كجم × دقيقة) وضغط الدم الانقباضي <90 مم زئبق،
- نقص الأكسجين الشرياني الشديد والمستعصي.
التحكم في نسبة السكر في الدم
من الجوانب المهمة في العلاج المعقد لحالات الإنتان الشديد المراقبة المستمرة لتركيز الجلوكوز في بلازما الدم والعلاج بالأنسولين. يُعد ارتفاع سكر الدم والحاجة إلى تصحيحه من العوامل التي تؤثر سلبًا على نتائج علاج الإنتان. في ظل الظروف المذكورة أعلاه، يُحافظ على مستوى سكر الدم الطبيعي (4.5-6.1 مليمول/لتر) لدى المرضى، وعند ارتفاع تركيز الجلوكوز عن القيم المقبولة، يُحقن المريض بالأنسولين (0.5-1 وحدة/ساعة). وحسب الحالة السريرية، يُراقب تركيز الجلوكوز كل ساعة إلى أربع ساعات. وقد لوحظت زيادة ملحوظة إحصائيًا في بقاء المريض على قيد الحياة عند تطبيق هذه الخوارزمية.
 [ 9 ]، [ 10 ]، [ 11 ]، [ 12 ]، [ 13 ]
[ 9 ]، [ 10 ]، [ 11 ]، [ 12 ]، [ 13 ]
الجلوكوكورتيكويدات
تتلخص نتائج الدراسات الحديثة فيما يتعلق بفعالية استخدام الجلوكوكورتيكويد في المرضى الذين يعانون من الصدمة الإنتانية في العبارات التالية:
- من غير المناسب استخدام الهرمونات بجرعات عالية [ميثيل بريدنيزولون 30-120 ملغ/(كجم × يوم) مرة واحدة أو لمدة 9 أيام، ديكساميثازون 2 ملغ/(كجم × يوم) لمدة يومين، بيتاميثازون 1 ملغ/(كجم × يوم) لمدة 3 أيام] - زيادة خطر الإصابة بعدوى المستشفيات، لا تأثير على البقاء على قيد الحياة،
- يؤدي استخدام الهيدروكورتيزون بجرعة 240-300 ملغ يوميًا لمدة 5-7 أيام إلى تسريع استقرار المعايير الديناميكية الدموية، ويسمح بسحب الدعم الوعائي ويحسن البقاء على قيد الحياة لدى المرضى الذين يعانون من قصور الغدة الكظرية النسبي المصاحب (فئة الأدلة ب).
من الضروري التخلي عن الوصفات التجريبية العشوائية للبريدنيزولون والديكساميثازون - فلا أساس لاستنتاج معلومات جديدة منهما. في حال عدم وجود أدلة مخبرية على قصور كظري نسبي، يُعطى هيدروكورتيزون بجرعة 300 ملغ يوميًا (3-6 حقن).
- في حالة الصدمة المقاومة،
- إذا كانت هناك حاجة لجرعات عالية من المواد الضاغطة للأوعية الدموية للحفاظ على فعالية الديناميكا الدموية.
من المحتمل أن فعالية الهيدروكورتيزون، في حالات الالتهاب الجهازي المصاحب للصدمة الإنتانية، ترتبط بتنشيط مثبط العامل النووي kB (NF-kB-a) وتصحيح قصور الغدة الكظرية النسبي. بدوره، يؤدي تثبيط نشاط العامل النووي النسخي (NF-kB) إلى انخفاض في تكوين إنزيم أكسيد النيتريك القابل للتحريض (NO هو أقوى مُوسِّع للأوعية الدموية داخلي المنشأ)، والسيتوكينات المُحفِّزة للالتهابات، وCOX، وجزيئات الالتصاق.
البروتين المنشط سي
من المظاهر المميزة لتسمم الدم اضطراب التخثر الجهازي (تنشيط سلسلة التخثر وتثبيط انحلال الفيبرين)، مما يؤدي في النهاية إلى نقص التروية وخلل في وظائف الأعضاء. ويتجلى تأثير البروتين C المنشط على الجهاز الالتهابي بعدة طرق:
- تقليل ارتباط السيلكتين بالكريات البيضاء، والذي يحمي بطانة الأوعية الدموية من التلف، والذي يلعب دورًا رئيسيًا في تطور الالتهاب الجهازي،
- انخفاض إطلاق السيتوكينات من الخلايا الوحيدة،
- منع إطلاق TNF-a من الكريات البيضاء،
- تثبيط إنتاج الثرومبين (يعزز الاستجابة الالتهابية).
تأثير مضاد للتخثر ومحلل للبروبرينول ومضاد للالتهابات
- البروتين المنشط C يرجع إلى
- تدهور العوامل Va و VIIIa - قمع تكوين الخثرة،
- تثبيط منشط البلازمينوجين - تنشيط انحلال الفيبرين،
- تأثير مضاد للالتهابات مباشر على الخلايا البطانية والعدلات،
- حماية بطانة الأوعية الدموية من موت الخلايا المبرمج
يُقلل إعطاء بروتين سي المُنشَّط [دروتريكوجين ألفا (مُنشَّط)] بجرعة ٢٤ ميكروغرام/كغ/ساعة لمدة ٩٦ ساعة من خطر الوفاة بنسبة ١٩.٤٪. دواعي الاستعمال: تسمم الدم مع التهاب رئوي حاد وارتفاع خطر الوفاة (APACHE II > ٢٥ نقطة، خلل في وظائف عضوين أو أكثر، فئة الدليل ب).
لا يقلل البروتين C المنشط من معدل الوفيات عند الأطفال، والمرضى الذين يعانون من خلل في عضو واحد، وAPACHE II < 25 نقطة، وفي المرضى الذين يعانون من الإنتان غير الجراحي.
 [ 14 ]، [ 15 ]، [ 16 ]، [ 17 ]
[ 14 ]، [ 15 ]، [ 16 ]، [ 17 ]
الغلوبولينات المناعية
يرتبط إعطاء الغلوبولينات المناعية (IgG وIgG+IgM) عن طريق الوريد بقدرتها على الحد من التأثير المفرط للسيتوكينات المسببة للالتهابات، وزيادة تصفية السموم الداخلية والمستضد الفائق للمكورات العنقودية، والقضاء على الحساسية، وتعزيز تأثير المضادات الحيوية بيتا لاكتام. يُعد استخدامها في علاج الإنتان الشديد والصدمة الإنتانية الطريقة الوحيدة لتصحيح المناعة التي تزيد من معدلات البقاء على قيد الحياة. وقد سُجل أفضل تأثير عند استخدام مزيج من IgG وIgM [RR=0.48 (0.35-0.75)، فئة الدليل A]. يتراوح نظام الجرعات القياسي بين 3-5 مل/كجم × يوم لمدة 3 أيام متتالية. وعند استخدام الغلوبولينات المناعية، تم الحصول على أفضل النتائج في المرحلة المبكرة من الصدمة ("الصدمة الدافئة") ولدى المرضى المصابين بإنتان شديد (درجة APACHE II تتراوح بين 20 و25 نقطة).
الوقاية من تجلط الأوردة العميقة
تؤثر الوقاية من تجلط الأوردة العميقة في الأطراف السفلية بشكل كبير على نتائج العلاج لدى مرضى الإنتان (فئة الدليل أ). ويُستخدم كلٌّ من الهيبارين غير المجزأ والهيبارين منخفض الوزن الجزيئي لهذا الغرض. تتمثل المزايا الرئيسية للهيبارينات منخفضة الوزن الجزيئي في انخفاض معدل حدوث المضاعفات النزفية، وتأثير أضعف على وظيفة الصفائح الدموية، وفعاليتها طويلة الأمد (يمكن إعطاؤها مرة واحدة يوميًا).
الوقاية من تكون قرحة الإجهاد في الجهاز الهضمي
يلعب هذا التوجه دورًا هامًا في تحقيق نتائج إيجابية في علاج المرضى المصابين بتسمم الدم الشديد والصدمة الإنتانية، حيث يتراوح معدل الوفيات بسبب النزيف الناتج عن قرح الإجهاد في الجهاز الهضمي بين 64% و87%. في حال عدم اتخاذ إجراءات وقائية، تُصاب قرح الإجهاد بنسبة 52.8% من المرضى ذوي الحالات الحرجة. ومع ذلك، فإن استخدام مثبطات مضخة البروتون وحاصرات مستقبلات الهيستامين H2 يُقلل من خطر الإصابة بأكثر من الضعف (المجموعة الأولى من الأدوية أكثر فعالية من الثانية). يتمثل التوجه الرئيسي للوقاية والعلاج في الحفاظ على درجة حموضة تتراوح بين 3.5 و6.0. تجدر الإشارة إلى أنه بالإضافة إلى الأدوية المذكورة أعلاه، تلعب التغذية المعوية دورًا هامًا في منع تكوّن قرح الإجهاد.
تنقية الدم خارج الجسم
تُستهدف طرق إزالة السموم العديد من المواد النشطة بيولوجيًا والمنتجات الأيضية التي تُسهم في تطور الالتهاب المعمم، وهو أمر بالغ الأهمية في ظل غياب التصفية الكبدية الكلوية الطبيعية في حالات فشل الأعضاء المتعددة. تُعتبر طرق العلاج ببدائل الكلى واعدة، إذ لا تقتصر فعاليتها على التأثير على الاضطرابات البولية لدى مرضى الفشل الكلوي فحسب، بل تؤثر أيضًا بشكل إيجابي على التغيرات الأخرى في التوازن الداخلي واختلال وظائف الأعضاء التي تحدث في حالات الإنتان والصدمة وفشل الأعضاء المتعددة.
حتى الآن، لا توجد بيانات تؤكد ضرورة استخدام طرق تنقية الدم خارج الجسم كأحد التوجهات الرئيسية للعلاج الممرض لتسمم الدم والصدمة الإنتانية. ويُبرر استخدامها في حالات فشل الأعضاء المتعددة مع هيمنة وظائف الكلى.
 [ 18 ]، [ 19 ]، [ 20 ]، [ 21 ]، [ 22 ]، [ 23 ]
[ 18 ]، [ 19 ]، [ 20 ]، [ 21 ]، [ 22 ]، [ 23 ]
غسيل الكلى
جوهر هذه الطريقة هو نشر مواد ذات وزن جزيئي منخفض (حتى 5x10 3 دالتون) عبر غشاء شبه نافذ، وإزالة السوائل الزائدة من الجسم على طول تدرج الضغط. يُستخدم غسيل الكلى على نطاق واسع لعلاج مرضى الفشل الكلوي المزمن والحاد. يعتمد معدل انتشار المواد بشكل كبير على وزنها الجزيئي. على سبيل المثال، تكون إزالة الببتيدات قليلة التكافؤ أبطأ من تخليقها.
ترشيح الدم
ترشيح الدم هو طريقة فعالة لإزالة المواد ذات الوزن الجزيئي 5x10⁻³ - 5x10⁻³ دالتون ، وهو الطريقة الوحيدة لإزالة مجموعة كبيرة من المواد النشطة بيولوجيًا والمستقلبات من الجسم. تعتمد هذه الطريقة على طريقة الحمل الحراري لنقل الكتلة. بالإضافة إلى التصحيح المناسب لآزوتيمية الدم، يزيل ترشيح الدم بفعالية السموم التحسسية C3a وC5a، والسيتوكينات المسببة للالتهابات (TNF-a، IL-1b، 6 و8)، وΟ2-ميكروغلوبولين، والميوغلوبين، وهرمون الغدة الدرقية، والليزوزيم (الوزن الجزيئي - 6000 دالتون)، وα-أميليز (الوزن الجزيئي - 36000-51000 دالتون)، وفوسفوكيناز الكرياتين، والفوسفاتيز القلوي، وناقلات الأمين، ومواد أخرى. يزيل ترشيح الدم الأحماض الأمينية وبروتينات البلازما (بما في ذلك الغلوبولينات المناعية والمجمعات المناعية المنتشرة).
ترشيح الدم
يُعدّ ترشيح الدم أقوى طرق تنقية الدم، إذ يجمع بين الانتشار والحمل الحراري (أي GD وGF). ويساهم امتصاص المواد المُمرضة على غشاء الفلتر مساهمة إضافية في عملية إزالة السموم.
فصل البلازما
يُعتبر فصل البلازما (تبادل البلازما، ترشيح البلازما) أيضًا طريقةً ممكنةً لتصحيح الالتهاب المعمم لدى مرضى الإنتان والصدمة الإنتانية. وتُعتبر الطريقة الأمثل هي استخدام تبادل البلازما بشكل مستمر مع إزالة 3-5 أحجام من البلازما واستبدالها في الوقت نفسه بمحاليل طازجة مجمدة، وألبومين، وغرواني، وبلوري. مع معامل غربلة 1، يضمن ترشيح البلازما إزالةً جيدةً لبروتين سي التفاعلي، والهابتوغلوبين، وشظية المتمم C3، و1-أنتيتريبسين، والإنترلوكين 6، والثرومبوكسان-B2، وعامل تحفيز الخلايا المحببة، وعامل نخر الورم. يُقلل استخدام المواد الماصة لتنقية بلازما المريض من خطر العدوى ويُقلل من تكلفة الإجراء، نظرًا لعدم الحاجة إلى استخدام بروتينات غريبة.
يؤدي استخدام التسريب المطول من سيلينيت الصوديوم (سيليناز) بجرعة 1000 ميكروجرام / يوم في حالات الإنتان الشديد إلى انخفاض معدل الوفيات.
السيلينيوم عنصر دقيق أساسي، وترتبط أهميته بدوره المحوري في أنظمة مضادات الأكسدة في الخلايا. يبقى مستوى السيلينيوم في الدم ضمن نطاق 1.9-3.17 ميكرومول/لتر. وتتراوح الحاجة اليومية من السيلينيوم بين 50 و200 ميكروغرام، ويعتمد ذلك على توافر مضادات الأكسدة والعناصر الدقيقة الأخرى.
السيلينيوم مضاد أكسدة قوي، وهو أحد مكونات الجلوتاثيون بيروكسيديز، والفوسفولين جلوتاثيون بيروكسيديز، وبعض إنزيمات الأكسدة والاختزال الأخرى، وبعض إنزيمات الترانسفيراز. يُعد الجلوتاثيون بيروكسيديز الحلقة الأهم في نظام مضادات الأكسدة الذاتية.
دُرست فعالية السيلينيوم في الحالات الحرجة في السنوات الأخيرة. وقد أظهرت هذه الدراسات أن آليات عمل السيلينيوم الرئيسية هي:
- قمع فرط نشاط NF-kB؛
- انخفاض تنشيط المكمل؛
- تأثيره كمنظم للمناعة ومضاد للأكسدة ومضاد للالتهابات
- الحفاظ على استخدام بيروكسيد؛
- قمع الالتصاق البطاني (انخفاض التعبير عن ICAM-1 وVCAM-2،
- E- سيلكتيين، P- سيلكتيين)؛
- حماية بطانة الأوعية الدموية من الجذور الحرة (باستخدام سيلينوبروتين P، الذي يمنع تكوين بيروكسينتريت من O2 و NO).
ولتلخيص ما سبق، يمكننا تحديد مهام محددة للعناية المركزة في حالات الإنتان الشديد:
- الدعم الديناميكي الدموي: الضغط الوريدي المركزي 8-12 مم زئبق، متوسط ضغط الدم >65 مم زئبق، إدرار البول 0.5 مل/(كجم/ساعة)، الهيماتوكريت >30%، تشبع الدم الوريدي المختلط >70%.
- دعم الجهاز التنفسي ضغط مجرى الهواء الأقصى <35 سم مكعب من الماء، الكسر الشهيقي للأكسجين <60%، حجم المد والجزر <10 مل/كجم، نسبة الشهيق إلى الزفير غير المقلوبة.
- الجلوكوكورتيكويدات - "جرعات منخفضة" (هيدروكورتيزون 240-300 ملغ يوميا).
- بروتين سي المنشط 24 ميكروجرام/(كجم/ساعة) لمدة 4 أيام في حالات الإنتان الشديد (APACHE II >25).
- العلاج التعويضي لتصحيح المناعة باستخدام البنتاغلوبين.
- الوقاية من تجلط الأوردة العميقة في الأطراف السفلية.
- الوقاية من تشكل قرحة الإجهاد في الجهاز الهضمي: استخدام مثبطات مضخة البروتون وحاصرات مستقبلات الهيستامين H2.
- العلاج البديل للفشل الكلوي الحاد.
- الدعم الغذائي: القيمة الغذائية للطعام 25-30 سعرة حرارية/كجم من وزن الجسم × يوم)، البروتين 1.3-2.0 جم/(كجم من وزن الجسم × يوم)، ثنائيات الببتيد الجلوتامين 0.3-0.4 جم/(كجم × يوم)، الجلوكوز - 30-70% من السعرات الحرارية غير البروتينية، بشرط الحفاظ على نسبة السكر في الدم <6.1 مليمول/لتر، الدهون - 15-50% من السعرات الحرارية غير البروتينية.

