منشورات جديدة
باحثون يحددون الطفرات التي تحمي من سرطان الخلايا البائية
آخر مراجعة: 02.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
تمكن باحثون في المركز الطبي بجامعة تكساس الجنوبية الغربية من قمع سرطان الدم والليمفوما في نموذج الفأر المهيأ وراثيًا لهذه السرطانات عن طريق استنزاف بروتين يسمى ميدولين في الخلايا البائية بشكل كامل أو جزئي.
وقد تؤدي نتائجهم، التي نشرت في مجلة الطب التجريبي ، إلى اكتشاف علاجات جديدة لهذه الأمراض تتجنب الآثار الجانبية الخطيرة للعلاجات الحالية.
وقال الدكتور بروس بويتلر، قائد الدراسة ومدير مركز الدفاع الجيني للمضيف وأستاذ علم المناعة والطب الباطني في المركز الطبي بجامعة تكساس الجنوبية الغربية: "لقد استخدمنا نهجًا وراثيًا بحتًا للعثور على هدف للدواء، وكان هذا الهدف مثيرًا للإعجاب لأن سرطان الدم والليمفوما في الخلايا البائية يعتمدان عليه بشكل كبير، في حين أن معظم أنسجة المضيف لا تعتمد عليه".
لقد استخدم الدكتور بوتلر، الذي فاز بجائزة نوبل في علم وظائف الأعضاء أو الطب في عام 2011 لاكتشافه مجموعة مهمة من مستشعرات مسببات الأمراض المعروفة باسم مستقبلات Toll-like الموجودة على الخلايا المناعية، منذ فترة طويلة الطفرات الجينية - إدخال الطفرات في جينات النماذج الحيوانية عن طريق التعرض لمادة كيميائية تسمى N-ethyl-N-nitrosourea (ENU) - كأداة رئيسية لدراسة وظيفة الجينات.
في الآونة الأخيرة، قام مختبر بويتلر بتطوير طريقة تعرف باسم رسم الخرائط الانقسامية الآلية (AMM)، والتي تتتبع السمات غير العادية في الفئران المتحولة إلى الطفرات المسببة، وبالتالي تحديد الجينات اللازمة للحفاظ على الحالة الفسيولوجية الطبيعية.
غالبًا ما تُسبب الطفرات الجينية أمراضًا وراثية لدى الحيوانات، مما يُتيح فهمًا أعمق لوظيفة الجينات المُصابة من خلال دراسة التشوهات في الحيوانات. ومع ذلك، وكما أوضح الدكتور بوتلر، يُمكن للطفرات أيضًا أن تُوفر الحماية من الأمراض.
من الأمثلة على ذلك الطفرات التي تحمي المصابين بفيروس نقص المناعة البشرية أو مرض فقر الدم المنجلي الوراثي من ظهور أعراض المرض. وقد ألهمت الآليات الكامنة وراء بعض الطفرات الوقائية تطوير أدوية لعلاج مجموعة متنوعة من الأمراض.
في بحثهم عن طفرات وقائية لاضطرابات المناعة، فحص الباحثون فئرانًا متحولة بحثًا عن خلايا مناعية ذات خصائص غير عادية. في عدة مجموعات من الحيوانات ذات أعداد منخفضة بشكل غير عادي من الخلايا البائية - وهي مكون مهم في الجهاز المناعي التكيفي المسؤول عن إنتاج الأجسام المضادة - استخدم الباحثون AMM لتتبع النقص إلى طفرات في ميدنولين، وهو بروتين موجود بشكل أساسي في الخلايا البائية.
وعلى الرغم من أن الحيوانات التي تفتقر إلى الميدولين بشكل كامل تموت أثناء النمو قبل الولادة، فإن الطفرات الأخف، بما في ذلك بعض الطفرات التي يتم إدخالها من خلال التقنيات الجينية التي تسمح بحذف الجين في مرحلة البلوغ، لا تسبب أي ضرر واضح.
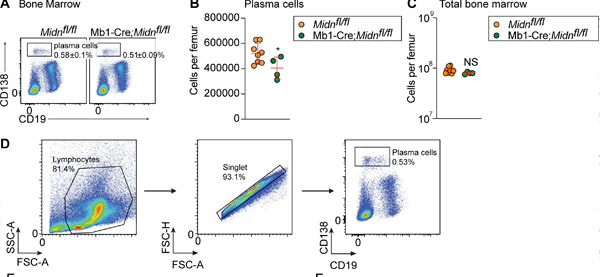
إنتاج خلايا البلازما بعد التطعيم بمستضد TD بيتا-غالاكتوزيداز في فئران Mb1-Cre؛Midn fl/fl. (أ و ب) رسوم بيانية تمثيلية لقياس التدفق الخلوي (أ) وأعداد (ب) لخلايا البلازما في نخاع العظم لفئران Mb1-Cre؛Midn fl/fl وMidn fl/fl بعمر 8 أسابيع بعد التطعيم بمستضد TD بيتا-غالاكتوزيداز. (ج) إجمالي خلايا نخاع العظم لكل عظمة فخذ. (د) استراتيجية عزل خلايا البلازما. المصدر: مجلة الطب التجريبي (2024). DOI: 10.1084/jem.20232132
قام الباحثون بخفض أو إزالة الميدولين بشكل ملحوظ لدى الفئران المُهيأة وراثيًا لسرطان الدم والليمفوما البائية، وهما سرطانان تنقسم فيهما الخلايا البائية بشكل لا يمكن السيطرة عليه. على الرغم من أن الفئران ذات المستويات الطبيعية من الميدولين ماتت بسبب هذه الأمراض بعد خمسة أشهر، إلا أن معظم الفئران التي كانت مستويات الميدولين لديها أقل أو معدومة لم تُصب بأورام خبيثة.
أظهرت تجارب إضافية أن دور الميدولين في الخلايا البائية هو تحفيز نشاط البروتيازومات، وهي عضيات خلوية تتخلص من البروتينات التالفة أو التي لم تعد ضرورية. وأوضح الدكتور بوتلر أن بعض العلاجات المستخدمة حاليًا لعلاج سرطان الدم والليمفوما في الخلايا البائية تعمل عن طريق تثبيط نشاط البروتيازوم، تمامًا كما تفعل إزالة الميدولين.
ومع ذلك، وعلى عكس هذه الأدوية، التي لها العديد من الآثار الجانبية الخطيرة المحتملة، فإن إزالة أو تقليل الميدنولولين في النماذج الحيوانية لم يظهر أي آثار سلبية.
وسوف تركز الأبحاث المستقبلية على تطوير الأدوية التي تمنع الميدولين، والتي قد تشكل في نهاية المطاف الأساس لعلاجات جديدة لسرطانات الخلايا البائية.
