منشورات جديدة
لماذا لا تصل نسبة بقاء الخلايا المستقبلة للضوء إلى 100%: توضيح الآليات الرئيسية
آخر مراجعة: 09.08.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
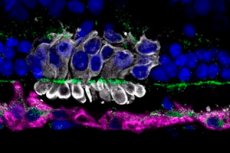
اكتشف علماء من جامعة بنسلفانيا، بقيادة راغافي سودارسان، سبب موت حوالي 70% من الخلايا السلفية الحسية الضوئية المزروعة من الخلايا الجذعية متعددة القدرات المستحثة خلال الأيام القليلة الأولى بعد زرعها في شبكية العين. ويشير بحثهم، المنشور في مجلة أبحاث الخلايا الجذعية والعلاج ، إلى أن الإجهاد الأيضي في خلايا المتبرع هو السبب الرئيسي وراء هذا الفقد المبكر.
المتطلبات الأساسية
تُعتبر زراعة خلايا PRPCs نهجًا واعدًا لعلاج أمراض الشبكية التنكسية المتقدمة (التهاب الشبكية الصباغي، والتنكس البقعي). إلا أن انخفاض معدل بقاء الخلايا المتبرع بها يحد من فعالية العلاج. حتى الآن، كان التركيز الرئيسي منصبًا على تثبيط الاستجابة المناعية، ولكن حتى مع تثبيط المناعة بشكل مكثف، ظلت الخسائر كارثية.
التصميم والأساليب
النماذج:
تم حقن الكلاب السليمة والكلاب النموذجية المصابة بالتهاب الشبكية الصباغي تحت الشبكية بـ PRPCs المصبوغة بالفلورسنت.
تقدير البقاء على قيد الحياة:
تم تسجيل حجم الخلايا المزروعة باستخدام تصوير الأوعية الدموية بالفلوريسين والتصوير المقطعي البصري (OCT) في اليوم الأول، وفي اليوم الثالث، وفي اليوم السابع.
تحليل النسخ الجيني للخلية الواحدة (scRNA-seq):
تم عزل PRPCs من مواقع الشبكية في اليوم الثالث وتم تحليل التعبير عن الجينات المرتبطة بالتمثيل الغذائي والاستماتة.
المناعة الكيميائية:
تم تقييم علامات الإجهاد التأكسدي (4-HNE)، وحالة الميتوكوندريا (Tom20)، وتنشيط الخلايا الدبقية الصغيرة (Iba1) في منطقة الزرع.
النتائج الرئيسية
- فقدان الخلايا الهائل: اختفى ما يقرب من 70% من خلايا PRPCs بحلول اليوم السابع في كل من شبكية العين السليمة والمتدهورة على الرغم من تثبيط المناعة.
- الإجهاد الأيضي: أظهر scRNA-seq انخفاضًا كبيرًا في التعبير عن جينات الفسفرة التأكسدية (CYCS، COX4I1) وزيادة في نسخ العلامات المسببة للموت الخلوي (BAX، CASP3).
- خلل الميتوكوندريا: أظهرت المناعة الكيميائية تجزئة وفقدان وسم Tom20 في خلايا PRPCs المزروعة، كما أشارت مستويات 4-HNE المرتفعة إلى الضرر التأكسدي.
- دور الخلايا الدبقية الصغيرة: في منطقة الزرع، زاد نشاط الخلايا الدبقية الصغيرة Iba1⁺ استجابة لموت PRPCs، مما قد يؤدي إلى تفاقم الالتهاب الموضعي ويساهم في المزيد من الخسائر.
التأثيرات على علاجات الخلايا
تُغيّر هذه النتائج المفهوم السائد: لزيادة زراعة خلايا PRPCs، لا يقتصر الأمر على تثبيط الاستجابة المناعية فحسب، بل يشمل أيضًا دعم استقلاب الطاقة في خلايا المتبرع. التدخلات الممكنة:
- "التدريب الأيضي الأولي" لخلايا PRPCs في ظل ظروف الثقافة الطبيعية على حافة التحميل تحت الضغط لتعزيز مرونتها الميتوكوندريا.
- كوكتيلات من مثبتات الميتوكوندريا (أنزيم Q₁₀، الكارنيتين) أثناء وبعد عملية الزرع مباشرة.
- تعديل البيئة الشبكية المحلية: توصيل مضادات الأكسدة أو حماة الميتوكوندريا إلى منطقة الزرع.
الاستنتاجات والآفاق العملية
- التكييف الأيضي المسبق: تكييف خلايا PRPCs تحت ظروف الإجهاد الأيضي الخفيف قبل عملية الزرع لتعزيز مرونتها.
- التسليم باستخدام السقالة: استخدام مصفوفات قابلة للتحلل البيولوجي والتي تضمن الانتقال التدريجي للخلايا المانحة من وسط ثقافي غني إلى البيئة الشبكية.
- الدعم الغذائي: توصيل مضادات الأكسدة أو ركائز التنفس الميتوكوندريا بالاشتراك مع PRPCs.
"لقد كنا نحارب منذ فترة طويلة الحاجز المناعي فقط، ولكن من الواضح الآن أنه بدون حل مشكلة الصدمة الأيضية، فإن عمليات زرع الأعضاء محكوم عليها بالموت المبكر"، يختتم راغافي سودارسان.
ويمهد هذا العمل، الذي يدعمه المعهد الوطني للعيون، الطريق أمام المزيد من العلاجات الخلوية القابلة للتطبيق لاستعادة الرؤية لدى المرضى الذين يعانون من أمراض الشبكية التنكسية.
