تسلط الدراسة الضوء على الحاجة إلى علاجات خاصة بنوع الخلية لفيروس نقص المناعة البشرية
آخر مراجعة: 14.06.2024

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
أثبت باحثون من جامعة إلينوي أهمية استهداف أنواع معينة من الخلايا في علاج فيروس نقص المناعة البشرية. دراستهم، المنشورة في وقائع الأكاديمية الوطنية للعلوم، هي واحدة من أولى الدراسات التي فحصت التأثيرات التفاضلية أو الخاصة بنوع الخلية لتعديل زمن انتقال فيروس نقص المناعة البشرية على الخلايا النقوية.. الخلايا، وهي نوع من الخلايا المناعية يتم إنتاجها في نخاع العظم.
تتمثل إحدى العوائق الرئيسية أمام القضاء على العدوى بفيروس نقص المناعة البشرية في إدارة الكمون، أو الفترة التي تكون فيها الخلية المصابة في حالة سبات ولا يمكنها إنتاج الفيروس. تتجمع خلايا فيروس نقص المناعة البشرية الكامنة في الجسم في أماكن تعرف باسم الخزانات. تمثل الخزانات الكامنة مشكلة لأنها يمكن أن تبدأ في إنتاج الفيروس في أي لحظة.
يتطلب الاستئصال الكامل للمرض إزالة جميع الخلايا الكامنة من الجسم أو المقاومة الدائمة لمحفزات التنشيط. ومع ذلك، يمكن أن تحدث إعادة التنشيط بسبب مجموعة متنوعة من العوامل، بما في ذلك الإشارات التي توجه تمايز الخلايا النقوية.
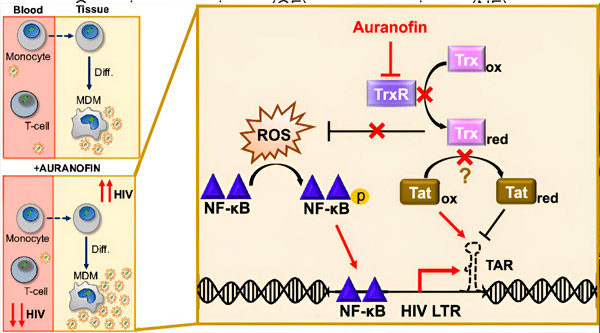
إن تنظيم زمن انتقال فيروس نقص المناعة البشرية في الخلايا البلعمية المشتقة من الخلايا الوحيدة (MDMs) قد يشكل خطرًا لانتشار الفيروس. يمكن أن يؤدي تمايز الخلايا الوحيدة إلى بلاعم إلى إعادة تنشيط فيروس نقص المناعة البشرية، مما قد يؤدي إلى تعزيز انتشار الفيروس في الأنسجة (أعلى اليسار). يقلل المرشح السريري، أورانوفين، الحمض النووي الفيروسي في الدم ويعزز كمون فيروس نقص المناعة البشرية في الخلايا التائية وحيدات الخلية، ولكنه يسبب إعادة تنشيط فيروس نقص المناعة البشرية في MDM (أسفل اليسار). في MDM، نفترض أن تثبيط TrxR بواسطة Auranofin يؤدي إلى تراكم أنواع الأكسجين التفاعلية (ROS)، مما يسبب تنشيط NF-andB وتفعيل مروج فيروس نقص المناعة البشرية LTR (يمين). من المحتمل أن يؤدي تثبيط TrxR إلى تقليل تقليل الركيزة عن طريق السماح لبروتين Tat بالبقاء مؤكسدًا في الغالب، حيث يمكن أن يرتبط بـ TAR ويبدأ نسخ فيروس نقص المناعة البشرية. المصدر: وقائع الأكاديمية الوطنية للعلوم (2024). دوى: 10.1073/pnas.2313823121
لسنوات عديدة، تمحورت الأبحاث حول علاج فيروس نقص المناعة البشرية حول أسلوبين معروفين باسم "الصدمة والقتل" و"الحظر والقفل". يعمل الأول جنبًا إلى جنب مع العلاج المضاد للفيروسات القهقرية لتنشيط الخلايا المصابة بالعدوى الكامنة وقتلها من خلال موت الخلايا المبرمج، أو موت الخلايا المبرمج، بينما يتسبب الأخير في دخول الخلايا المصابة إلى حالة كامنة عميقة لا يمكنها إعادة تنشيطها من تلقاء نفسها.
ركزت الأبحاث حول هذه التقنيات تقليديًا على نوع من خلايا الدم البيضاء تسمى الخلايا التائية، والتي تعد الهدف الرئيسي للإصابة بفيروس نقص المناعة البشرية. ومع ذلك، لا تتكون الخزانات الكامنة من الخلايا التائية فقط؛ في الواقع، فهي تحتوي على العشرات من أنواع الخلايا المختلفة، ولكل منها أنماط فريدة خاصة بها من التعبير الجيني لفيروس نقص المناعة البشرية.
وقال كولين كيفير، الأستاذ المساعد في علم الأحياء الدقيقة ومؤلف الدراسة: "هناك تنوع كبير في الخلايا، حتى داخل سلالة واحدة". "يزداد التباين في الاستجابة في هذه الخزانات مع كل نوع جديد من الخلايا."
أرادت ألكسندرا بلانكو، وهي طالبة دراسات عليا في مختبر كيفير، دراسة أنواع الخلايا التي لم يتم اكتشافها في أبحاث فيروس نقص المناعة البشرية التقليدية. بالتركيز على الخلايا النقوية، أنشأت مكتبة مستنسخة تحتوي على 70 مجموعة من الخلايا الوحيدات المصابة بالعدوى الكامنة. ثم قام بلانكو بتحليل المجموعات النسيلية واستجاباتها للتنشيط. وتباينت الإجابات بشكل كبير، مما سلط الضوء على التنوع الكبير داخل نوع الخلية الواحدة.
تثير هذه الملاحظة سؤالًا جديدًا: هل تظهر أنواع الخلايا المختلفة بالفعل استجابات مختلفة لعلاجات زمن انتقال فيروس نقص المناعة البشرية؟ في الواقع، أظهرت نتائج دراستهم أن بعض علاجات الكمون المضادة لفيروس نقص المناعة البشرية يمكن أن تعزز الكمون في الخلايا التائية والخلايا الوحيدة، بينما في البلاعم يمكنها عكس الكمون.
"ليست كل الخلايا في الجسم متشابهة"، قال كيففر. "لذا فمن المنطقي ألا تستجيب جميع الخلايا المصابة للفيروس بنفس الطريقة".
تسلط ورقتهم الضوء على ضرورة أن تأخذ علاجات فيروس نقص المناعة البشرية المستقبلية في الاعتبار جميع أنواع الخلايا وكيف يمكن أن تستجيب كل خلية للعلاجات المحتملة.
تستند النتائج التي توصلوا إليها إلى بحث أجراه روي دار، أستاذ الهندسة الحيوية السابق في إلينوي والذي قام مختبره بدراسة عدم التجانس في التعبير الجيني لفيروس نقص المناعة البشرية.
وقال كيفر: "لقد بدأ الأمر واستلمناه وأوصلناه إلى ما هو عليه الآن". "وبالتالي فإن التعاون أدى بالفعل إلى هذه النتائج. لقد تحول إلى اتجاه جديد لمختبرنا، ونحن متحمسون جدًا لذلك."كشفت نتيجة إضافية وغير متوقعة من تحليل بلانكو عن تغيرات في حجم الخلية وشكلها استجابة للعدوى، مما يشير إلى أن فيروس نقص المناعة البشرية قد يغير شكل الخلية. هدف بلانكو التالي هو تحديد الآليات البيولوجية الكامنة وراء هذه التغيرات المظهرية.
يتطلع كيفير وأعضاء مختبره أيضًا إلى تكرار نتائجهم، والتي تم إجراؤها إلى حد كبير على خط الخلية، في الخلايا الأولية. وأوضح كيفر أن تكرار النتائج في نموذج أكثر شبهاً بالإنسان من شأنه أن يحسن الأهمية السريرية للدراسة.
وقال بلانكو: "نود إجراء فحوصات أكبر على الخلايا التائية والخلايا الوحيدة والبلاعم لتحديد الأدوية المحتملة التي يمكن أن تعمل في جميع أنواع الخلايا هذه". "يمكننا العثور على المزيد من الجزيئات التي لا تتصرف بطريقة محددة لنوع الخلية."
