منشورات جديدة
نظام الحلقة المغلقة لتوصيل الدواء يمكن أن يحسن من توصيل العلاج الكيميائي
آخر مراجعة: 02.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
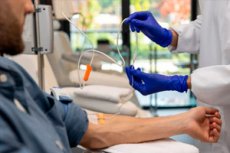
عندما يخضع مرضى السرطان للعلاج الكيميائي، تُحسب جرعات معظم الأدوية بناءً على مساحة سطح جسم المريض. ويُقدَّر ذلك باستخدام معادلة تأخذ في الاعتبار طول المريض ووزنه. وُضعت هذه المعادلة عام ١٩١٦ بناءً على بيانات من تسعة مرضى فقط.
هذا النهج المُبسَّط للجرعات لا يأخذ في الاعتبار عوامل أخرى، وقد يؤدي إلى إعطاء المريض جرعة زائدة أو قليلة جدًا من الدواء. نتيجةً لذلك، قد يُعاني بعض المرضى من سُمِّية غير ضرورية أو فعالية غير كافية للعلاج الكيميائي الذي يتلقونه.
لتحسين دقة جرعات العلاج الكيميائي، طوّر مهندسو معهد ماساتشوستس للتكنولوجيا (MIT) نهجًا بديلًا يسمح بتخصيص الجرعة لكل مريض. يقيس نظامهم كمية الدواء في جسم المريض، ويُدخل هذه البيانات إلى وحدة تحكم تُعدّل معدل التسريب وفقًا لذلك.
ويقول الباحثون إن هذا النهج قد يساعد في تعويض الاختلافات في الحركية الدوائية الناجمة عن تكوين الجسم، والاستعداد الوراثي، والسمية العضوية الناجمة عن العلاج الكيميائي، والتفاعلات مع الأدوية الأخرى والأطعمة، والاختلافات اليومية في الإنزيمات المسؤولة عن تكسير أدوية العلاج الكيميائي.
وقال جيوفاني ترافيرسو، أستاذ مشارك في الهندسة الميكانيكية في معهد ماساتشوستس للتكنولوجيا، وأخصائي أمراض الجهاز الهضمي في مستشفى بريغهام والنساء، والمؤلف الرئيسي للدراسة: "من خلال الاعتراف بالتقدم في فهم كيفية استقلاب الأدوية وتطبيق الأدوات الهندسية لتبسيط الجرعات الشخصية، نعتقد أنه يمكننا المساعدة في تحويل سلامة وفعالية العديد من الأدوية".
لويس دي ريدر، طالب دراسات عليا في معهد ماساتشوستس للتكنولوجيا، هو المؤلف الرئيسي للورقة البحثية المنشورة في مجلة Med.
المراقبة المستمرة
في هذه الدراسة، ركز الباحثون على دواء يُسمى 5-فلورويوراسيل ، ويُستخدم لعلاج سرطان القولون والمستقيم وأنواع أخرى من السرطان. يُعطى الدواء عادةً على مدار 46 ساعة، وتُحدد جرعته باستخدام صيغة تعتمد على طول المريض ووزنه، والتي تُعطي تقديرًا لمساحة سطح الجسم.
مع ذلك، لا يأخذ هذا النهج في الاعتبار اختلافات تركيب الجسم التي قد تؤثر على توزيع الدواء في الجسم، أو الاختلافات الجينية التي تؤثر على استقلابه. قد تؤدي هذه الاختلافات إلى آثار جانبية ضارة في حال إعطاء جرعة زائدة من الدواء. وإذا لم تُعطَ جرعة كافية، فقد لا يقضي الدواء على الورم كما هو متوقع.
يقول دي ريدر، وهو مرشح للحصول على درجة الدكتوراه في برنامج الهندسة الطبية والفيزياء الطبية في برنامج هارفارد-معهد ماساتشوستس للتكنولوجيا في العلوم الصحية والتكنولوجيا: "يمكن للأشخاص الذين لديهم نفس مساحة سطح الجسم أن يكون لديهم أطوال وأوزان مختلفة للغاية، أو كتلة عضلية مختلفة، أو جينات مختلفة، ولكن طالما أن الطول والوزن المدخلين في هذه المعادلة يعطيان نفس مساحة سطح الجسم، فإن جرعتهم متطابقة".
هناك عامل آخر يُمكن أن يُغير كمية الدواء في الدم في أي وقت، وهو الاختلاف اليومي في إنزيم يُسمى ديهيدروبيريميدين ديهيدروجينيز (DPD)، والذي يُحلل 5-فلورويوراسيل. يُنظم التعبير عن DPD، كغيره من الإنزيمات في الجسم، من خلال إيقاع يومي. وبالتالي، فإن تحلل 5-فلورويوراسيل بواسطة DPD ليس ثابتًا، بل يتغير باختلاف الوقت من اليوم. يُمكن أن تُؤدي هذه الإيقاعات اليومية إلى تباين عشرة أضعاف في كمية 5-فلورويوراسيل في دم المريض أثناء التسريب.
باستخدام مساحة سطح الجسم لحساب جرعة العلاج الكيميائي، نعلم أن سمية 5-فلورويوراسيل قد تختلف اختلافًا كبيرًا بين شخصين. قد يخضع مريض لدورات علاجية بسمية ضئيلة، ثم لدورة أخرى بسمية شديدة. لقد تغير شيء ما في طريقة استقلاب المريض للعلاج الكيميائي من دورة لأخرى. لا تلتقط طريقة الجرعات القديمة هذه التغييرات، مما يؤدي إلى معاناة المرضى، كما يقول دوغلاس روبنسون، أخصائي الأورام السريرية في معهد دانا فاربر للسرطان ومؤلف الدراسة.
إحدى طرق تعويض التباين في الحرائك الدوائية للعلاج الكيميائي هي استراتيجية تُسمى مراقبة الأدوية العلاجية، حيث يُعطي المريض عينة دم في نهاية دورة العلاج. بعد تحليل هذه العينة لتحديد تركيزات الدواء، يُمكن تعديل الجرعة، عند الضرورة، في بداية الدورة التالية (عادةً ما تكون أسبوعين لـ 5-فلورويوراسيل).
وقد ثبت أن هذا النهج يؤدي إلى نتائج أفضل للمرضى، ولكن لم يتم استخدامه على نطاق واسع في العلاجات الكيميائية مثل 5-فلورويوراسيل.
أراد باحثو معهد ماساتشوستس للتكنولوجيا تطوير نوع مماثل من المراقبة، ولكن بطريقة آلية تسمح بتخصيص جرعات الأدوية في الوقت الحقيقي، مما قد يؤدي إلى نتائج أفضل للمرضى.
في نظام الحلقة المغلقة، يمكن مراقبة تركيزات الأدوية بشكل مستمر ويتم استخدام هذه المعلومات لضبط معدل ضخ دواء العلاج الكيميائي تلقائيًا للحفاظ على الجرعة ضمن النطاق المستهدف.
يتيح هذا النظام ذو الحلقة المغلقة تخصيص جرعات الأدوية مع الأخذ في الاعتبار الإيقاعات اليومية لمستويات إنزيمات استقلاب الدواء، بالإضافة إلى أي تغييرات في الحركية الدوائية للمريض منذ العلاج الأخير، مثل السمية العضوية الناجمة عن العلاج الكيميائي.
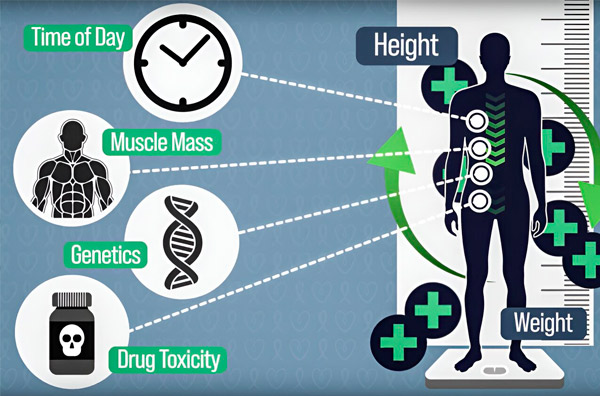
لزيادة دقة جرعات العلاج الكيميائي، طوّر مهندسو معهد ماساتشوستس للتكنولوجيا (MIT) طريقةً لقياس كمية الدواء في جسم المريض باستمرار خلال عملية تسريب تستغرق ساعات. سيساعد هذا في تعويض الاختلافات الناتجة عن تركيب الجسم، والجينات، وسمية الدواء، والتقلبات اليومية. المصدر: بإذن من الباحثين.
يستخدم النظام الجديد الذي طوره الباحثون، والمعروف باسم CLAUDIA (منظم التسريب الدوائي الآلي ذو الحلقة المغلقة)، معدات متوفرة تجاريًا في كل خطوة. تُؤخذ عينات الدم كل خمس دقائق وتُجهّز سريعًا للتحليل. يُقاس تركيز 5-فلورويوراسيل في الدم ويُقارن بالنطاق المستهدف.
يتم إدخال الفرق بين التركيزات المستهدفة والتركيزات المقاسة في خوارزمية التحكم، والتي تقوم بعد ذلك بضبط معدل التسريب حسب الضرورة للحفاظ على الجرعة ضمن نطاق التركيزات التي يكون فيها الدواء فعالاً وغير سام.
ويقول ديريدر: "لقد قمنا بتطوير نظام يمكننا من خلاله قياس تركيز الدواء بشكل مستمر وضبط معدل التسريب وفقًا لذلك للحفاظ على تركيز الدواء ضمن النافذة العلاجية".
تعديل سريع
وفي الاختبارات التي أجريت على الحيوانات، وجد الباحثون أنه باستخدام CLAUDIA، يمكنهم الحفاظ على كمية الدواء المتداولة في الجسم ضمن النطاق المستهدف بنسبة 45 في المائة من الوقت.
في المتوسط، بقيت مستويات الدواء في الحيوانات التي خضعت للعلاج الكيميائي دون استخدام عقار كلوديا ضمن النطاق المستهدف بنسبة 13% فقط. لم يختبر الباحثون فعالية مستويات الدواء في هذه الدراسة، ولكن يُعتقد أن الحفاظ على التركيزات ضمن النطاق المستهدف يُؤدي إلى نتائج أفضل وأقل سمية.
تمكنت كلوديا أيضًا من الحفاظ على جرعة 5-فلورويوراسيل ضمن النطاق المستهدف حتى عند إعطاء دواء يثبط إنزيم DPD. في الحيوانات التي أُعطيت هذا المثبط دون مراقبة وتعديل مستمرين، ارتفعت مستويات 5-فلورويوراسيل حتى ثمانية أضعاف.
وفي هذا العرض التوضيحي، قام الباحثون بتنفيذ كل خطوة من خطوات العملية يدويًا باستخدام معدات جاهزة، ولكنهم يخططون الآن لأتمتة كل خطوة بحيث يمكن إجراء المراقبة وتعديل الجرعة دون تدخل بشري.
ولقياس تركيزات الأدوية، استخدم الباحثون تقنية كروماتوغرافيا السائل عالية الأداء-مطياف الكتلة (HPLC-MS)، وهي تقنية يمكن تكييفها للكشف عن أي نوع من أنواع الأدوية تقريبًا.
يقول ديريدر: "نرى مستقبلًا حيث يمكننا استخدام CLAUDIA لأي دواء يتمتع بخصائص الحركية الدوائية المناسبة ويمكن اكتشافه بواسطة HPLC-MS، مما يسمح بجرعات شخصية للعديد من الأدوية المختلفة".
