منشورات جديدة
جرد العلماء خلايا سرطان الدماغ من قدرتها على البقاء على قيد الحياة بطريقة جديدة
آخر مراجعة: 02.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
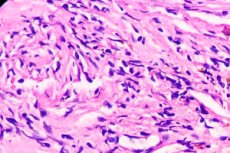
عند إيقاف مكابح سيارة سباق، تتحطم بسرعة. يسعى الدكتور باراك روتبلات إلى تجربة مشابهة مع خلايا سرطان الدماغ: إيقاف قدرتها على البقاء عند نفاد الجلوكوز. ويهدف إلى تسريع نمو خلايا الورم لتموت بنفس السرعة. ويستند هذا النهج الجديد لعلاج سرطان الدماغ إلى عقد من الأبحاث في مختبره.
اكتشافات جديدة
نشر الدكتور روتبلات وطلابه والباحث المشارك غابرييل ليبريفير من معهد أمراض الأعصاب في مستشفى جامعة دوسلدورف نتائجهم الأسبوع الماضي في مجلة Nature Communications.
حتى الآن، كان يُعتقد أن الخلايا السرطانية تهدف أساسًا إلى النمو والتكاثر السريع. ومع ذلك، فقد تبيّن أن الأورام تحتوي على نسبة غلوكوز أقل من الأنسجة الطبيعية.
إذا كانت الخلايا السرطانية مُركّزة كليًا على التكاثر السريع، فمن المفترض أن تعتمد على الجلوكوز أكثر من الخلايا الطبيعية. ولكن، ماذا لو كانت أولويتها القصوى هي البقاء، وليس النمو المُتسارع؟ إذًا، فإن تحفيز النمو عند نقص الجلوكوز قد يُؤدي إلى نفاد طاقة الخلية وموتها.
آفاق الطب الشخصي
يوضح الدكتور روتبلات: "هذا اكتشافٌ مثيرٌ حققناه بعد عقدٍ من البحث. يُمكننا استهداف الخلايا السرطانية حصريًا دون التأثير على الخلايا السليمة، مما سيُمثل خطوةً مهمةً نحو الطب المُخصص والعلاجات التي تتجاوز الخلايا السليمة كما يفعل العلاج الكيميائي والإشعاعي".
ويضيف: "إن اكتشافنا لنقص الجلوكوز ودور مضادات الأكسدة يفتح آفاقًا علاجية لتطوير جزيء قد يعالج الورم الدبقي (سرطان الدماغ)". ويمكن تطبيق هذا العامل العلاجي أيضًا على أنواع أخرى من السرطان.
البحث ونتائجه
بدأ روتبلات وطلابه، الدكتور تال ليفي والدكتورة حولا الأسد، بدراسة أن الخلايا تنظم نموها بناءً على الطاقة المتاحة. فعندما تكون الطاقة وفيرة، تُراكم الخلايا الدهون وتُنتج كميات كبيرة من البروتينات لتخزين الطاقة والنمو. أما عندما تكون الطاقة محدودة، فيجب على الخلايا إيقاف هذه العملية لتجنب نفادها.
عادةً ما تكون الأورام في حالة نقص حاد في الجلوكوز. وقد بدأ الباحثون بالبحث عن مكابح جزيئية تُمكّن الخلايا السرطانية من البقاء على قيد الحياة في ظل نقص الجلوكوز. إذا أمكن إيقاف هذه المكابح، سيموت الورم، بينما تبقى الخلايا الطبيعية غير المحرومة من الجلوكوز سليمة.
مسار MTOR ودور 4EBP1
درس روتبلات وفريقه مسار mTOR (هدف الثدييات للراباميسين)، المزود ببروتينات تقيس حالة طاقة الخلية وتنظم نموها. ووجدوا أن بروتينًا في مسار mTOR يُعرف باسم 4EBP1، والذي يثبط تخليق البروتين عند انخفاض مستويات الطاقة، ضروري لبقاء خلايا الإنسان والفئران، وحتى خلايا الخميرة، عند نقص الجلوكوز.
أثبتوا أن 4EBP1 يقوم بذلك عن طريق التنظيم السلبي لمستويات إنزيم رئيسي في مسار تخليق الأحماض الدهنية، وهو ACC1. تستخدم الخلايا السرطانية، وخاصة خلايا سرطان الدماغ، هذه الآلية للبقاء في أنسجة الورم وتكوين أورام عدوانية.
تطوير علاج جديد
ويعمل الدكتور روتبلات الآن مع شركة BGN Technologies والمعهد الوطني للتكنولوجيا الحيوية في النقب لتطوير جزيء من شأنه أن يمنع 4EBP1، مما يتسبب في استمرار الخلايا السرطانية التي تعاني من نقص الجلوكوز في تصنيع الدهون واستنزاف مواردها عندما يتم استنفاد الجلوكوز.
