منشورات جديدة
لقد أظهر علاج الورم الأرومي الدبقي نتائج مشجعة
آخر مراجعة: 03.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
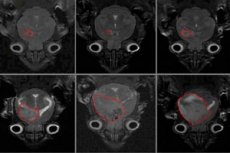
اكتشف باحثون في مركز ميموريال سلون كيترينج للسرطان جزيئًا صغيرًا يُسمى غليوسيدين، يقضي على خلايا الورم الأرومي الدبقي دون الإضرار بالخلايا السليمة. قد يُقدم هذا الاكتشاف نهجًا علاجيًا جديدًا لعلاج هذا الورم الدماغي العدواني.
لماذا يعد علاج الورم الأرومي الدبقي صعبًا؟
يظل الورم الأرومي الدبقي أحد أكثر أورام الدماغ الأولية فتكًا. ولا تزيد العلاجات الحالية من بقاء المرضى إلا بشكل طفيف. التحديات الرئيسية:
- عدم تجانس الورم: يتكون الورم الأرومي الدبقي من العديد من أنواع الخلايا، مما يجعل من الصعب استهدافها جميعًا بشكل فعال.
- تغيرات جينية قليلة: يفتقر الورم إلى أهداف دوائية مهمة.
- البيئة المثبطة للمناعة: يعمل الورم على قمع الاستجابة المناعية للجسم.
- حاجز الدم الدماغي: معظم الأدوية غير قادرة على اختراق الدماغ.
كيف تم اكتشاف الجليوسيدين؟
في دراسة نشرت في مجلة Nature بعنوان "الجليوسيدين هو دواء أولي يحاكي النيكوتيناميد ويستهدف الورم الأرومي الدبقي"، أجرى الفريق فحصًا عالي الإنتاجية لأكثر من 200 ألف مركب كيميائي على خلايا الورم الأرومي الدبقي لدى الفئران.
وقد تبين أن الجليوسيدين هو مركب سام بشكل انتقائي لخلايا الورم الدبقي ولكنه آمن للخلايا السليمة.
آلية عمل الجليوسيدين
لتوضيح آلية العمل، استخدم الباحثون تقنية فحص كريسبر-كاس9 لتحديد الجينات التي تؤثر على فعالية الجليوسيدين ضد الورم الأرومي الدبقي. ووجدوا أن الجليوسيدين:
- يقوم بمنع إنزيم IMP dehydrogenase 2 (IMPDH2)، الذي يشارك في تخليق نيوكليوتيدات الجوانين.
- وهذا يؤدي إلى:
- اختلال توازن النوكليوتيدات
- الإجهاد أثناء تكرار الحمض النووي،
- موت الخلايا السرطانية.
الجليوسيدين دواءٌ مُساعد يُنشَّط في الجسم. بمجرد تنشيطه، يُشكِّل شكلاً يُسمى جليوسيدين أدينين ثنائي النوكليوتيد (GAD)، والذي يرتبط بـ IMPDH2 ويُعطِّل وظيفته.
الفعالية في نموذج الفأر
في التجارب التي أجريت على الفئران، أظهر الجليوسيدين القدرة على:
- اختراق حاجز الدم الدماغي.
- إبطاء نمو الورم.
- تمديد البقاء على قيد الحياة.
تم الحصول على نتائج مهمة بشكل خاص عندما تم دمج الجليوسيدين مع عقار تيموزولوميد الكيميائي (الذي يعزز التعبير عن إنزيم NMNAT1، الذي يشارك في تنشيط الجليوسيدين).
فوائد الجليوسيدين
- السلامة: لم تظهر على الفئران أي خسارة في الوزن، أو تغيرات في الأعضاء الرئيسية، أو مشاكل في الجهاز المناعي.
- فعالية عالية: أدى الجمع بين الجليوسيدين وتيموزولوميد إلى تحسن كبير في معدلات البقاء على قيد الحياة.
خاتمة
يُظهر الجليوسيدين إمكاناتٍ كنهجٍ علاجيٍّ جديدٍ لعلاج الورم الأرومي الدبقي. وتُعدّ تجاربه الناجحة على الفئران مُرشّحًا واعدًا للتجارب السريرية المستقبلية.
